Definicja geometrii molekularnej
Różne / / January 11, 2022
Definicja pojęciowa
To struktura cząsteczki decyduje o trójwymiarowym rozmieszczeniu tworzących ją atomów w przestrzeni.

Inżynier chemiczny
Geometrie molekularne są obecnie definiowane na podstawie Teoria odpychania par elektronicznych warstwy Walencji (TRPECV). Ta teoria pozwala przewidzieć zachowanie chemiczny substancji (w szczególności kowalencyjnych) i pomaga zrozumieć dystrybucja elektronika, prowadząca do geometria z cząsteczka. To z kolei pozwala nam zrozumieć wiele właściwości, które nabywają substancje.
Ta teoria opiera się na szeregu fundamentalnych filarów, które przeanalizujemy, a następnie spróbujemy je zrozumieć podanie ćwiczyć. Przede wszystkim elektrony związane i niezwiązane (walencyjne) są uważane za morze elektronów, które dzięki posiadają ten sam rodzaj ładunku, odpychają się nawzajem, więc zawsze będą znajdować się jak najdalej od centralnego atomu cząsteczka.
Po drugie, to „morze” elektronów lub „chmura elektronów” tworzy obszary o dużej gęstości elektronów, które są utworzone w wiązaniach, w których elektrony są wspólne, lub w parach elektronów, które nie są wspólne. Z kolei tworzone wiązania mogą być pojedyncze, podwójne, a nawet potrójne.
Wreszcie dla decydować się geometria molekularna, bardzo pomocne jest posiadanie struktury Lewisa, w której obliczona zostanie ilość gęstości elektronów wokół centralnego atomu, co da wskazanie od nazwy swojej geometrii i kształtu, jaki przybiera cząsteczka trójwymiarowo.
Należy zauważyć, że te gęstości będą rozmieszczone jak najdalej od siebie, aby przyjąć najbardziej stabilną strukturę i gdzie będzie mniej odpychania. W ten sposób najpierw identyfikuje się geometrię elektronową, a następnie geometrię molekularną.
Sześć poziomów gęstości
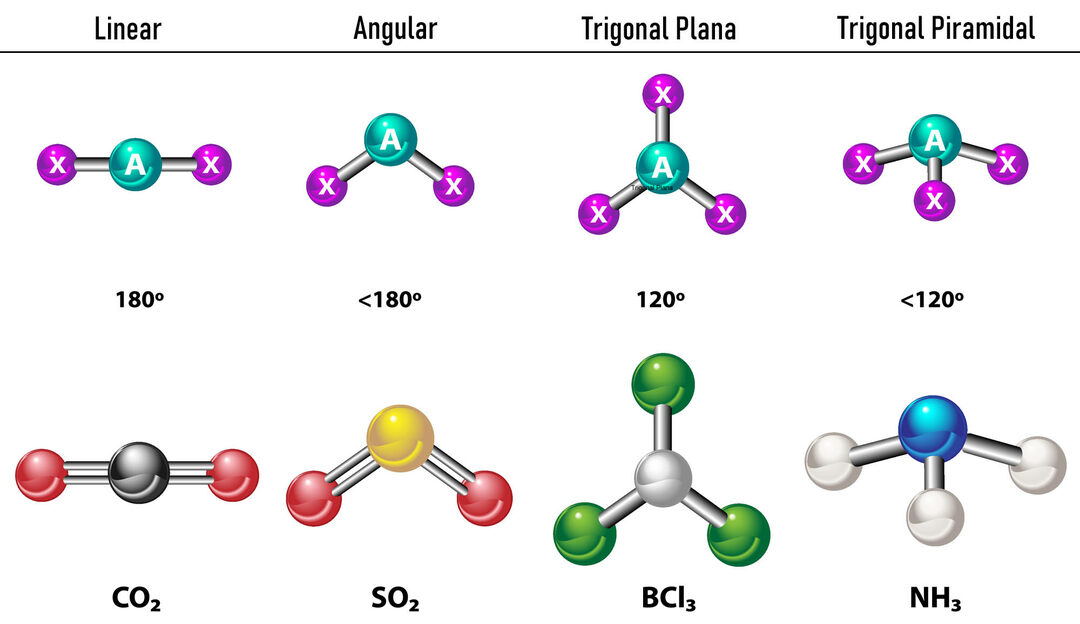
W przypadku, gdy wokół centralnego atomu występują dwie gęstości elektronowe, wiązania będą znajdować się tak daleko od siebie między nimi, to znaczy 180º od siebie, a zatem ich geometria elektronowa jest liniowa i molekularnie jest również liniowa.
W przypadku, gdy wokół centralnego atomu istnieją trzy gęstości elektronowe, istnieją dwie opcje: trzy wiązania lub dwa wiązania i jedna niezwiązana para. Jeśli istnieją trzy wiązania, geometria elektronowa jest Płaski trójkątny, z kątami 120º między wiązaniami a geometrią molekularną, ma tę samą nazwę. Teraz, jeśli jest para niezwiązana, odpychają się więcej intensywność że związane ładunki mają zatem tendencję do ściskania kątów wiązania. Kąt między wolną parą a każdym wiązaniem wynosi 120º, a geometria elektronowa to płaszczyzna trygonalna, podczas gdy geometria molekularna to kątowa.
W przypadku, gdy wokół centralnego atomu występują cztery gęstości elektronowe, geometria elektronowa jest czworościenna. Jeśli wszystkie cztery pary elektronów są związane, ich geometria molekularna jest zbieżna z geometrią elektronową, a kąt wiązania wynosi 109,5º. Teraz, jeśli jedna z par jest wolna, kąt wiązania zmniejsza się (107º), a geometria molekularna jest typu Piramida Trygonalna. Wreszcie, jeśli dwie są wolnymi parami, a dwie są połączone, kąt wiązania wynosi 104,5º, podczas gdy nazywa się geometrię molekularną Kątowy.
Gdy gęstość elektronów wokół centralnego atomu wynosi pięć, nazywa się to a Trygonalna bipiramida jego elektroniczna geometria. Jeżeli wszystkie obciążenia są połączone, to pomiędzy ogniwami położonymi pod równikiem występują kąty 120°C, a pomiędzy osiowymi i równikowymi kąty 90°. Teraz geometria molekularna jest również nazywana bipiramidą trygonalną, podczas gdy mając cztery połączone pary i jedną wolną parę, geometria molekularna jest zniekształcona, tworząc dobrze znaną "biegun”, Nazywa się tam Zniekształcony czworościan. Natomiast jeśli dwie z pięciu par elektronów są wolne, a trzy z nich są związane, ma geometrię w kształcie litery „T” i swoją nazwę zawdzięcza właśnie swojej budowie. Wreszcie, jeśli jest odwrotnie, trzy wolne pary i dwa ładunki związane, geometria molekularna jest liniowa.
Wreszcie, wokół centralnego atomu występuje sześć gęstości elektronów i powstaje ośmiościan, stąd jego nazwa w geometrii elektronowej. Podobnie geometria molekularna jest nazywana, jeśli wszystkie jej pary są połączone. Jeśli masz pięć połączonych par i jedną wolną parę, geometrią molekularną jest piramida o podstawie kwadratowej. Jeśli masz cztery związane pary i dwie wolne pary, geometria molekularna to Kwadratowe mieszkanie.
Rysunek: słodka natura
Tematy w geometrii molekularnej


