30 przykładów sprzedaży binarnej
Przykłady / / November 09, 2023
The sole binarne (sole obojętne) powstają, gdy metal i niemetal łączą się. Czy związki chemiczne składa się tylko z dwóch pierwiastki chemiczne. Na przykład: chlorek sodu (NaCl) i bromek potasu (KBr).
- Zobacz też: Metale i niemetale
Przykłady soli binarnych
- Chlorek sodu (NaCl)
- Chlorek żelaza(II) (FeCl2)
- Chlorek żelaza(III) (FeCl3)
- Siarczek kobaltu(II) (CoS)
- Siarczek kobaltu(III) (Co2Tak3)
- Siarczek ołowiu(II) (PbS)
- Siarczek ołowiu(IV) (PbS2)
- Chlorek wapnia (CaCl2)
- Fluorek sodu (NaF)
- Chlorek litu (LiCl)
- Chlorek strontu (SrCl2)
- Chlorek baru (BaCl2)
- Chlorek glinu (AlCl3)
- Siarczek magnezu (MgS)
- Chlorek rubidu (RbCl)
- Bromek wapnia (CaBr2)
- Siarczek potasu (K2S)
- Bromek magnezu (MgBr2)
- Siarczek cynku (Zn2S)
- Bromek litu (LiBr)
- Chlorek niklu (NiCl2)
- Chlorek uranu(III) (UCl3)
- Bromek srebra (AgBr)
- Jodek srebra (AgI)
- Bromek potasu (KBr)
Nazewnictwo soli binarnych
Według tradycyjnej nomenklatury sole binarne nazywa się poprzez wpisanie nazwy pierwiastka niemetalicznego z końcówką -ide. Z drugiej strony nazwa pierwiastka metalicznego jest zapisywana zgodnie z jego stopniem utlenienia:
- Dla najniższego stopnia utlenienia zapisuje się go z końcówką -oso. Na przykład: chlorek żelazawy (FeCl2), gdzie żelazo ma stopień utlenienia 2+.
- W przypadku najwyższego stopnia utlenienia jest on zapisywany z końcówką -ico. Na przykład: chlorek żelazowy (FeCl3), gdzie żelazo ma stopień utlenienia 3+.
Według Nomenklatury Systematycznej sole binarne nazywa się poprzez wpisanie nazwy pierwiastka niemetalicznego z przedrostkiem wskazującym ilość atomy tego pierwiastka w związku. Dodatkowo w nazwie elementu niemetalicznego umieszczana jest końcówka –uro. Następnie umieszczana jest nazwa elementu metalicznego. Na przykład: dichlorek magnezu (MgCl2) i trójchlorek żelaza (FeCl3).
Według nomenklatury Stocka, sole binarne nazywa się poprzez wpisanie nazwy pierwiastka niemetalicznego z końcówką -ide. Następnie umieszczana jest nazwa pierwiastka metalicznego i jego stopień utlenienia zapisany cyframi rzymskimi i w nawiasach. Na przykład: chlorek żelaza(II) (FeCl2) i siarczek kobaltu (III) (Co2Tak3).
Zastosowania soli binarnych
- Stosowane są jako czynniki chłodnicze w przemyśle spożywczym i farmaceutycznym. Na przykład: chlorek wapnia (CaCl2).
- Stosowane są do zabezpieczania powierzchni metalowych przed korozją. Na przykład: fluorek sodu (NaF).
- Stosowane są do regulacji wilgotności w przemyśle papierniczym i budowlanym. Na przykład: chlorek wapnia (CaCl2).
- Wykorzystuje się je w przemyśle szklarskim do usuwania zanieczyszczeń. Na przykład: czterochlorek krzemu (SiCl4).
- Wykorzystuje się je jako składniki do gotowania. Na przykład: chlorek sodu (NaCl).
Właściwości fizyczne soli binarnych
- Mają wysoką temperaturę topnienia, ponieważ są zbudowane z wiązania jonowe.
- Przewodzą prąd elektryczny po rozpuszczeniu lub stopieniu.
- Najpopularniejsze sole mają niską twardość.
- Nie są ściśliwe.
- Większość może rozpuścić się w wodzie.
Jak otrzymuje się sole binarne?
Sole binarne można otrzymać w wyniku następujących reakcji chemicznych:
Reakcja metalu z niemetalem. Na przykład: reakcja pomiędzy sodem (Na) i dichlorkiem (Cl2) wytwarza chlorek sodu (NaCl).
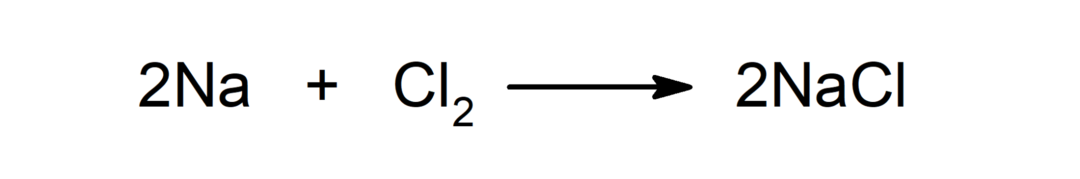
Reakcja metalu z kwasem. Na przykład: Reakcja pomiędzy potasem (K) i kwasem chlorowodorowym (HCl) wytwarza chlorek potasu (KCl) i diwodór (H2).
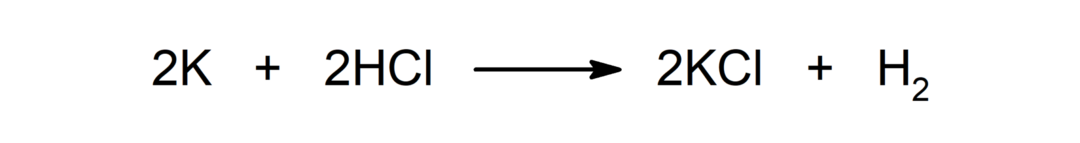
Reakcja pomiędzy kwasem i zasadą. Na przykład: W wyniku reakcji kwasu solnego (HCl) i wodorotlenku sodu (NaOH) powstaje chlorek sodu (NaCl) i woda (H2ALBO).
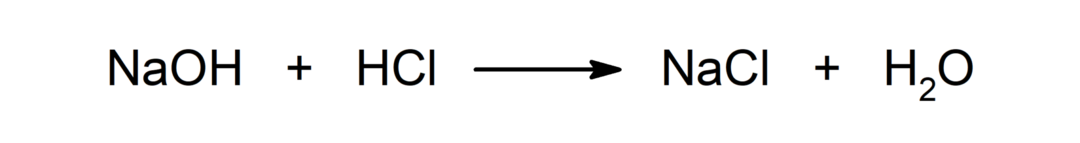
Postępuj zgodnie z:
- sole tlenowe
- sole obojętne
- sole kwasowe
Bibliografia
- Cerón Villalba, A., Novoa Ramírez, C. S. i Alpizar Juárez, E. (2020). Film z nomenklaturą 1: sole binarne i reakcja chemiczna.
- Acurio Arias, M. V. i Delgado Méndez, M. I. (2022). Przewodnik edukacyjny oparty na grach dla „związków binarnych” w chemii w szkole średniej w Jednostce Edukacyjnej „Herlinda Toral” (Praca licencjacka, Narodowy Uniwersytet Pedagogiczny).
- Cabrera, M. J. H. (2005). Badanie z pierwszych zasad właściwości elektronowych i strukturalnych związków binarnych i trójskładnikowych (Rozprawa doktorska, Uniwersytet La Laguna).



