Przykłady reakcji endotermicznych
Przykłady / / November 09, 2023
A reakcja endotermiczna Jest to reakcja pochłaniająca energię z ośrodka w postaci ciepła. W reakcjach tych, aby reagenty przekształciły się w produkty, konieczne jest pochłonięcie przez nie ciepła, co powoduje, że produkty mają większą energię niż reagenty, z których powstały. Oto kilka przykładów reakcji endotermicznych: fotosynteza i elektroliza wody.
- Zobacz też: Reakcje chemiczne
Przykłady reakcji endotermicznych w życiu codziennym
Niektóre z głównych reakcji endotermicznych to:
Produkcja ozonu w atmosferze. Ozon powstaje w atmosferze, gdy tlen cząsteczkowy (O2) pochłania promieniowanie ultrafioletowe i ulega rozkładowi. Następnie atom tlenu (O) może oddziaływać z inną cząsteczką tlenu (O2) i tworzą ozon ( O3).

Elektroliza wody. Jest to proces, w ramach którego jest on stosowany energia elektryczna do wody w celu rozdzielenia jej na dwa składniki, wodór (H) i tlen (O).
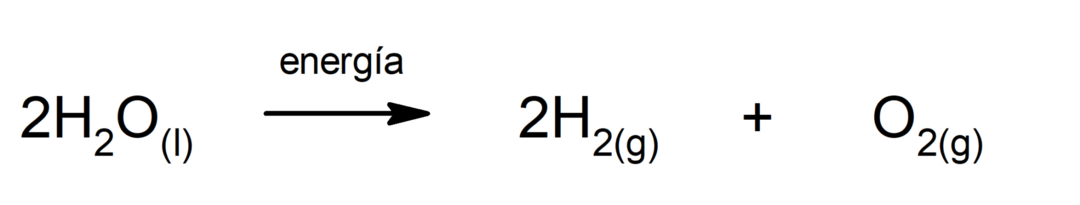
Fotosynteza. Jest to reakcja chemiczna, w wyniku której następuje wchłanianie energia słoneczna, dwutlenek węgla (CO2) ulega przemianie w glukozę. Reakcja ta stanowi główną drogę odżywiania roślin.
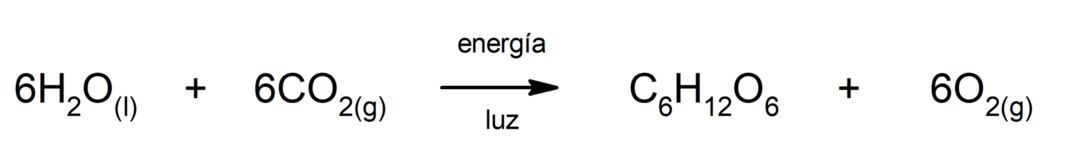
Produkcja siarczku żelaza(II).. Aby doszło do reakcji siarki z żelazem, konieczne jest dostarczenie energii w postaci ciepła.
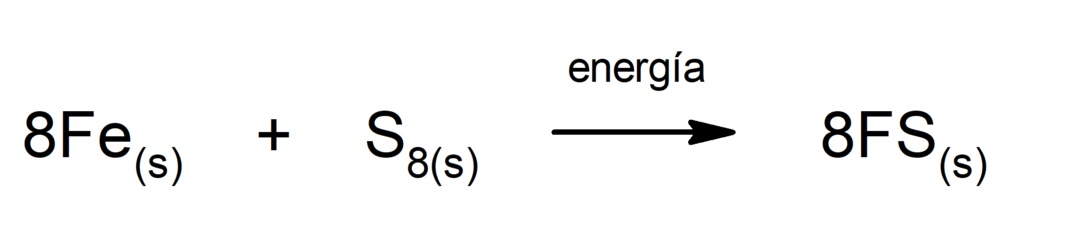
Rozkład dwutlenku węgla (CO2). Rozkład CO2 W wysokich temperaturach wytwarza tlenek węgla (CO) i tlen (O2).
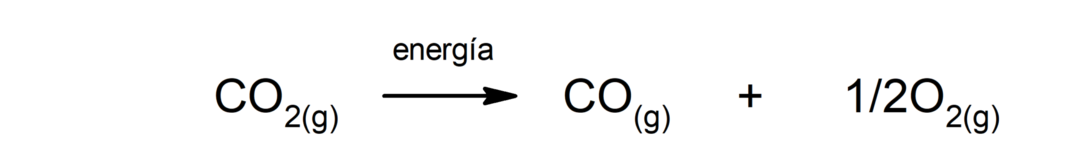
Rozkład węglanu wapnia (CaCO3). Węglan wapnia rozkłada się pod wpływem ciepła, tworząc tlenek wapnia (CaO) i dwutlenek węgla (CO2).
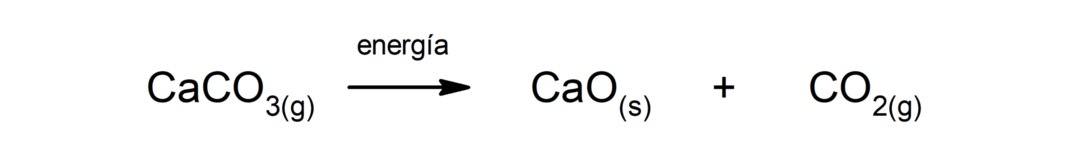
Różnica między reakcją endotermiczną i egzotermiczną
Główna różnica między reakcjami endotermicznymi i egzotermicznymi polega na tym, że reakcje endotermiczne pochłaniają ciepło, podczas gdy reakcje egzotermiczne uwalniają ciepło.
Ponadto reakcje endotermiczne charakteryzują się wzrostem entalpii, podczas gdy reakcje egzotermiczne są związane ze spadkiem entalpii.
Entalpia jest wielkością termodynamiczną, która określa przepływ energii cieplnej pod stałym ciśnieniem podczas reakcji chemicznej. Jest ona reprezentowana przez literę H, a jej zmienność jest jednym z głównych wskaźników określających, czy reakcja chemiczna jest endotermiczna, czy egzotermiczna.
- Jeżeli reakcja chemiczna ma zmianę entalpii większą od zera (ΔH > 0) jest endotermiczny.
- Jeżeli reakcja chemiczna ma zmianę entalpii mniejszą od zera (ΔH < 0) jest egzotermiczny.
Postępuj zgodnie z:
- Zjawiska fizykochemiczne
- Chemia w życiu codziennym
- Chemia w życiu codziennym
- Chemia organiczna i nieorganiczna
Bibliografia
- Soto-Córdoba, S. (2016). Reakcje endotermiczne. Repozytorium technologii Instytut Technologiczny Kostaryki.
- Corominas, J. (2017). Reakcje chemiczne życia codziennego. Alembik, (90), 8-26.
- Sanchez, M. T. M. i Sanchez, M. M. (2002). Eksperymentalne badanie reakcji endotermicznych dla studentów ESO. Roczniki chemii RSEQ, (4), 36-39.



