Przykład związków heterocyklicznych
Chemia / / July 04, 2021
Istnieją cykliczne związki chemiczne, które składają się wyłącznie z atomów węgla, z ich wartościowością uzupełnioną atomami wodoru. Takie związki nazywane są homocykliczny. ZA związek heterocykliczny Jest to substancja organiczna, która zawiera pierścień utworzony przez więcej niż jeden rodzaj atomów; Oprócz węgla najbardziej rozpowszechnione są azot, tlen i siarka. Te różne atomy nazywają się heteroatomy.
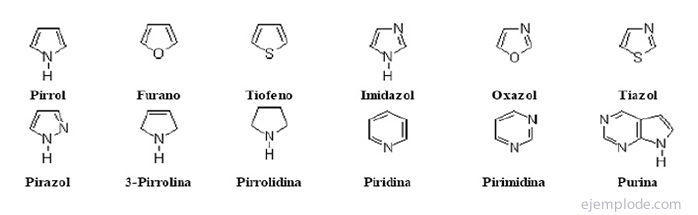
Powyższe związki nazywane są nazwami trywialnymi, czyli nazwami handlowymi, które nie dostarczają informacji strukturalnych o cząsteczce, ale zostały zaakceptowane i uznane przez IUPAC.
Klasyfikacja związków heterocyklicznych
Związki heterocykliczne są klasyfikowane według dwóch głównych kryteriów: Rodzaj linków który zawiera (jeśli są pojedyncze lub podwójne) i in Liczba dzwonków która ma.
Dla niego Rodzaj linków zawierają, są klasyfikowane do Związki alicykliczne, gdy jego wiązania są pojedyncze lub podwójne, ale geometria ma 5 atomów lub mniej; Tak Związki aromatyczne, kiedy mają pierścień Benzen w swojej strukturze, czyli na jakiej podstawie istnieje heteroatom.
Dla niego Liczba dzwonków że jest właścicielem, można go sklasyfikować jako Monocykliczny, bicykliczny, Trójpierścieniowy, a w stosownych przypadkach dodawany jest kolejny prefiks numeryczny.
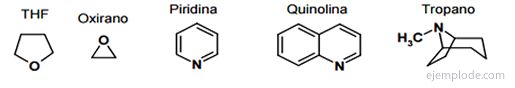
Związki heterocykliczne o trzech atomach
Istnieją pierścienie heterocykliczne o trzech atomach, które są bardzo reaktywne ze względu na łatwość ich otwierania przez nukleofile, zwane epoksydami i azyrydynami. Są cennymi materiałami wyjściowymi w syntezie organicznej.
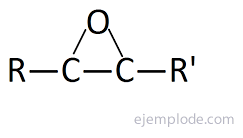
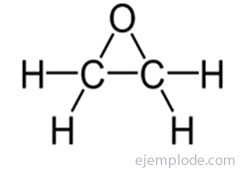
Epoksydy, zwane również Oxyranami, to cykliczne etery, które składają się z połączenia atomu tlenu z dwoma kolejnymi atomami węgla, które z kolei tworzą część łańcucha wiązań kowalencyjnych. Jest to struktura trójkątna, której podstawą jest węgiel, a wierzchołkiem tlen. Są to bezbarwne ciecze, rozpuszczalne w alkoholach, eterach i benzenie. Najprostszym terminem jest Tlenek etylenu, nazywany również Epoksyetan lub Oksiran. Jego synteza jest częstsza przez zerwanie podwójnego wiązania między atomami węgla kwasami zawierającymi kilka atomów tlenu. Są one nazwane, wskazując pozycje, w których atom tlenu jest przyłączony, po których następuje przedrostek „Epoksyd-” i nazwa węglowodoru, który go obsługuje.
Obecne w polimerach znajdują zastosowanie jako tworzywa sztuczne na konstrukcje, powłoki i kleje. Ponadto mają istotny udział w produkcji materiałów ściernych, materiałów ciernych, w przemyśle włókienniczym, w żeliwie, filtrach i lakierach. Również do wełny mineralnej, impregnatów, materiałów drzewnych, pianek, proszków formierskich. W przemyśle spożywczym epoksydy stosuje się jako chemiczne środki sterylizujące w żywności o niskiej wilgotności i aseptycznych materiałach opakowaniowych.
AzyrydynyPodobnie jak epoksydy mają strukturę trójkątną, tyle że heteroatomem jest azot. Są to ciecze bezbarwne, rozpuszczalne w wodzie, trujące i o zapachu amoniaku. Mają specjalną właściwość fizyczną, która jest przypisywana geometrii pierścienia; atom azotu ma znacznie wyższą barierę dla inwersji piramidalnej niż inne aminy monocykliczne i acykliczne. Przydatną procedurą syntezy azyrydyny jest piroliza lub fotoliza 1,2,3-triazolin. Związki te łatwo wytwarza się w reakcji azydków z alkenami w 1,3-dipolarnej reakcji cykloaddycji.
Przez odparowanie azyrydyna może osiągnąć szkodliwe stężenia w powietrzu w temperaturze 20 ° C. Reaguje z utleniaczami i jest podatny na spalanie, tworząc tlenki azotu.

Związki heterocykliczne o pięciu atomach
Najprostsze z pięcioatomowych związków heterocyklicznych to: Pyrrol, z heteroatomem azotu, Furan, tlen heteroatomowy i Tiofen, Heteroatom siarki.
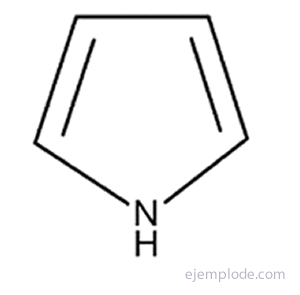
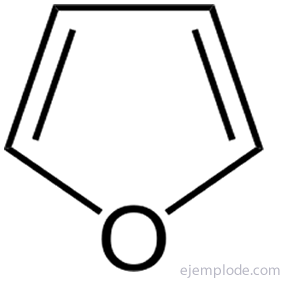
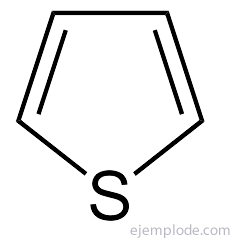
Pierścień pirolu jest podstawową jednostką układu porfirynowego występującego na przykład w chlorofilu i hemoglobinie.
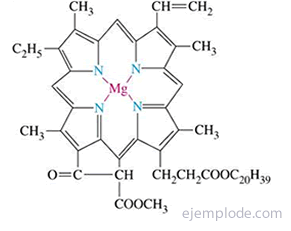
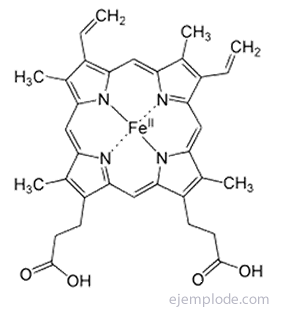
Pyrrol znajduje się w niewielkich ilościach w smole węglowej, podobnie jak Tiofen. Przez frakcyjną destylację smoły tiofen (temperatura wrzenia 84 ° C) jest zbierany razem z benzenem (temperatura wrzenia 80 ° C).
Najłatwiejszym sposobem uzyskania furanu jest dekarbonylacja (usuwanie tlenku węgla) furfuralu (furfuraldehyd), który z kolei jest otrzymywany przez obróbkę łusek owsa lub ryżu lub kolb kukurydzy kwasem wrzący chlorowodorek.
Związki heterocykliczne o sześciu atomach
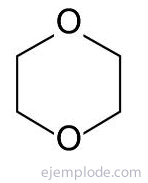
Spośród terminów nasyconych jednym z najważniejszych jest 1,4 dioksan lub dioksan, który jest cieczą bezbarwny, o charakterystycznym zapachu, którego para jest gęstsza od powietrza i może rozprzestrzeniać się wzdłuż Ja zwykle. W kontakcie z powietrzem może tworzyć wybuchowe nadtlenki. Reaguje z utleniaczami i mocnymi kwasami. Reaguje gwałtownie z niektórymi katalizatorami.
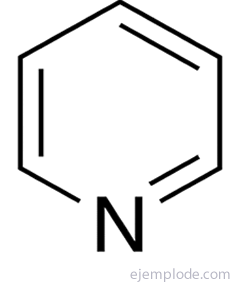
Spośród nienasyconych heterocykli jednym z najważniejszych terminów jest pirydyna, która składa się ze struktury pierścienia benzenowego z heteroatomem azotu. Jest to konfiguracja prekursora wielu ważnych cząsteczek, takich jak składniki kwasu dezoksyrybonukleinowego.
Systematyczna nomenklatura związków heterocyklicznych
W przypadku związków heterocyklicznych pierścienia (monocyklicznego), odpowiednią nomenklaturę uzyskuje się przez połączenie przedrostka i przyrostka odpowiedniego dla danego pierwiastka, zgodnie z następującymi zasadami:
prefiks oznacza naturę heteroatomu, the Korzeń wyjaśnia rozmiar pierścionka, a Przyrostek określa stopień nienasycenia. Kolejność, której należy przestrzegać w nomenklaturze to Prefiks-Root-Suffix.
natura heteroatomu jest oznaczony przedrostkami, takimi jak okso dla tlenu, wujek dla siarki lub aza do azotu.
krotność heteroatomów jest oznaczony dodatkowym przedrostkiem, takim jak di, tri, tetra itp.
Gdy istnieją dwa lub więcej różnych heteroatomów, są one nazywane z następującym priorytetem: O> S> N; na przykład oksazo dla tlenu i azotu, Tiaz do siarki i azotu, Oxatio dla tlenu i siarki.
Rozmiar pierścionka jest oznaczony przez właściwą łodygę.
stopień nienasycenia jest określony przyrostkiem. Należy zauważyć, że sufiks jest nieznacznie zmodyfikowany, gdy w pierścieniu heterocyklicznym nie ma azotu.
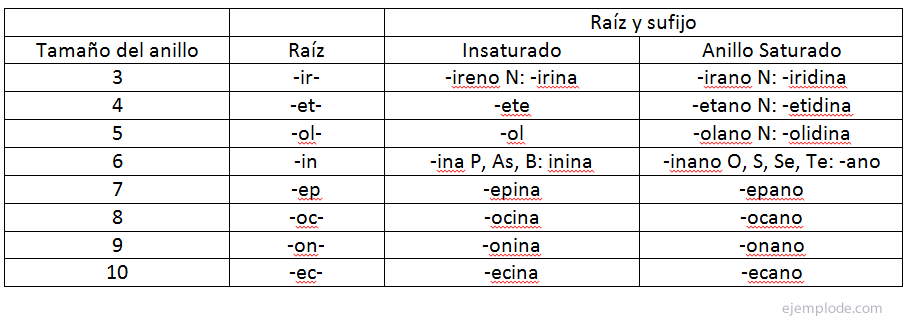
Numeracja pierścienia rozpoczyna się od heteroatomu o najwyższym priorytecie i jest kontynuowana wokół pierścienia, przypisując najniższe możliwe numery innym heteroatomom lub podstawnikom.
Gdy układ, który ma maksymalną liczbę wiązań podwójnych nadal zawiera nasycony atom w pierścieniu, jest to oznaczone liczbą wskazującą jego pozycję i literą H- wielkie kursywa jako przedrostek.


