10 exemplos de misturas de gases
Miscelânea / / July 04, 2021
Misturas de substâncias gasosas Eles são alguns dos mais fáceis de alcançar, pois é muito possível que substâncias que se encontram neste estado de agregação sejam misturadas. Por exemplo: Mistura de néon, argônio e xenônio, inseticida em aerossol, ar e hélio.
Praticamente todos os gases podem ser combinados ilimitadamente, é claro, condicionados por alguns química, física e fundamentalmente relacionada aos aspectos de segurança do usuário que manipula. Como os diferentes tipos de misturas que se estabelecem entre as substâncias, as misturas de gases eles também têm propriedades que são exclusivas deles.
O estudo de misturas efervescentes é geralmente tão útil quanto o de gases em seu estado puro: o mesmo conhecimento sobre o ar que está presente em a atmosfera seria impossível se não fosse pelo conhecimento das proporções e comportamentos dos gases mistos.
Desta forma, é essencial conhecer alguns caracteristicas de misturas de gases, como a propriedade de pressão parcial (que é exercida por cada um dos gases dentro do mistura) e da fração molar (razão entre o número de moles de um componente gasoso com o da mistura total refrigerante). Os moles expressam a quantidade de gás na mistura.
O Lei de Dalton afirma que a pressão total de uma mistura de gases é igual à soma das pressões parciais de cada um dos gases individuais que participam dele (isto está sujeito aos gases não reagirem entre Sim). A pressão parcial é entendida aqui como aquela que cada um dos gases exerceria se fosse encontrado apenas no mesmo recipiente e nas mesmas condições de temperatura. A) Sim:
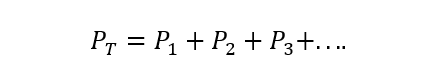
Onde PT é a pressão total e P1, P2 E P3 são as pressões parciais dos gases hipotéticos 1, 2 e 3 na mistura de gases.
Usando a Lei de Dalton, uma expressão foi desenvolvida para calcular o pressão parcial de um gás em uma mistura gasosa se conhecermos sua pressão total e sua fração molar.
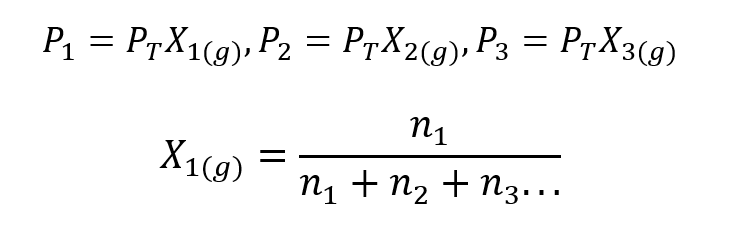
Onde X1, X2 Y X3 são as frações molares dos gases hipotéticos 1, 2 e 3 na mistura de gases, e n1, n2 Y n3 são as quantidades de substância de cada um desses gases na mesma mistura.
Uma das propriedades principais dos componentes nas misturas é a concentração, que pode ser expressa em unidades diferentes. No caso das misturas gasosas, a concentração de seus componentes pode ser expressa em ppm (partes por milhão), unidade referida ao seu volume. Ou seja, uma certa quantidade de ppm de um componente em uma mistura de gases é a razão entre o volume dessa certa quantidade e o volume de cada milhão de unidades da mistura.
É importante notar que ppm de um gás dependem da temperatura e pressão do gás. Por este motivo, para calcular o ppm de um gás, normalmente são utilizadas condições normais de pressão e temperatura. (CNPT), que dão um estado normal a 0 graus Celsius de temperatura e 1013 hectopascais (1 bar) de Pressão. Se essas condições não forem usadas, você deve especificar quais serão usadas.
Pode servir a você:
Exemplos de misturas de gases
A lista a seguir contém misturas de gases, especificando os elementos que aparecem na mistura:
- Ar (mistura de 21% de oxigênio e 79% de nitrogênio, além de outros gases em pequenas proporções)
- Cronigón (mistura de 99% de argônio e 1% de oxigênio)
- Trimix (mistura de oxigênio, nitrogênio e hélio)
- Mistura de néon, argônio e xenônio
- Mistura de 85% de metano, 9% de etano, 4% de propano e 2% de butano.
- Hexafluoreto de enxofre e ar
- Inseticida aerossol
- Ar e hélio
- Nitrox (mistura de ar, enriquecido em oxigênio e nitrogênio)
Siga com:



