50 exemplos de soluções
Miscelânea / / July 04, 2021
As soluções são um dos tipos de misturas que existem. Os componentes que constituem uma solução não reagem quimicamente, embora as propriedades físicas desses componentes possam ser modificadas ao se tornarem parte da solução. Por exemplo: fumaça, amálgama, café com leite.
Para uma mistura ser uma solução, deve ser homogêneo Y uniforme, ou seja, que os componentes misturados não podem ser distinguidos a olho nu e que, além disso, a proporção entre o soluto (substância que aparece em menor quantidade) e o solvente (substância que aparece em maior quantidade) permanece aproximadamente inalterada em qualquer volume que seja retirado da solução. A proporção do soluto na solução ou no solvente é chamada de "concentração" e normalmente a mesma solução pode ser preparada usando várias concentrações de soluto.
Soluções podem se formar entre substâncias que, antes de serem misturadas, estão em qualquer um dos diferentes estados de agregação. Existem soluções em praticamente todos os estados de agregação. Geralmente, o estado de agregação da solução é determinado pelo estado de agregação do solvente. Por exemplo:
É comum para presença de moléculas de soluto dentro de um solvente alteram as propriedades do próprio solvente. Por exemplo, os pontos de fusão e ebulição de dois compostos mudam quando esses compostos são misturados, assim como sua composição. densidades e cores.
O cientista francês Roult estudou este comportamento dos componentes nas soluções e também propôs sua lei principal (Lei de Roult), que afirma que a pressão de vapor parcial de cada componente na mistura de vapor em torno de uma solução ideal a partir de líquidos é igual à pressão parcial de cada componente puro vezes sua fração molar na solução. Uma solução ideal é considerada aquela em que as espécies químicas são muito semelhantes, portanto nenhuma variação na energia das interações entre elas é considerada. A equação fundamental da Lei de Roult é:
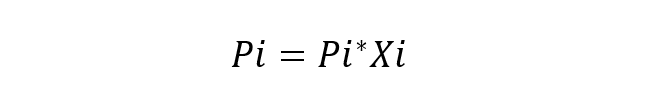
Onde:
- Pi é a pressão parcial do componente eu na mistura gasosa que envolve a solução.
- Pi * é a pressão do componente eu
- XI é a fração molar do componente eu em dissolução.
Obviamente, as pessoas estão em contato permanente com as soluções. O ar é uma dissolução de elementos em Estado gasoso: sua composição majoritária é dada pelo azoto (78%) e o restante é ocupado por 21% da oxigênio e 1% de outros componentes, embora essas proporções possam variar ligeiramente.
Exemplos de soluções
A lista a seguir inclui quarenta exemplos de soluções, destacando o estado de agregação em que cada uma se encontra, um soluto em um respectivo solvente.
- Ar (gás em gás). Uma composição de gases, onde o nitrogênio é mais abundante.
- Fumaça (sólido no gás). O ar está viciado pelo aparecimento de fumaça do fogo. É uma solução em que o ar atua como solvente.
- Ligas entre metais (sólido em sólido). Duralumínio é uma liga composta de alumínio, cobre, manganês, magnésio e silício.
- Poeira atmosférica (sólido no gás). A presença de sólidos (decompostos quase em uma unidade indivisível, mas finalmente sólidos) no gás é um exemplo de dissolução neste sentido.
- Aço (sólido em sólido). Liga entre o ferro e o carbono, com uma proporção muito maior do primeiro.
- Refrigerantes (gás no líquido). As bebidas carbonatadas têm uma dissolução de gases em um líquido.
- Amálgama (líquido no sólido). Eles são ligas de mercúrio dissolvidas em certos metais como ouro ou prata.
- Petróleo refinado (líquido em líquido). A combinação dos elementos que o compõem (a maioria é carbono) dá lugar a uma dissolução entre os líquidos.
- Butano no ar (gás em gás). Butano é um composto químico gasoso que pode ser armazenado em tubos, pronto para ser utilizado como combustível.
- Oxigênio na água do oceano (gás no líquido). A oxigenação da água do mar permite o desenvolvimento da vida aquática.
- Bebidas com teor alcoólico (líquido em líquido). São muito consumidos pelos humanos nas celebrações. Geralmente são soluções de etanol e sucos de frutas em concentrações controladas de álcool.
- Café com leite (líquido em líquido). Um líquido com maior teor recebe um pouco de outro, o que representa uma transformação de sua cor e sabor.
- Smog (gases em gases). A introdução de gases não típicos da atmosfera induz uma transformação do ar, que tem efeitos negativos nas sociedades que o respiram: quanto mais concentrado, mais prejudicial será.
- Sal na água (sólido em líquido). Muito utilizado para cozinhar.
- Sangue (líquido em líquido). O componente majoritário é o plasma (líquido) e nele aparecem outros elementos, entre os quais se destacam os glóbulos vermelhos.
- Amônia na água (líquido em líquido). Essa solução (que também pode ser transformada de gás em líquido) é funcional para muitos produtos de limpeza.
- Ar com vestígios de umidade (líquido no gás). O vapor de água está presente no ar devido ao aumento temperatura.
- Sucos em pó (sólido em líquido). O pó se dissolve em água e produz uma solução da cor de suco em pó.
- Hidrogênio em paládio (gás no sólido). O hidrogênio se dissolve muito bem em alguns metais.
- Vírus transportados pelo ar (sólido no gás). Como a poeira atmosférica, eles são unidades muito pequenas de um sólido que são transportadas por um gás.
- Mercúrio em prata (líquido no sólido). É um dos chamados “amálgamas”.
- Ele te (sólido em líquido). Um sólido de dimensões muito pequenas (os granitos do envelope) se dissolve na água.
- Água real (líquido em líquido). É uma composição de ácidos que permite dissolver diferentes metais, entre os quais aparece o ouro.
- Bronze (sólido em sólido). É a liga entre cobre e estanho.
- Limonada (líquido em líquido. Embora muitas vezes a mistura seja entre um sólido e um líquido, na verdade é um líquido presente naquele sólido, como o suco de limão.
- Água oxigenada (líquido em líquido). É uma solução de peróxido de hidrogênio (H2OU2) na água. É utilizado na desinfecção de feridas e na indústria cosmética.
- Latão (sólido em sólido). É a liga entre o cobre sólido e o zinco.
- Resfriamento de gelo (sólido em líquido). O gelo entra no líquido e o resfria, enquanto se dissolve. Se for introduzido na água, é o caso particular em que é a mesma substância.
- Solução fisiológica (líquido em líquido). A água atua como solvente e muitas substâncias líquidas atuam como soluto.
- Smoothies (sólidos em líquidos). Por meio de um processo de moagem, uma combinação de sólidos em líquidos é induzida.
Siga com:



