Definição de Geometria Molecular
Miscelânea / / January 11, 2022
Definição conceitual
É a estrutura de uma molécula que determina o arranjo tridimensional dos átomos que a compõem no espaço.

Engenharia Química
As geometrias moleculares são atualmente definidas com base na Teoria de Repulsão de Pares Eletrônicos da Camada Valenciana (TRPECV). Essa teoria permite prever o comportamento químico de substâncias (especificamente covalentes) e ajuda a entender o distribuição eletrônica, levando a geometria da molécula. Isso, por sua vez, nos permite compreender muitas das propriedades que as substâncias adquirem.
Esta Teoria assenta numa série de pilares fundamentais que iremos rever e depois tentar compreender a sua aplicativo prática. Em primeiro lugar, os elétrons ligados e não ligados (valência) são pensados como um mar de elétrons que, por possuem o mesmo tipo de carga, eles se repelem, então eles sempre estarão localizados o mais longe do átomo central do átomo. molécula.
Em segundo lugar, este "mar" de elétrons ou "nuvem eletrônica" forma áreas de alta densidade eletrônica, que são constituídos em ligações, onde os elétrons são compartilhados ou em pares de elétrons não compartilhados. Por sua vez, as ligações que se formam podem ser simples, duplas ou até triplas.
Finalmente, para decidir geometria molecular, é muito útil ter a estrutura de Lewis, onde a quantidade de densidades eletrônicas ao redor do átomo central será contada e isso dará indicação do nome de sua geometria e da forma que a molécula toma tridimensionalmente.
Ressalta-se que essas densidades serão localizadas o mais afastadas possível, de forma a adotar a estrutura mais estável e onde haja menos repulsão. É assim que se identifica primeiro a geometria eletrônica e depois a geometria molecular.
Seis níveis de densidade
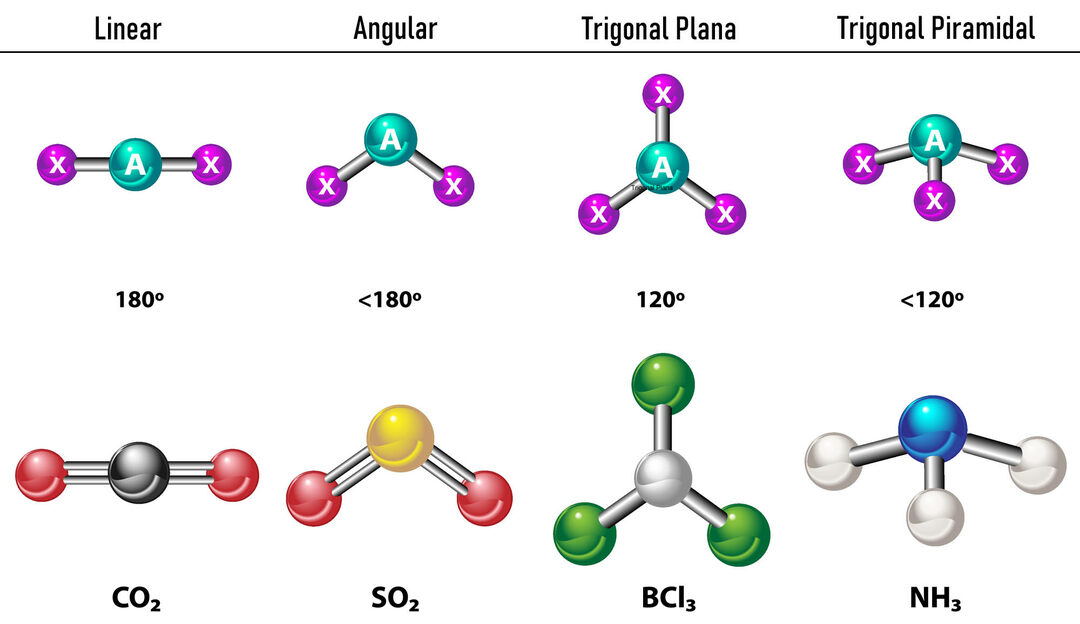
No caso de haver duas densidades eletrônicas ao redor do átomo central, as ligações estarão localizadas tão distantes entre si. entre eles, ou seja, 180º um do outro e, portanto, sua geometria eletrônica é linear e molecularmente também é linear.
No caso de haver três densidades eletrônicas ao redor do átomo central, há duas opções: três ligações ou duas ligações e um par não ligado. Se houver três ligações, a geometria eletrônica é Plano Trigonal, com ângulos de 120º entre ligações e geometria molecular leva o mesmo nome. Agora, se houver um par não ligado, eles se repelem com mais intensidade que as cargas ligadas, portanto, tendem a comprimir os ângulos de ligação. O ângulo entre o par livre e cada ligação é de 120º e a geometria eletrônica é Plano Trigonal enquanto a geometria molecular é Angular.
No caso de haver quatro densidades eletrônicas ao redor do átomo central, a geometria eletrônica é tetraédrica. Se todos os quatro pares de elétrons estão ligados, sua geometria molecular coincide em nome com sua geometria eletrônica e o ângulo de ligação é de 109,5º. Agora, se um dos pares estiver livre, o ângulo de ligação fica menor (107º) e a geometria molecular é do tipo Pirâmide Trigonal. Finalmente, se dois são pares livres e dois estão ligados, o ângulo de ligação é de 104,5º enquanto a geometria molecular é chamada Angular.
Quando as densidades eletrônicas ao redor do átomo central chegam a cinco, é chamado de Bipirâmide Trigonal sua geometria eletrônica. Se todas as cargas estiverem interligadas, há ângulos de 120º entre as ligações localizadas equatorialmente e de 90º entre as axiais com as equatoriais. Agora, a geometria molecular também é chamada de Bipirâmide Trigonal enquanto, tendo quatro pares ligados e um par livre, a geometria molecular é distorcida formando o conhecido "balancim”, Lá o nome que adquire é Tetraedro distorcido. Considerando que, se dois dos cinco pares de elétrons são livres e três deles estão ligados, ele tem uma geometria em forma de “T” e seu nome se deve justamente à sua estrutura. Finalmente, se for o inverso, três pares livres e duas cargas ligadas, a geometria molecular é linear.
Finalmente, existem seis densidades eletrônicas ao redor do átomo central e um octaedro é formado, daí seu nome em geometria eletrônica. Da mesma forma, a geometria molecular é nomeada se todos os seus pares estiverem ligados. Se você tiver cinco pares ligados e um par livre, a geometria molecular é Pirâmide de Base Quadrada. Se você tem quatro pares ligados e dois pares livres, a geometria molecular é Apartamento Quadrado.
Figura: Doce Natureza
Tópicos em Geometria Molecular


