50 exemplos de aldeídos e cetonas
Exemplos / / November 06, 2023
O aldeídos são compostos orgânicos que possuem em sua estrutura um grupo funcional carbonila (=C=O) que está ligado a uma cadeia de carbono e a um átomo de hidrogênio. Por exemplo: metanal (também chamado de formaldeído), etanal (também chamado de acetaldeído) e propanal (também chamado de propaldeído).
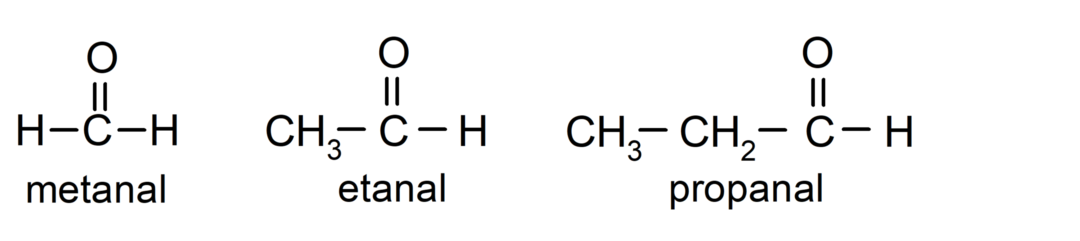
As cetonas São compostos orgânicos que possuem em sua estrutura um grupo carbonila ligado a dois átomos de carbono. Por exemplo: propanona (também chamada acetona), butanona e 2-pentanona.
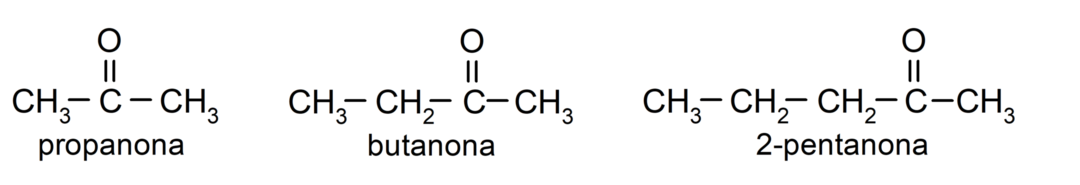
Diferenças entre aldeídos e cetonas
As principais diferenças entre aldeídos e cetonas são:
- Os aldeídos possuem em sua estrutura um grupo funcional carbonila localizado em uma extremidade terminal, enquanto as cetonas têm o grupo carbonila localizado em posições não terminais de seus estrutura.
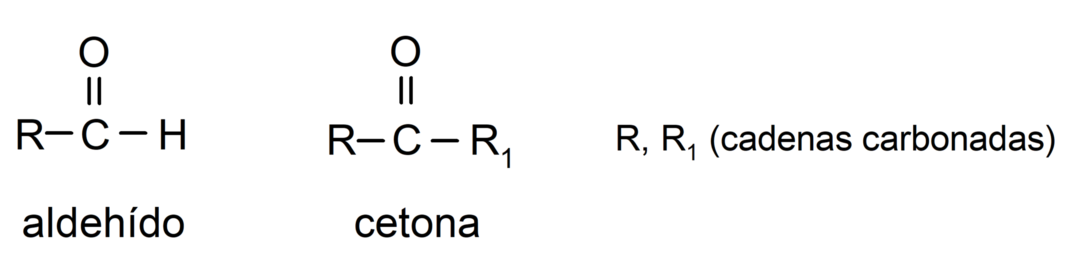
- Os aldeídos são oxidados pela reação com o reagente de Tollens, formando prata metálica. Eles também oxidam contra o reagente de Benedict, formando óxido cuproso. As cetonas não são oxidadas por nenhum dos reagentes.
- Os aldeídos são reduzidos a álcoois primários, enquanto as cetonas são reduzidas a álcoois secundários.
Propriedades físicas
Propriedades físicas dos aldeídos
As propriedades físicas dos aldeídos são muito diversas porque dependem da constituição da cadeia carbônica que está ligada ao grupo carbonila.
Alguns são:
- Os aldeídos mais solúveis em água são aqueles de tamanho menor, como metanal e etanal.
- Os aldeídos voláteis têm odores pungentes e até irritantes.
- O grupo carbonila lhes confere polaridade.
- Eles geralmente têm pontos de ebulição mais elevados do que compostos químicos de tamanho molecular semelhante.
Propriedades físicas das cetonas
As propriedades físicas das cetonas dependem de como se forma a cadeia de carbono ligada ao grupo carbonila.
- Muitas cetonas têm odores agradáveis.
- Sua solubilidade em água depende do tamanho da cadeia de carbono ligada ao grupo carbonila. Quanto menor a cadeia de carbono, mais solúvel será a cetona em água.
- O grupo carbonila lhes confere uma polaridade marcante.
- Eles têm pontos de ebulição bastante elevados em comparação com compostos químicos de tamanho molecular comparável.
Propriedades quimicas
Propriedades químicas dos aldeídos
Dentre as propriedades químicas dos aldeídos podemos encontrar:
Eles são oxidados para formar o ácido carboxílico correspondente, ou seja, o ácido formado terá o mesmo número de carbonos na cadeia de carbono que o aldeído que lhe deu origem. Por exemplo:
- Oxidação com reagente de Tollens (complexo de prata amoniacal em solução básica, [Ag (NH3)2]+) do etanal produz ácido etanóico e prata metálica.
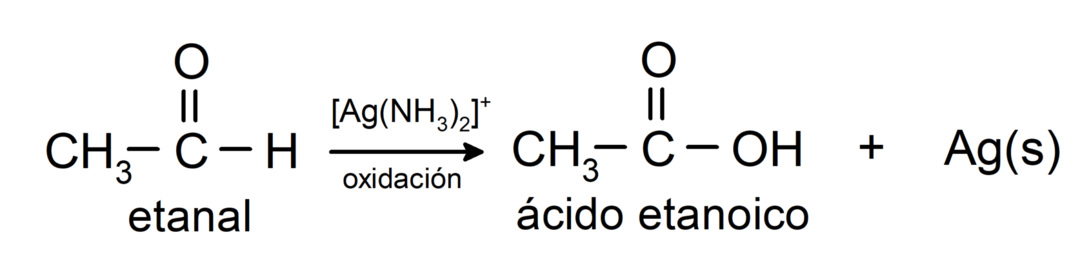
- A oxidação com reagente de Benedict (solução alcalina de sulfato de cobre) do etanal produz ácido etanóico e óxido cuproso.
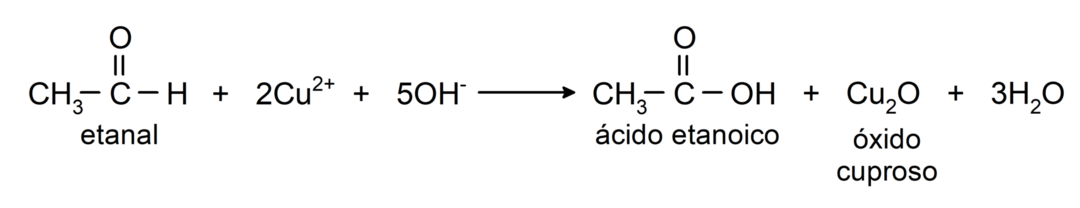
Eles sofrem reações de adição nucleofílica, isto é, adição de um nucleófilo ao grupo carbonila. Por exemplo:
- Adição de ácido cianídrico para formar cianidrinas ou cianidrinas.
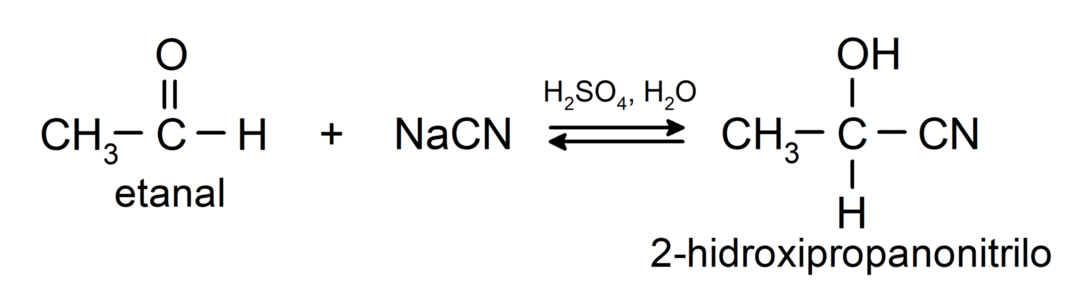
- Na presença de ácidos anidros, os álcoois são adicionados ao grupo carbonila dos aldeídos para formar acetais e hemiacetais.
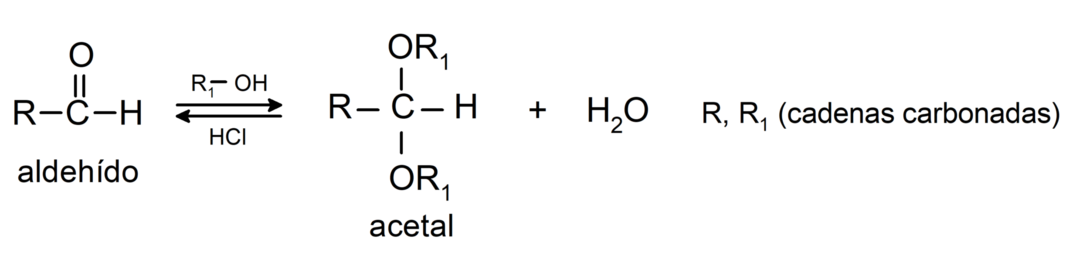
Eles sofrem reações de condensação aldólica. Nessas reações, a união de dois aldeídos ocorre na presença de hidróxido de sódio (NaOH) e do composto químico resultante é chamado aldol. Por exemplo:
- Reação de condensação do etanal na presença de NaOH diluído.
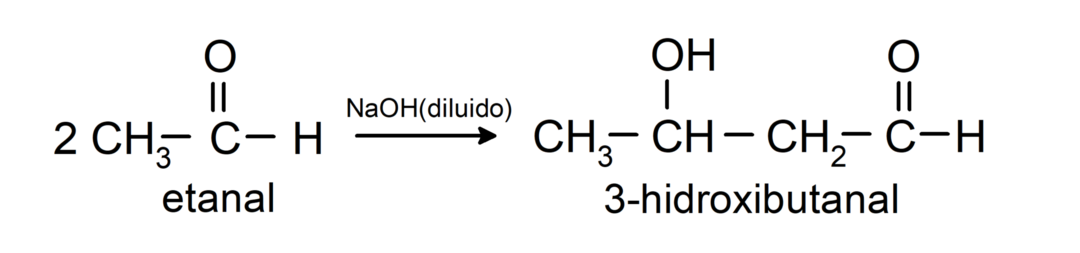
Eles são reduzidos a álcoois primários. Os aldeídos podem ser reduzidos a álcoois primários por hidrogenação catalítica ou por redução com borohidreto de sódio (NaBH).4) e hidreto de alumínio e lítio (LiAlH4).
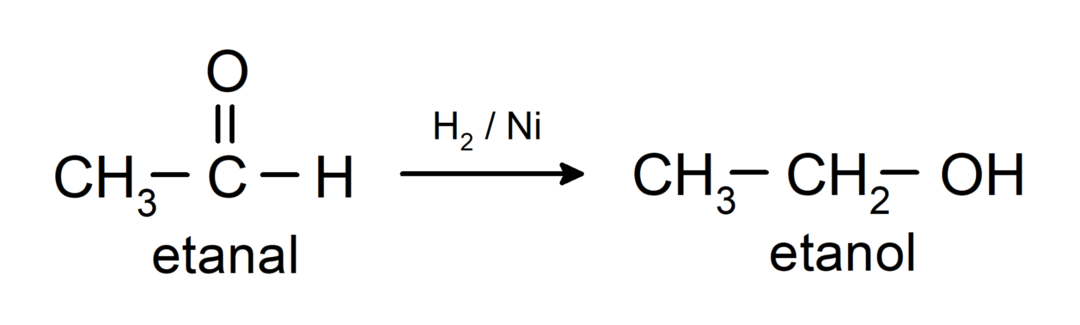
Propriedades químicas das cetonas
Entre as propriedades químicas das cetonas podemos encontrar:
Eles sofrem reações de adição nucleofílica. Por exemplo:
- Adição de ácido cianídrico para formar cianidrinas ou cianidrinas.
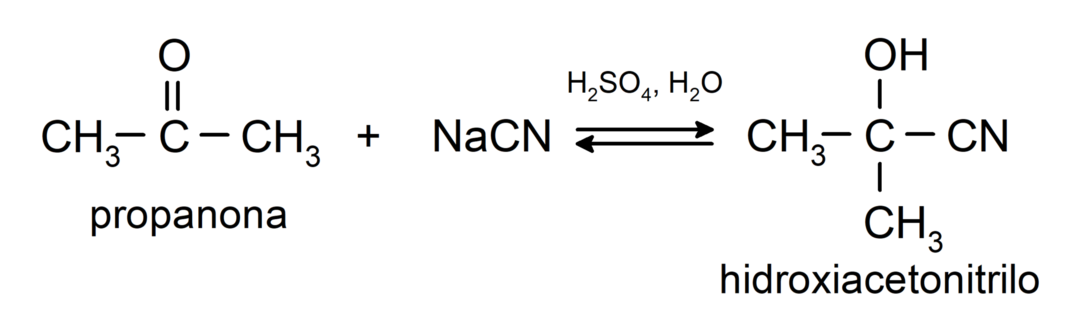
Eles adicionam álcoois (na presença de ácidos anidros) ao grupo carbonila das cetonas para formar cetais e hemicetais. Por exemplo:
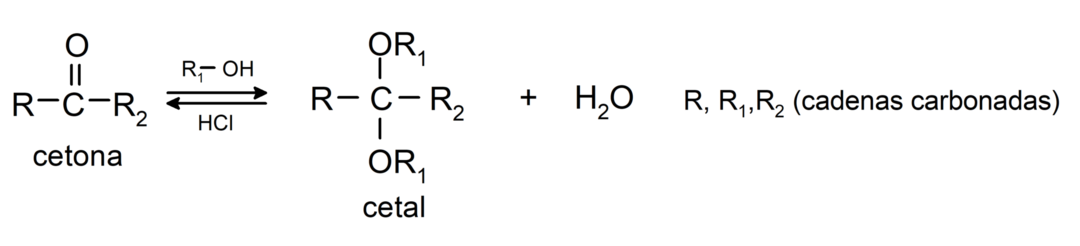
Eles sofrem reações de halogenação. Cetonas que possuem um hidrogênio alfa (α) reagem substituindo esse hidrogênio por halogênios (cloro (Cl), bromo (Br), iodo (I), flúor (F)) na presença de catalisadores ácidos ou básicos. A substituição ocorre quase exclusivamente em carbono α, isto é, o carbono que se ligou ao hidrogênio α. Por exemplo:
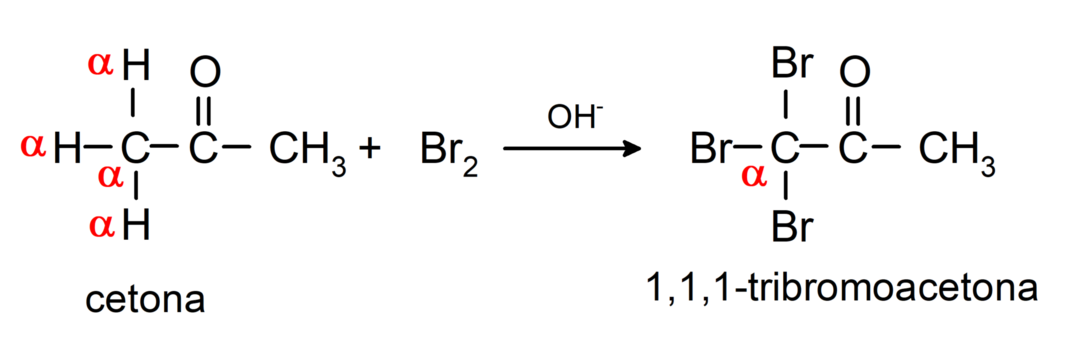
Eles são reduzidos a álcoois secundários por hidrogenação catalítica ou por redução com borohidreto de sódio (NaBH4) e hidreto de alumínio e lítio (LiAlH4). Por exemplo:
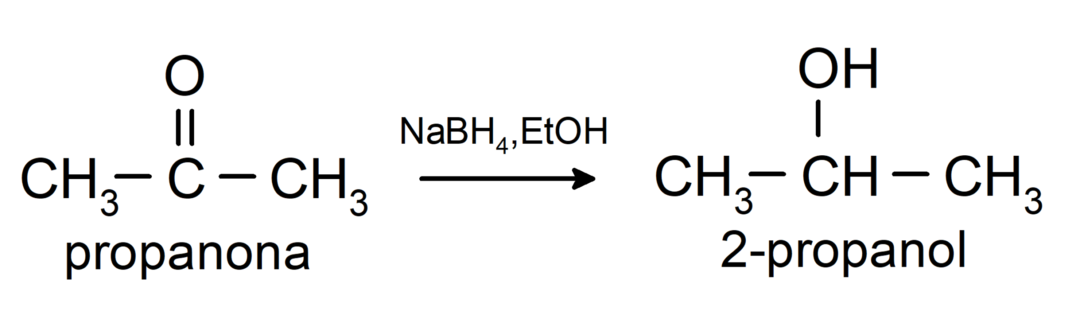
As cetonas não são oxidadas pelos reagentes de Tollens e Benedict.
Nomenclatura de aldeídos
De acordo com as regras estabelecidas pela União Internacional de Química Pura e Aplicada (IUPAC), Os aldeídos são nomeados usando prefixos que indicam o número de carbonos na cadeia. carbonatado. Não é necessário especificar a posição do grupo carbonila, pois ele está sempre na posição um, em uma das extremidades da molécula. Além disso, o sufixo -al é escrito no final do nome do aldeído. Por exemplo:
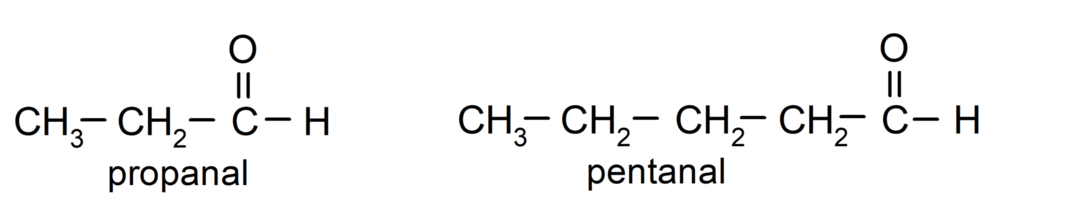
Se o aldeído for formado por diversas cadeias de carbono, ou seja, possui ramificações, a cadeia de carbono com maior número de átomos de carbono é escolhida como cadeia principal. As demais cadeias são denominadas grupos substituintes, e a posição de cada substituinte é escolhida de forma que ocupe o menor número possível na cadeia. Além disso, os átomos de carbono começam a ser contados a partir da extremidade que contém o grupo carbonila. Por exemplo:
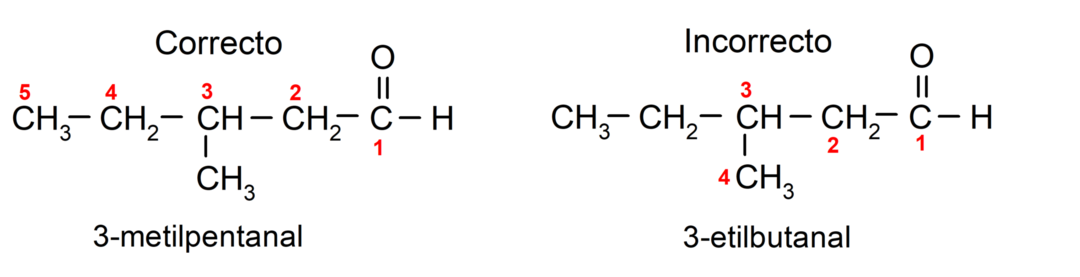
Aldeídos que possuem dois grupos carbonila são nomeados usando o sufixo -dial. Por exemplo:
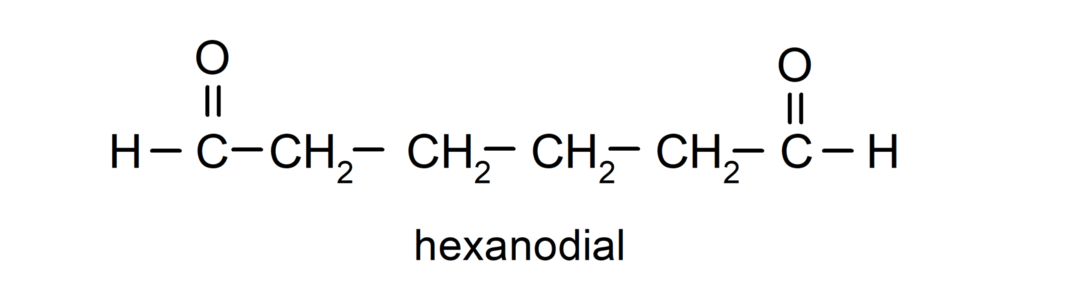
Nomenclatura de cetonas
De acordo com a União Internacional de Química Pura e Aplicada (IUPAC), as cetonas são nomeadas usando prefixos que indicam o número de carbonos na cadeia de carbono.
Por outro lado, o nome da acetona é escrito com o sufixo -one, precedido de um número que indica a posição do grupo carbonila na cadeia carbônica. A localização do grupo carbonila deve ser escolhida de forma que corresponda à numeração mais baixa possível. Por exemplo:
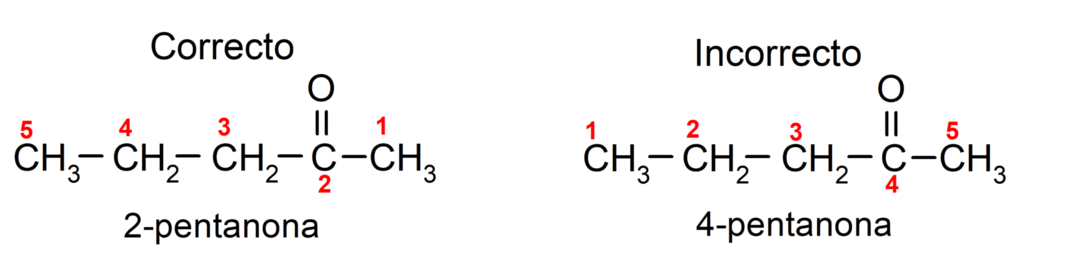
Para nomear uma cetona que é formada por diversas cadeias de carbono, ou seja, com ramificações, escolhemos como cadeia principal, a cadeia de carbono com maior número de átomos de carbono e que contém o grupo carbonila. O resto das cadeias são denominadas grupos substituintes. Por exemplo:
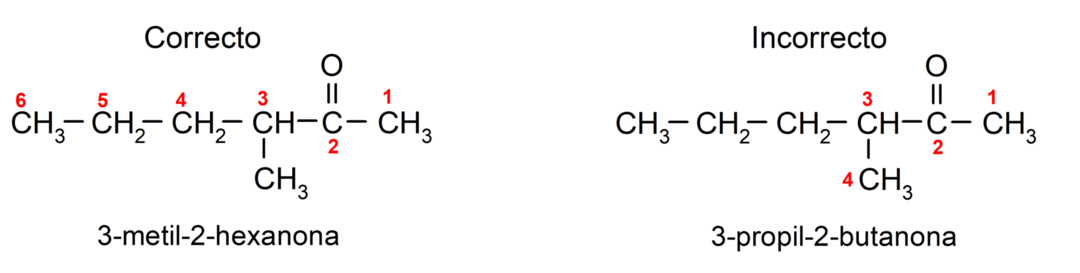
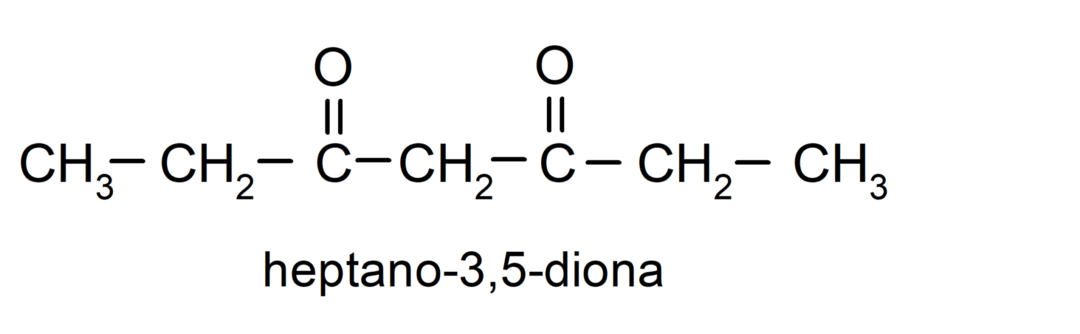
Existem cetonas que possuem dois grupos carbonila, são chamadas dionas. Por exemplo:
Exemplos de aldeídos
- metanal (formaldeído)
- etanal (acetaldeído)
- propanal (propaldeído)
- Butanal
- pentanal
- hexanal
- 3-bromociclopentanocarbaldeído
- ciclohexanocarbaldeído
- benzaldeído
- 4,4-dimetilpentanal
- 2-hidroxi-butanal
- 2-hidroxi-2-metil-butanal
- 2,3-dimetilpentanal
- pentanodial
- 4-hidroxi-3-metoxibenzaldeído
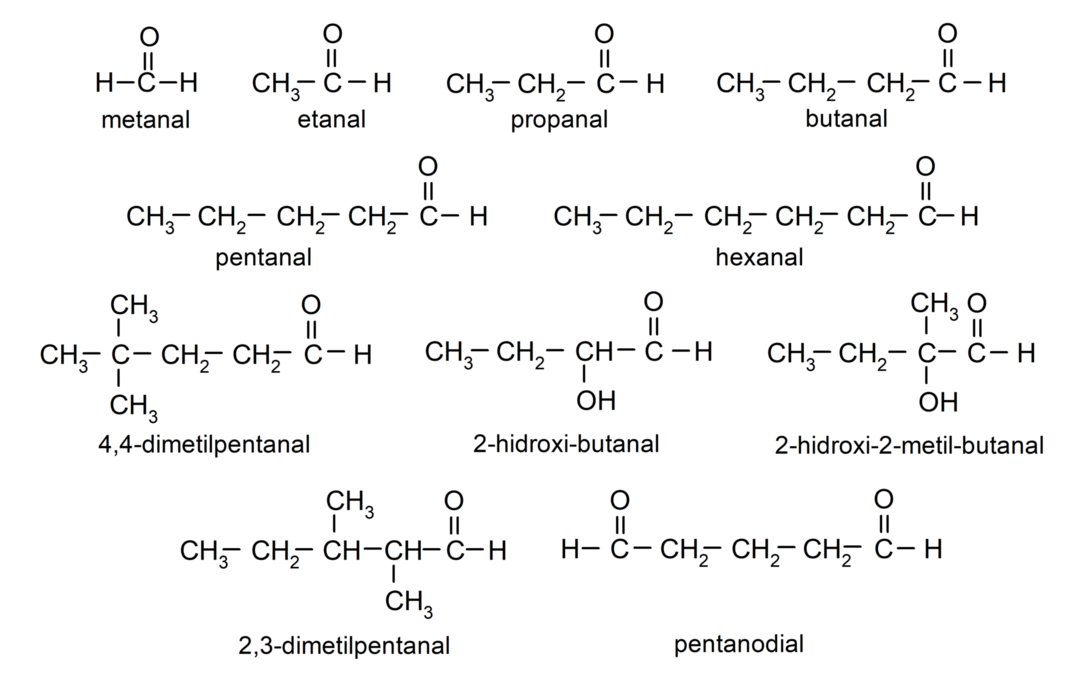
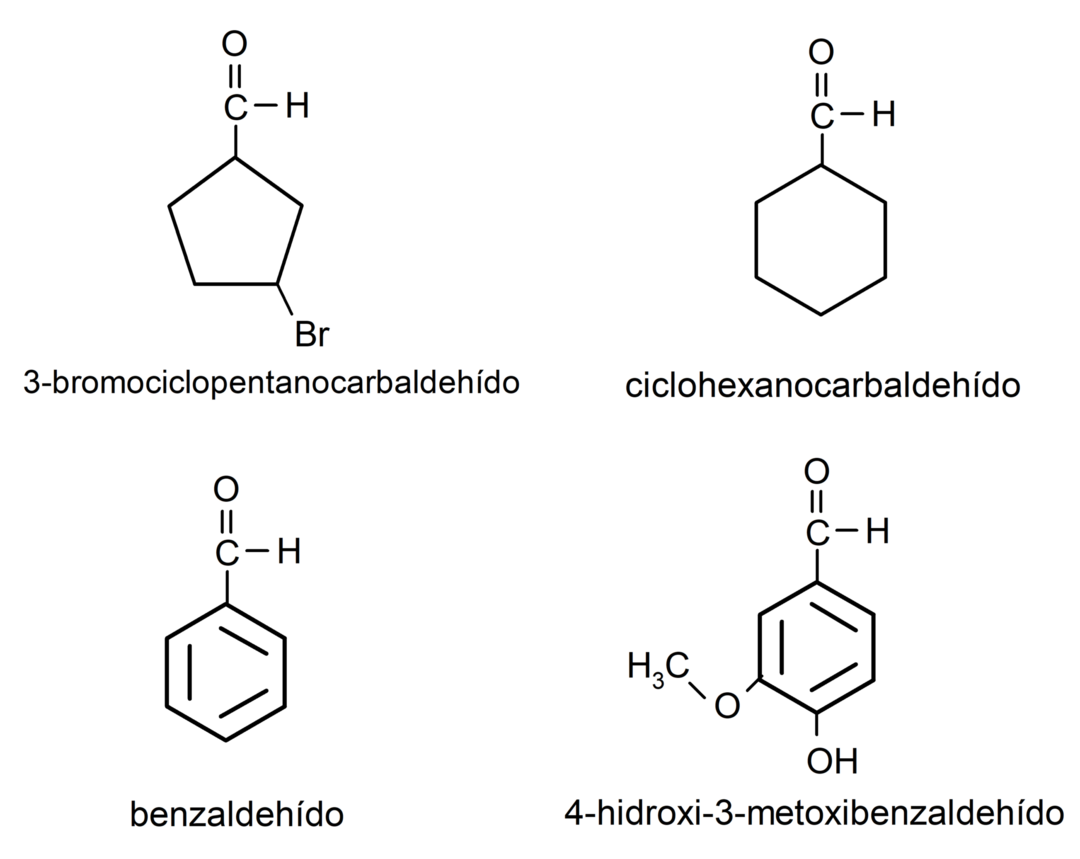
Exemplos de cetonas
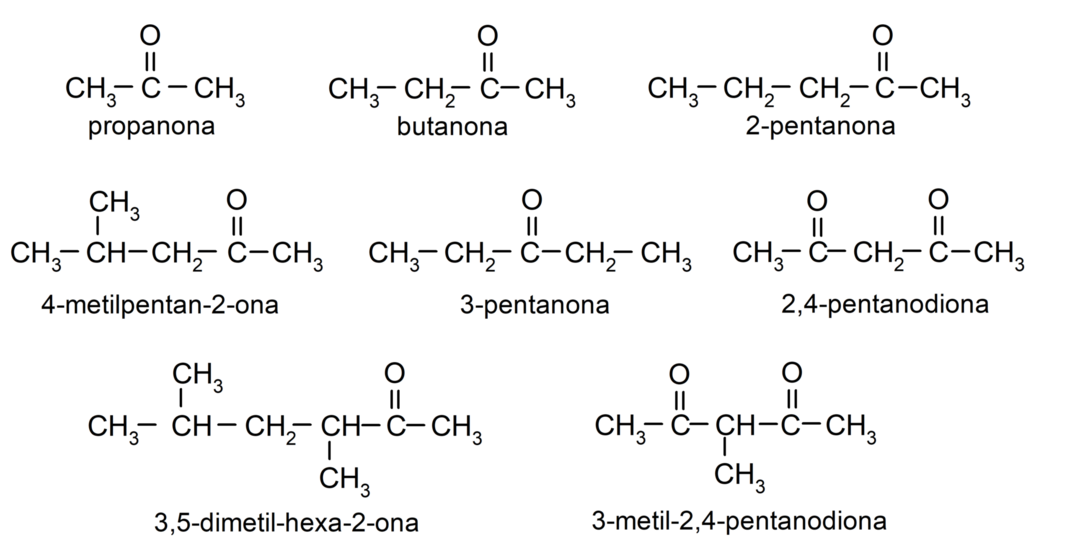
- propanona (acetona)
- butanona
- 2-pentanona
- 4-metilpentan-2-ona
- 3-metilciclohexanona
- ciclohexilmetilcetona
- 3,4 dimetil-hexan-2-ona
- etil fenil cetona
- 2,4-pentanodiona
- ciclohexanona
- 3-pentanona
- 3-metil-2,4-pentanodiona
- 1-fenilpropanona
- ciclopentanona
- difenil cetona
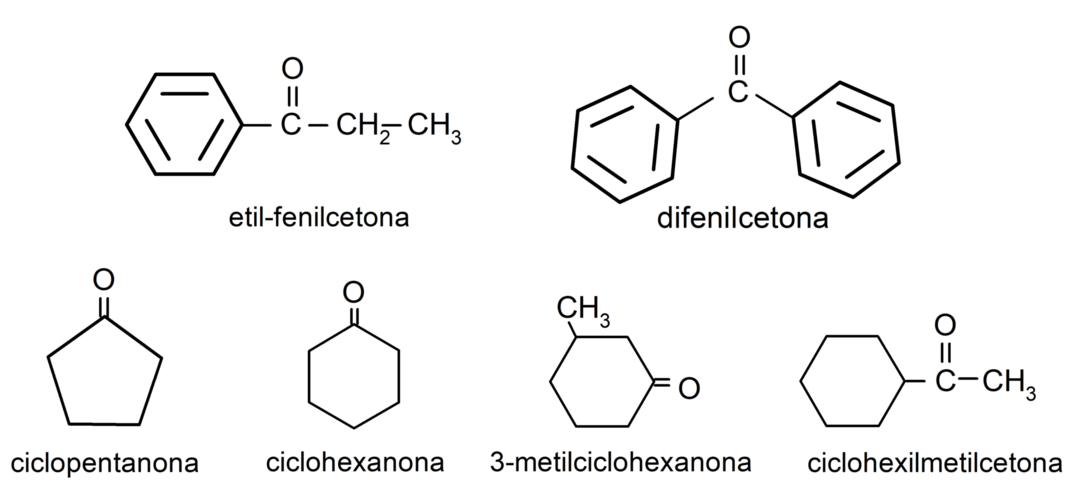
Usos de aldeídos na vida cotidiana
Alguns usos de aldeídos são:
- São utilizados na produção de solventes, tintas, perfumes, resinas e essências.
- São utilizados como conservantes em produtos cosméticos, amostras biológicas e cadáveres. O formaldeído é o mais utilizado para esses fins.
- São utilizados na produção de plásticos, que permitem a substituição de peças metálicas na indústria automotiva.
- Eles são usados como aromatizantes para alguns alimentos.
- Eles são usados como agentes desinfetantes.
- Eles têm sido usados para fabricar alguns explosivos, como o tetranitrato de pentaeritritol (TNPE).
Usos de cetonas na vida diária
Alguns usos das cetonas são:
- Eles são usados na produção de solventes. Especialmente a acetona é amplamente utilizada para remover tintas e lacas.
- São utilizados na fabricação de algumas borrachas e lubrificantes.
- Eles são usados para produzir tintas, lacas e vernizes.
- Eles são usados para produzir medicamentos e cosméticos.
Toxicidade de aldeído e cetona
- Os aldeídos. O contato com aldeídos causa irritação na pele, olhos e trato respiratório. Além disso, a exposição a aldeídos tem sido associada a doenças como câncer, dermatite de contato e doenças hepáticas e neurodegenerativas. O formaldeído, por exemplo, é considerado pela OMS (Organização Mundial da Saúde) um composto cancerígeno.
- cetonas. A exposição repetida a cetonas pode causar danos ao sistema nervoso central. Isso pode levar à perda de memória, fraqueza, dores musculares e cãibras. Além disso, se a pele entrar em contato com cetonas, ocorrerão ressecamento e rachaduras. Por outro lado, se as cetonas forem inaladas, ocorrem irritação do trato respiratório e tosse.
Referências
- Llorens Molina, JA. (2018). “Aldeídos e cetonas: alguns exemplos.” http://hdl.handle.net/
- Gabriel Pinto Cañón, Manuela Martín Sánchez, José María Hernández Hernández, María Teresa Martín Sánchez (2015) “O reagente de Tollens: da identificação de aldeídos à sua utilização em nanotecnologia. Aspectos históricos e aplicações didáticas.”Vol. 111 Não. 3. Real Sociedade Espanhola de Química.
- (2000) «Ácido Metacrílico e Derivados» na Enciclopédia de Química Industrial de Ullmann 2002, Wiley-VCH, Weinheim. DOI: 10.1002/14356007.a16_441.
- “Eles revelam um novo mecanismo de toxicidade em um grupo de compostos cancerígenos derivados da dieta e do meio ambiente” (2022) In: www.conicet.gov.ar Disponível em: https://www.conicet.gov.ar/ Acesso: 20 de junho de 2023.
Siga com:
- Álcoois
- Açúcares
- Alcanos
