20 exemplos de amidas
Exemplos / / November 06, 2023
As amidas são compostos químicos orgânicos derivados de ácidos carboxílicos, onde o grupo hidroxila (-OH) do grupo carboxila (-COOH) do ácido é substituído por um grupo amino (-NH2, -NH-R, -N-(R)2, sendo R qualquer cadeia de carbono).
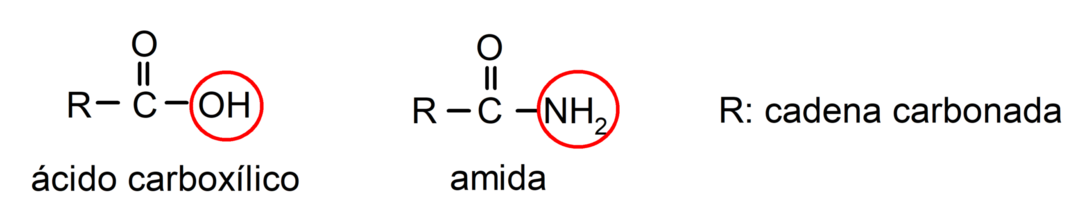
Amidas são moléculas orgânicas que contêm o grupo amida, que é composto por um grupo carbonila e um grupo amino. Por exemplo: etanamida, propanamida e N-metil-etanamida.

- Veja também: Aldeídos e cetonas
Tipos de amidas
As amidas podem ser classificadas de acordo com o número de hidrogênios (que estão ligados ao nitrogênio do grupo amino) que foram substituídos por diferentes grupos substituintes. Nesse sentido, existem amidas primárias, secundárias e terciárias.
- Amidas primárias. São amidas que não possuem os hidrogênios do grupo amino substituídos. Por exemplo:

- Amidas secundárias. São amidas que possuem um dos hidrogênios do grupo amino substituído. Por exemplo:

- Amidas terciárias. São amidas que possuem dois dos hidrogênios do grupo amino substituídos. Por exemplo:

Nomenclatura de amidas
De acordo com a nomenclatura comum, as amidas são denominadas como derivados de ácidos carboxílicos seguindo as seguintes regras:
- O carbono correspondente ao grupo carbonila está localizado na posição 1 e deste carbono é escolhida a cadeia de carbono mais longa. Por exemplo:

- As amidas primárias são nomeadas pelo prefixo correspondente ao número de átomos de carbono do ácido carboxílico que lhes deu origem. Por exemplo:

De acordo com a União Internacional de Química Pura e Aplicada (IUPAC), aminas Eles são nomeados usando as seguintes regras:
- As amidas secundárias e terciárias são nomeadas pelo prefixo correspondente ao número de átomos de carbono do ácido carboxílico que lhes deu origem. Além disso, para cada hidrogênio do grupo amino que foi substituído, é colocado um N. Assim, os diferentes substituintes são nomeados indicando sua quantidade e no final do nome é colocada a palavra amida. Por exemplo:

- Quando a molécula tem grupos prioritários em relação ao grupo amida, então a amida é denominada substituinte. Nestes casos, o grupo amida é denominado carbamoil. Por exemplo:
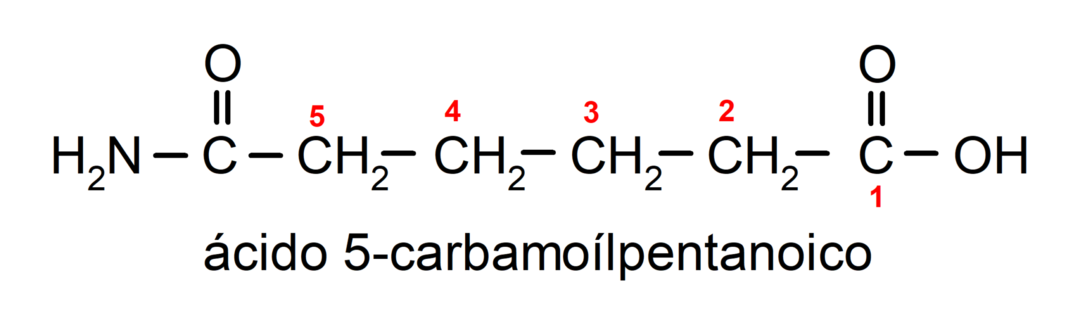
- Quando a molécula é formada por um ciclo e um grupo amida, o ciclo é tomado como cadeia principal e colocado o sufixo -carboxamida. Por exemplo:

Propriedades físicas das amidas
- As amidas são sólidas à temperatura ambiente, com exceção da metanamida.
- Eles têm pontos de ebulição elevados, ainda mais elevados do que os dos ácidos carboxílicos correspondentes.
- Amidas são bons solventes.
- São bases fracas.
Reações químicas de amidas
- As amidas reagem com um ácido aquoso para formar o ácido carboxílico correspondente e um sal de amônio. Por exemplo:

- As amidas reagem com o álcali para formar o ácido carboxílico correspondente e um sal carboxilato. Por exemplo:
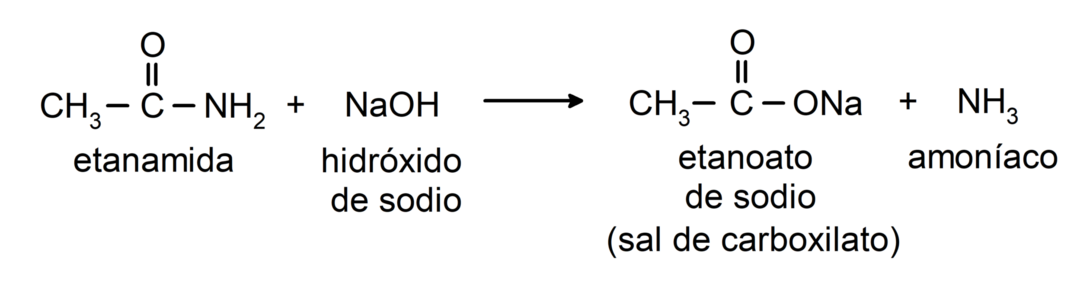
- Amidas são reduzidas a aminas na presença de tetrahidreto de alumínio e lítio:
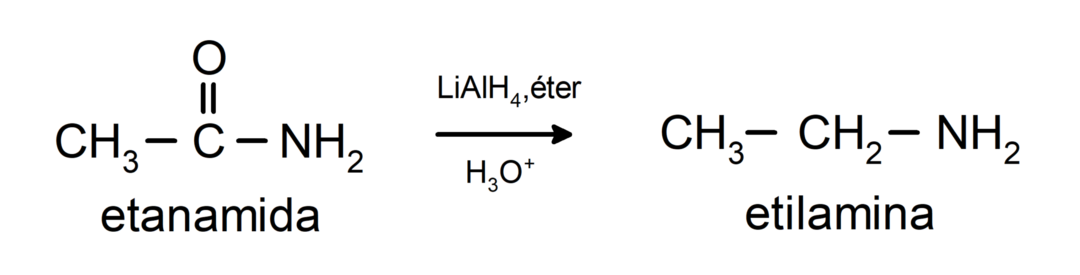
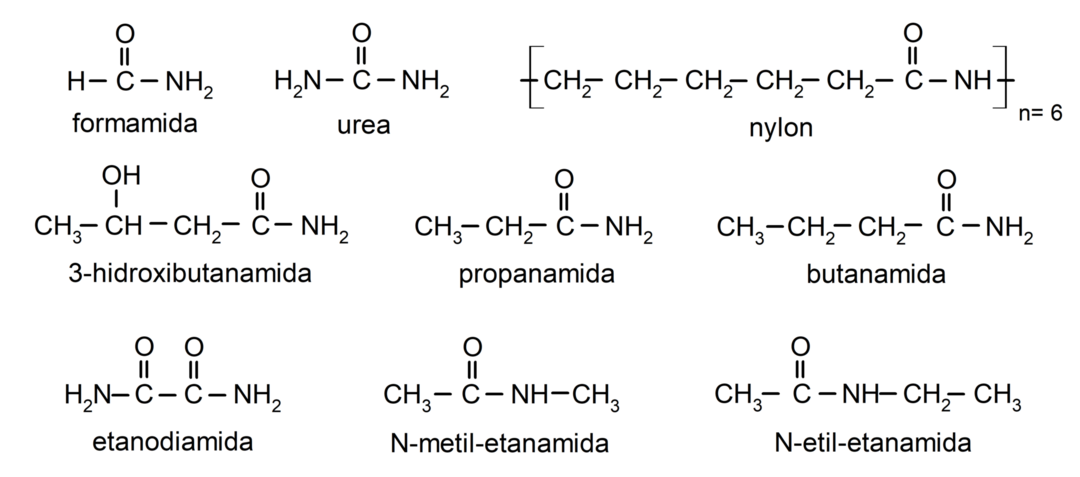
Exemplos de amidas
- formamida
- ureia
- nylon
- ε-caprolactama
- etanamida
- propanamida
- butanamida
- etanodiamida
- N-metil-etanamida
- N-etil-etanamida
- N-propil-etanamida
- N, N-dimetil-butanamida
- benzenocarboxamida
- 4-bromo-3-metil-ciclohexanocarboxamida
- 3-hidroxibutanamida

Usos de amidas
As amidas são amplamente utilizadas na indústria farmacêutica. Além disso, eles são usados como componentes desmoldantes na indústria de plásticos. Por outro lado, são utilizados como emulsificantes, surfactantes e solventes. Por exemplo, a ureia é uma amida amplamente utilizada na indústria farmacêutica e na indústria do náilon.
Referências
- Ramírez-Barrón, S. N., Sáenz-Galindo, A., López-López, L., & Cantú-Sifuentes, L. (2013). Amidas, Aplicação e Síntese. Revista Científica da Universidade Autônoma de Coahuila, 5(9).
- Caglieri, S. C. e Pagnan, M. (2013). Estudo teórico sobre hidrólise ácida de amidas alifáticas e aromáticas. Informação tecnológica, 24(3), 35-40.
- Martinez, C. H. M., Gomez, L. E. P., de Escobar, M. S., & Escalante, F. PARA. (2002). Quimica Organica. Universidade de Las Palmas de Gran Canaria, Vice-Reitoria de Estudos e Qualidade do Ensino.
Siga com:
- Aldeídos
- Álcoois
- Macronutrientes e micronutrientes
- Compostos orgânicos e inorgânicos


