30 exemplos de álcoois
Exemplos / / November 06, 2023
O álcoois são compostos químicos orgânicos que contêm em sua estrutura o grupo funcional hidroxila (- OH) ligado a um carbono (- C). O grupo (- C – OH) é denominado “carbinol”. Alguns exemplos de álcoois são: metanol, etanol e 1-propanol.
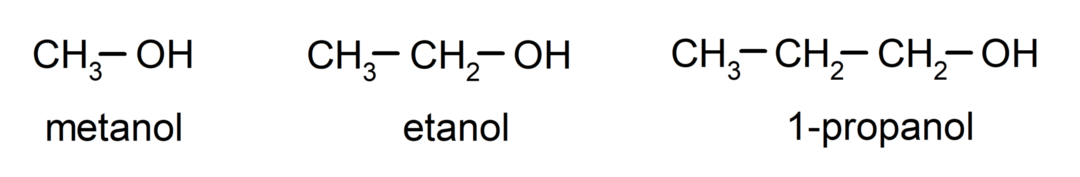
Os álcoois são compostos químicos com diversas utilizações no dia a dia, pois possuem propriedades antibacterianas e antissépticas. Por outro lado, podem ser perigosos para a saúde humana quando ingeridos de forma descontrolada.
Da mesma forma, nem todos os álcoois podem ser ingeridos por humanos.
- Veja também: Aminas e cetonas
Tipos de álcoois
Dependendo do número de átomos de carbono aos quais está ligado o átomo de carbono que tem o grupo hidroxila ligado, um álcool pode ser:
- Álcool primário. O átomo de carbono que possui o grupo hidroxila ligado também está ligado a um único átomo de carbono. Por exemplo:
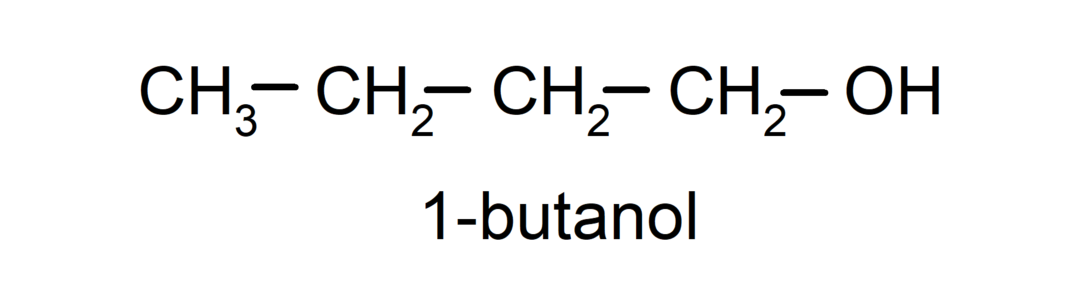
- Álcool secundário. O átomo de carbono que possui o grupo hidroxila ligado também está ligado a dois outros átomos de carbono. Por exemplo:
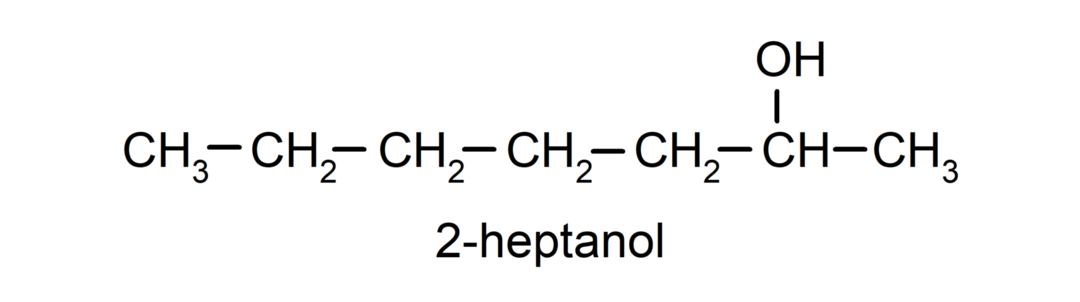
- Álcool terciário. O átomo de carbono que possui o grupo hidroxila ligado também está ligado a três átomos de carbono. Por exemplo:
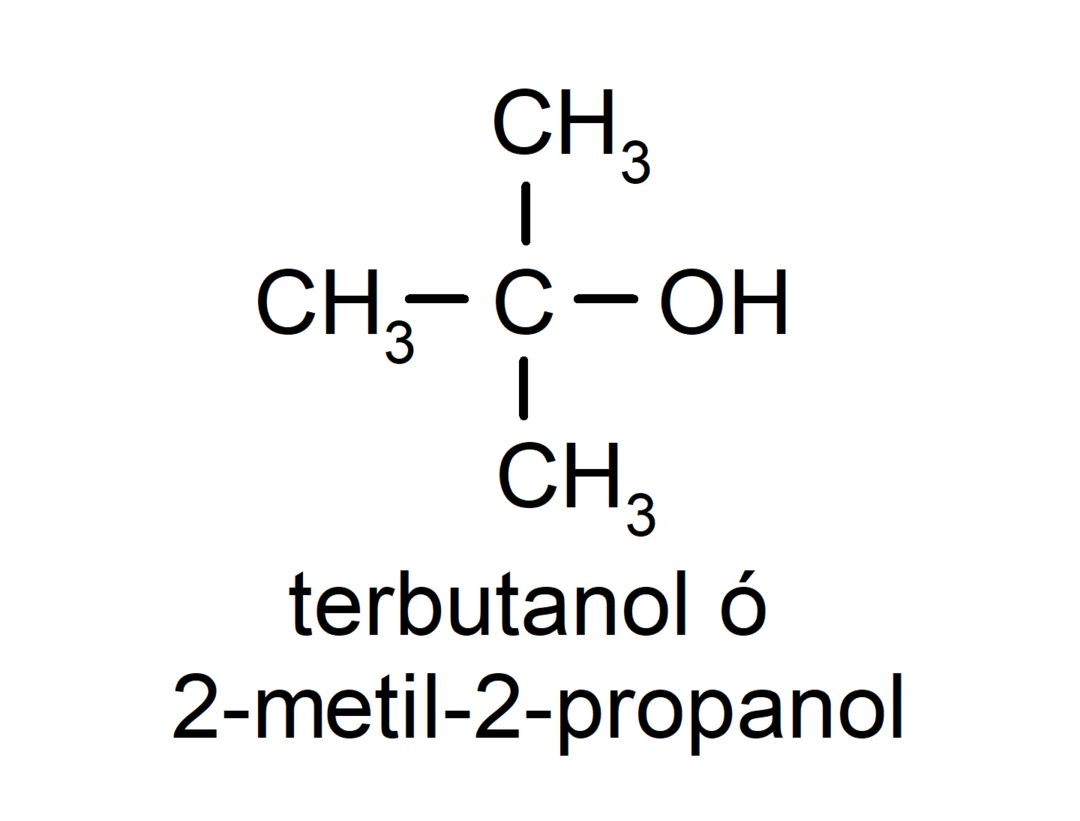
Dependendo do número de grupos hidroxila que possui, um álcool pode ser:
- Diol. Possui dois grupos hidroxila em sua estrutura. Por exemplo:
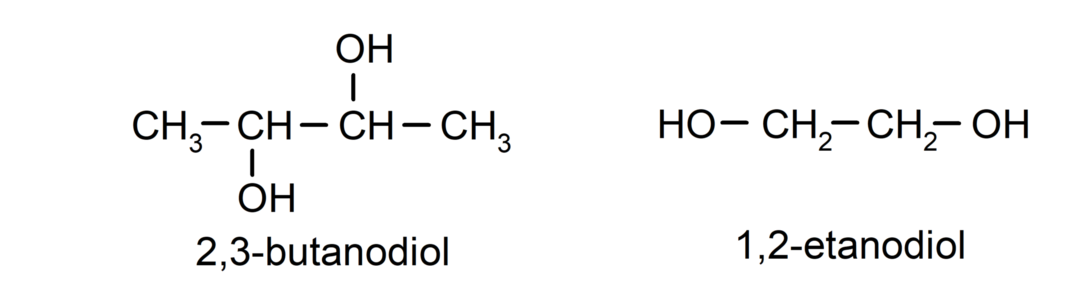
- Triol. Possui três grupos hidroxila em sua estrutura. Por exemplo:
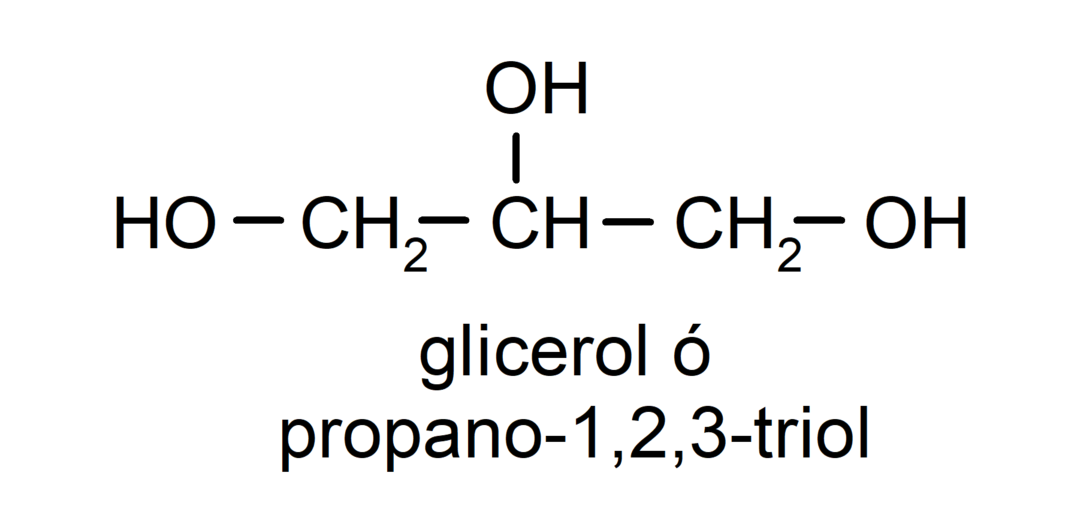
- Poliálcool. Possui muitos grupos hidroxila em sua estrutura. Por exemplo:
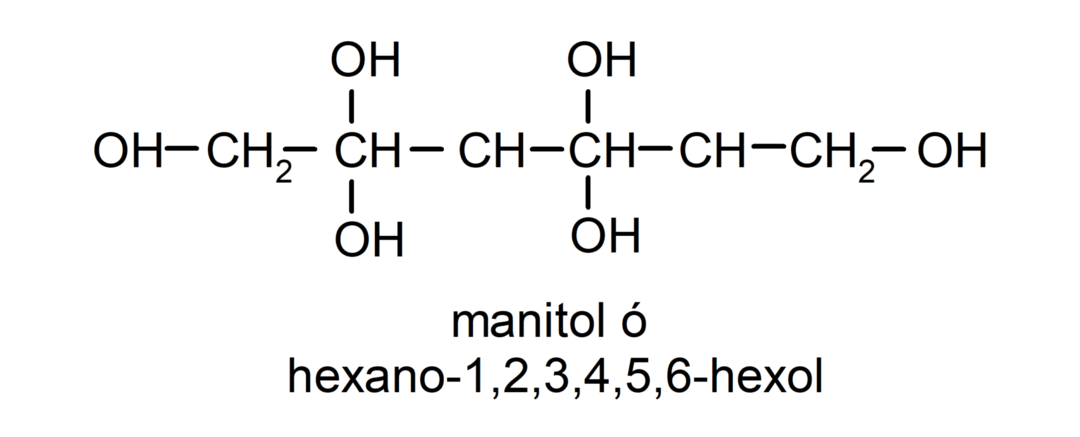
Propriedades físicas dos álcoois
Algumas das propriedades físicas dos álcoois são:
- Ponto de ebulição. O ponto de ebulição nos álcoois é bastante elevado devido à presença do grupo hidroxila, que permite a formação de ligações de hidrogênio. Além disso, quanto mais grupos funcionais hidroxila estiverem presentes na cadeia de carbono, maior será a ponto de ebulição de álcoois.
- Polaridade. Os álcoois são compostos bastante polares.
- Solubilidade. Álcoois de baixo peso molecular são solúveis em água. Por outro lado, quanto maior for a cadeia de carbono dos álcoois, menor será a sua solubilidade em água. Além disso, quanto mais grupos hidroxila os álcoois tiverem, maior será sua solubilidade em água.
- Estado de agregação. A maioria dos álcoois são líquidos à temperatura ambiente (25ºC) e apresentam odores característicos.
Propriedades químicas dos álcoois
Algumas das propriedades químicas dos álcoois são:
- Os álcoois se comportam como ácidos e bases.. Seu comportamento como ácidos pode ser observado em reações com metais ativos para liberar gás hidrogênio e formar alcóxidos.

Seu comportamento como bases pode ser observado em reações como a reação do metanol com brometo de hidrogênio para formar brometo de metiloxônio.
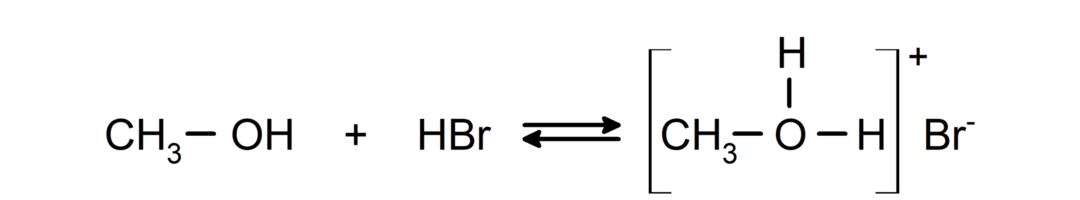
- Álcoois sofrem reações de halogenação. Eles reagem com haletos de hidrogênio para formar haletos de alquila.
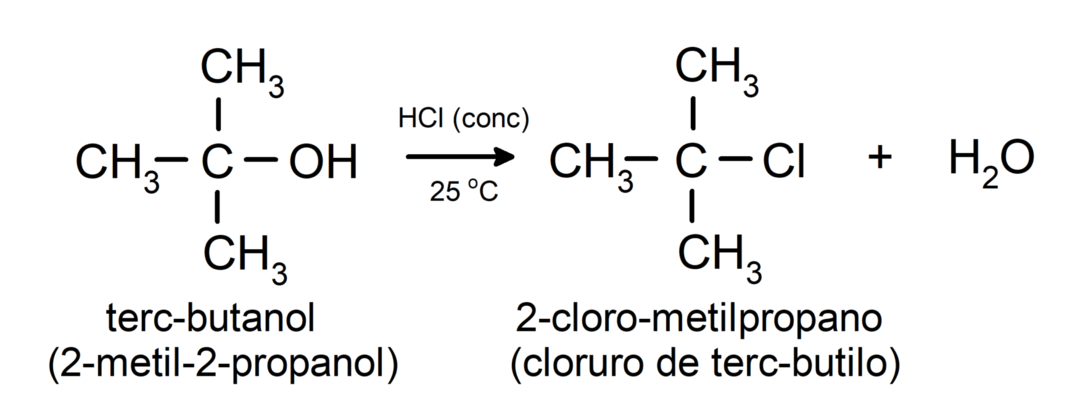
-
Álcoois sofrem reações de oxidação quando reagem com certos compostos oxidantes. Os produtos das reações de oxidação dependem do tipo de álcool que reage, ou seja, se é primário, secundário ou terciário.
Oxidação de álcool primário para formar aldeído ou ácido carboxílico.
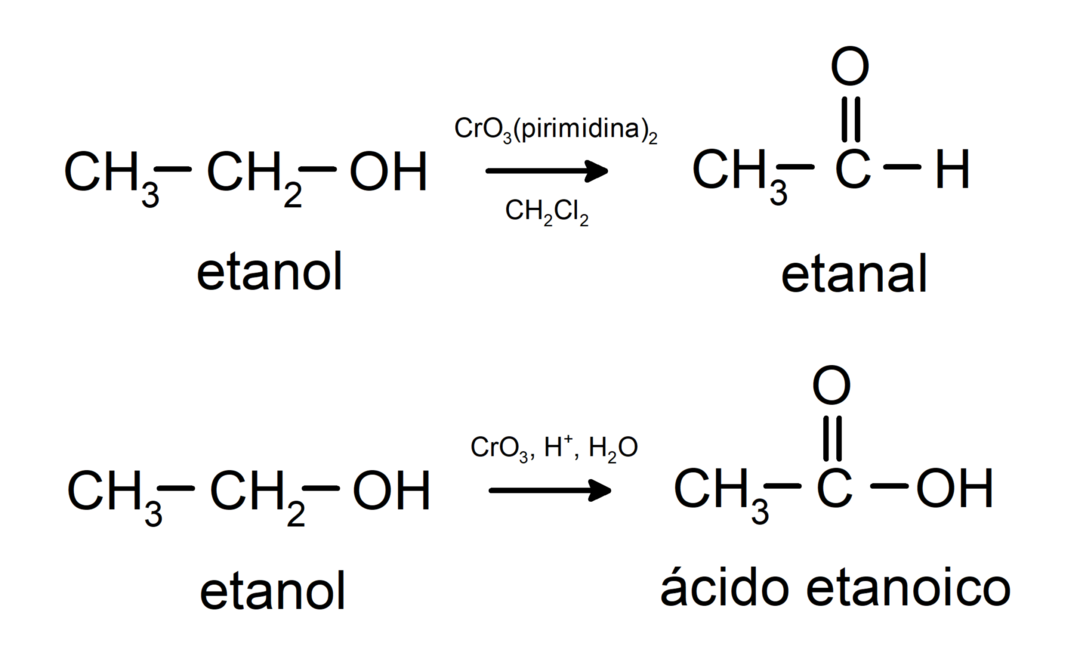
Oxidação do álcool secundário para formar cetona.
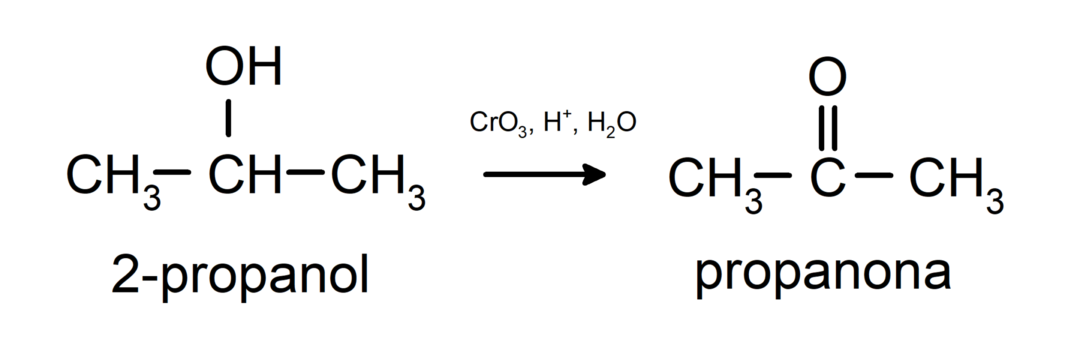
Os álcoois terciários não oxidam com oxidantes comuns. Com agentes oxidantes muito fortes podem ser transformados em alcenos, que podem então ser oxidados.
Álcoois que possuem dois grupos hidroxila localizados em carbonos adjacentes são oxidados com tetraacetato de chumbo para formar duas cetonas.
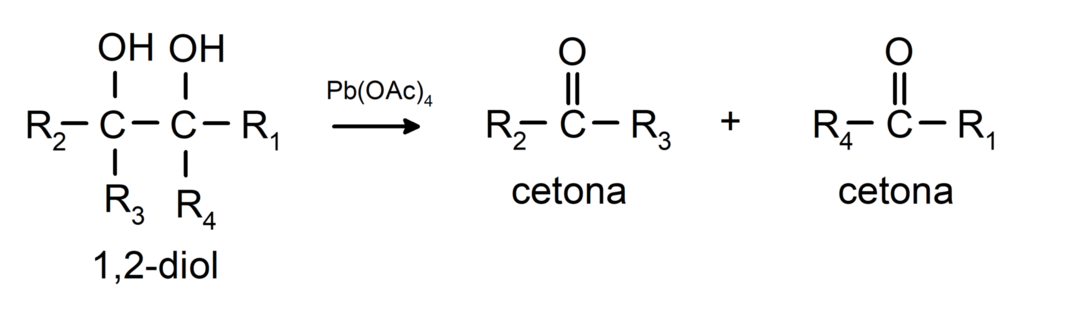
- Álcoois sofrem reações de desidrogenação. Estas reações ocorrem apenas com álcoois primários e secundários, que quando submetidos a altas temperaturas na presença de catalisadores liberam hidrogênios.
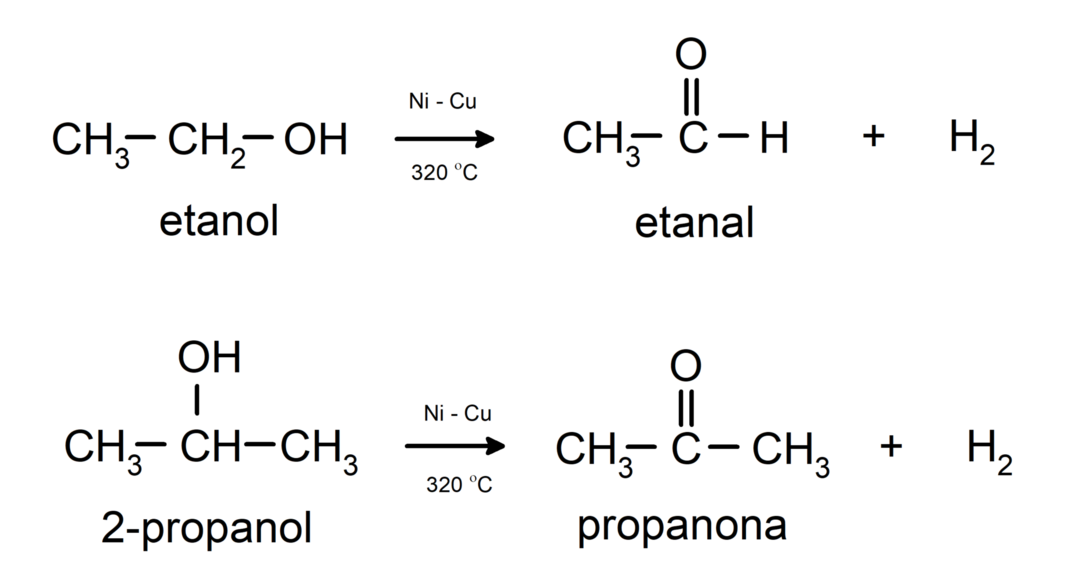
- Álcoois sofrem reações de desidratação. Os álcoois desidratam para formar os alcenos correspondentes. Esta reação ocorre na presença de temperaturas ácidas e intermediárias.
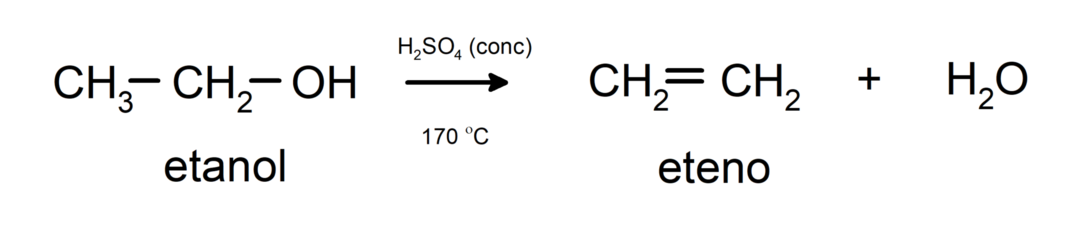
Nomenclatura do álcool
De acordo com a nomenclatura estabelecida pela IUPAC (União Internacional de Química Pura e Aplicada), os álcoois são nomeados seguindo as seguintes regras:
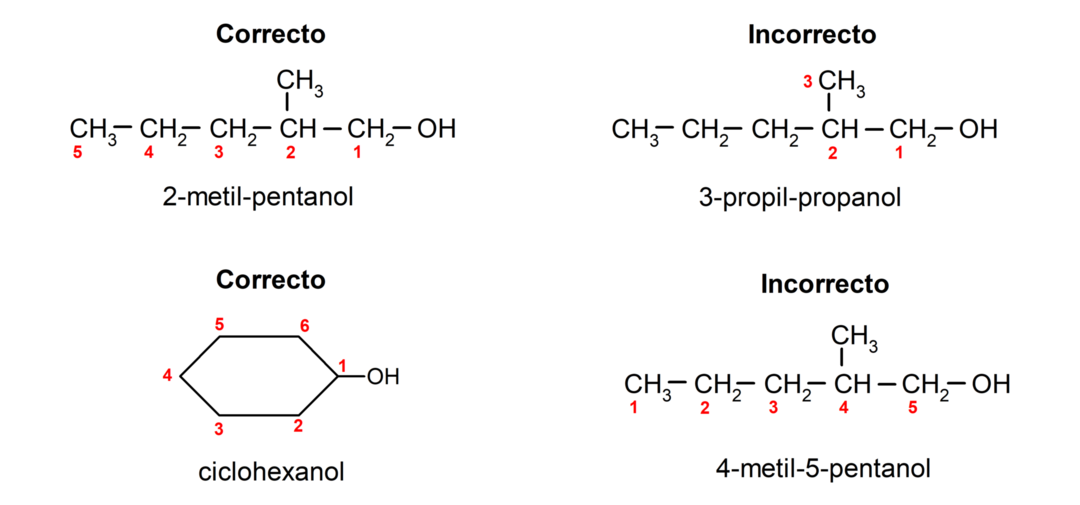
- A posição do grupo hidroxila é escolhida levando-se em consideração que ocupa o menor número possível na cadeia de carbono. Se a estrutura do álcool for cíclica, a posição 1 no carbono que possui o grupo hidroxila ligado é considerada e o prefixo ciclo- é usado para nomeá-lo.
- O nome do álcool é escrito com prefixos que indicam o número de átomos da cadeia de carbono e, além disso, é colocado o sufixo -ol.
- Se a estrutura do álcool tiver ramificações, a cadeia mais longa que também contém o grupo hidroxila é escolhida como cadeia carbônica principal.
De acordo com a nomenclatura tradicional, os álcoois são nomeados escrevendo a palavra “álcool” e depois escrevendo o nome do álcool. alcano correspondente à cadeia de carbono, mas em vez de usar a terminação -ano do alcano, a terminação -ilílico.
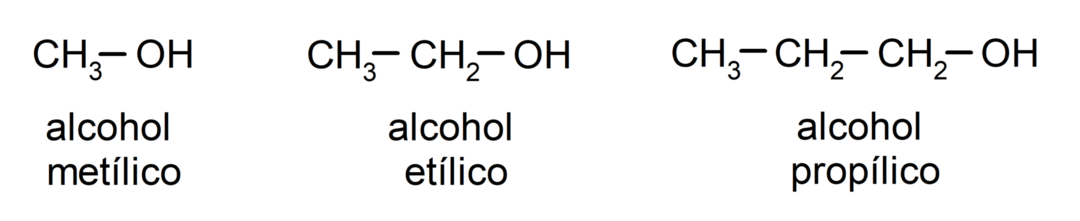
Exemplos de álcoois
- metanol
- etanol
- 1-propanol
- 2-propanol
- 1-butanol
- 3-etilhexan-2-ol
- glicerol
- fenol
- 2-metil-2-butanol
- 1,2-etanodiol
- 1,5-heptadieno-3-ol
- 3-metil-2-butanol
- benzilmetanol
- 3-pentanol
- 2-metilfenol
- 1,2-dihidroxifenol
- cicloheaxnol
- 1-feniletanol


Usos de álcoois
Os usos mais comuns de álcoois são:
- São utilizados como desinfetantes e anti-sépticos, pois impedem o crescimento de alguns microorganismos ou destruí-los. O etanol e o álcool isopropílico são os mais utilizados para esse fim.
- Eles são usados na síntese de diferentes compostos químicos. O metanol, por exemplo, é usado para obter metanal (formaldeído).
- Eles são usados para produzir anticongelante. O metanol é um dos mais utilizados para esse fim.
- Eles são usados como solventes na indústria farmacêutica. O etanol é um dos mais utilizados nesse sentido.
- Eles são usados como solventes para lacas, corantes e tintas. O metanol é amplamente utilizado para esse fim.
- São utilizados como combustível e há uma tendência importante de substituição parcial do uso de combustíveis fósseis pelo uso de bioetanol combustível.
- Eles são usados para fazer resinas. O fenol é usado nesse sentido.
Perigos do consumo de álcool
Embora o consumo de álcool seja hoje aceito socialmente, o abuso dessa substância gera dependência e dependência.
O etanol é o álcool presente nas bebidas alcoólicas, que quando consumido em excesso afeta habilidades cognitivas e pode causar doenças cardiovasculares, cirrose hepática e Câncer.
Além disso, quando é atingido o grau de intoxicação alcoólica, ou seja, um estado de embriaguez, se a dose do o álcool estiver muito alto, pode ocorrer coma alcoólico, que pode levar à paralisia respiratória e até à morte. morte.
Referências
- T. PARA. Geissman. (1974) “Princípios de Química Orgânica” Segunda Edição. Editorial Reverté, S.A. ISBN: 8429171800
- Ahumada-Cortez, J. G., Gámez-Medina, M. E., & Valdez-Montero, C. (2017). Consumo de álcool como problema de saúde pública. Ra Ximhai, 13(2), 13-24.
- Morrison, R. T. e Boyd, R. N. (1998). Quimica Organica. Educação Pearson.
- Weininger, S. J. e Stermitz, F. R. (1988). Quimica Organica. Eu inverti.
Siga com:
- Álcool etilico
- Combustíveis
- Quimica Organica

