Exemplo de ligação peptídica
Química / / July 04, 2021
O Peptide Bond é aquele em que duas moléculas de aminoácidos são unidas por condensação.
Para entender melhor as ligações peptídicas, os aminoácidos devem primeiro ser definidos:
O Aminoácidos são moléculas orgânicas curta contendo pelo menos um grupo amino (-NH2), de natureza alcalina, e um grupo carboxil (-COOH), de caráter ácido.
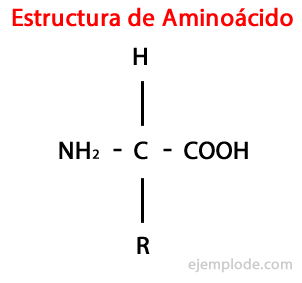
Embora os seres vivos sintetizem, para diferentes fins, tipos muito diversos de aminoácidos, os mais importantes são aqueles que fazem parte das proteínas, todos os quais pertencem à classe do α-aminoácidos.
Os α-aminoácidos são caracterizados por terem os grupos ácido e amino ligados ao mesmo átomo de carbono, denominado carbono α. Além disso, este carbono α liga, como um terceiro substituinte, um átomo de hidrogênio e, como um quarto substituinte, um grupo adicional de diversos tamanhos e características, que diferencia cada aminoácido de Os demais.
O quarto substituinte é chamado Cadeia lateral do Aminoácido e é frequentemente representado de forma simplificada pela letra R.
Como os quatro substituintes do carbono α são diferentes e adotam um arranjo tetraédrico em torno dele, os α-aminoácidos presentes isomeria óptica, que é quando uma molécula tem um forma alternativa que se parece com um imagem no espelho his, que no final não é uma molécula igual. Essas duas formas isoméricas da molécula são designadas pelas letras D ou L, dependendo de como os substituintes estão dispostos no espaço. Todos os aminoácidos que estão nas proteínas são L.
Os aminoácidos são classificados de acordo com seu caráter químico em Polar e apolar. Os Polars, por sua vez, são divididos em Neutro e Carregado (que pode ser ácido ou básico). O Não polar pode ser alifático ou aromático.
Peptídeos e a ligação peptídica
Os peptídeos são o produto da união covalente de aminoácidos através de ligações amida, formando-se por condensação da extremidade carboxila de uma e da extremidade amino da outra, liberando uma molécula de água no reação. Essa união é chamada de Peptide Bond.
O mecanismo desta reação é apresentado a seguir, em que o Grupos Amino e Carboxil, e a condensação das moléculas de aminoácidos ocorre para formar o peptídeo.
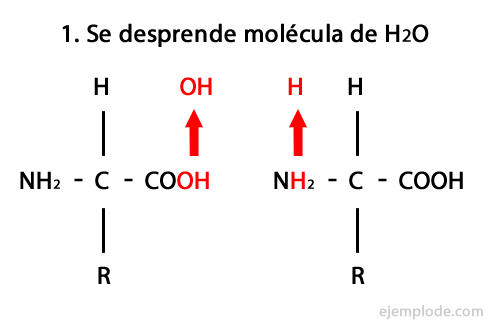
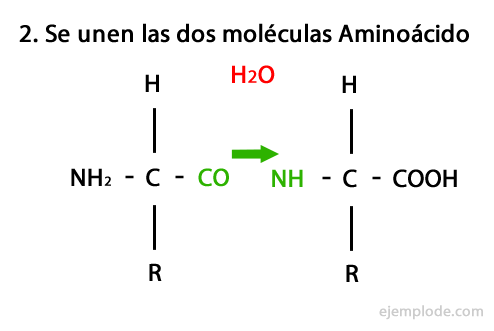

Peptídeos, como aminoácidos e proteínas, têm um grupo amino e um grupo carboxila em suas extremidades sem reagir.
Para especificar a fórmula de um simples peptídeo, e mesmo de uma proteína, basta listar os aminoácidos que o compõem, começando com aquele com um grupo Amino grátis, e terminando com aquele com seu grupo Carboxyl livre.
Alguns peptídeos encontrados no corpo são os Vasopressina, que aumenta a pressão arterial e aumenta a reabsorção de água nos rins; a Encefalina, que reduz a sensação de dor; e a Oxitocina, o que faz com que o útero se contraia.
Características de ligação peptídica
A condensação do grupo Amino de um aminoácido com o Carboxil de outro, ocorre em solvente aquoso, pelo que não é espontâneoe, portanto, a síntese de proteínas requer um suprimento de energia.
A ligação peptídica, como em qualquer ligação amida, apresenta ressonância entre duas formas extremas: a forma neutra, com uma ligação simples unindo o carbono carbonil do primeiro aminoácido e o nitrogênio do amino do segundo (C-N), e a forma com separação de cargas em que os dois átomos estão ligados por uma ligação dupla (C = N). Na realidade, a ligação peptídica não adota nenhuma das duas situações extremas, mas é um híbrido ressonante de ambas.
Aí está a chamada Plano Peptídico, que consiste em todos os átomos envolvidos na ligação peptídica, que unem os dois aminoácidos iniciais. De um lado, os átomos de Nitrogênio e Hidrogênio, com seus respectivos Carbonos α no primeiro aminoácido. Por outro lado, o Carbono α do outro aminoácido, com o Oxigênio e o Carbono do grupo Carbonila.
Diferenças entre peptídeos e proteínas
O peptídeos têm um baixo número de aminoácidos, que varia de duas a algumas dezenas deles, e sua conformação em solução torna-se flexível.
As pequenas proteínas, estruturalmente perto de grandes peptídeos, têm um conformação definida e muito menos flexível.
Existem proteínas que, como os peptídeos, têm uma conformação desordenada e flexível, mas essa ordem quando interagem com outras macromoléculas na célula.
20 exemplos de aminoácidos que participam da ligação peptídica
- Glicínia
- A menina
- Valine
- Leucina
- Isoleucina
- Proline
- Metionina
- Fenilalanina
- Tirosina
- Triptofano
- Serine
- Treonina
- Cisteína
- Asparagina
- Glutamina
- Ácido aspártico
- Ácido glutâmico
- Lisina
- Arginina
- Histidina