Exemplo de nomenclatura de compostos orgânicos
Química / / July 04, 2021
Os compostos orgânicos são moléculas cuja característica é serem formados por uma base de moléculas de carbono e hidrogênio, também conhecido como esqueleto, e combinado com outros elementos, principalmente oxigênio, nitrogênio e enxofre.
O IUPAC (União Internacional de Química Pura e Aplicada, União Internacional de Química Pura e Aplicada) estabeleceu regras gerais para a classificação e nomenclatura de moléculas orgânicas, das quais explicamos as mais importantes.
Hidrocarbonetos
Os hidrocarbonetos são as moléculas orgânicas mais simples, constituídas por um esqueleto de carbono e átomos de hidrogênio. Existem três tipos de hidrocarbonetos:
Alcanos
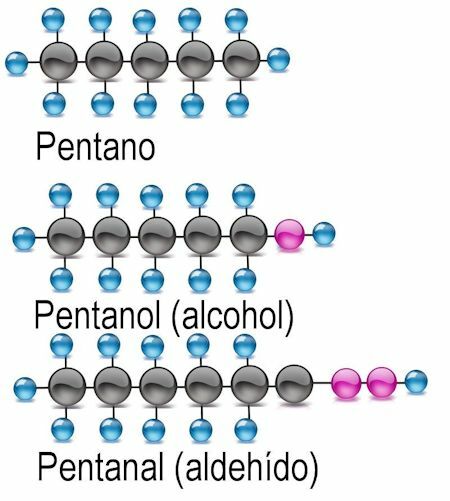
Eles são os mais simples, formados por átomos de carbono unidos por ligações covalentes simples aos átomos de hidrogênio, com a formulação geral H = 2n + 2, ou seja, os átomos de hidrogênio têm o dobro do número de átomos de hidrogênio. carbono, mais 2. Sua nomenclatura é formada pelos prefixos numéricos met- para 1 átomo de carbono, et- para 2, prop- para 3 e but- para 4; a partir de 5 átomos de carbono, os prefixos comuns pent-, hex-, hept-, oct-, etc. são usados. A todos os alcanos adiciona-se a terminação -ano.
Exemplo: CH4: metano; C2H6: etano; C4H10: butano; C6H14: hexano
Alcenos
Eles são formados por um esqueleto de carbono no qual existe uma ligação dupla entre os átomos de carbono. Sua fórmula geral é H = 2n, ou seja, seus átomos de hidrogênio têm o dobro do número de átomos de carbono. Como os alcanos, eles usam prefixos que indicam seu número de átomos de carbono e, neste caso, a desinência -eno é adicionada. Além disso, em moléculas com mais de três átomos de carbono, o carbono onde a ligação dupla é encontrada, começando a contar a partir do carbono mais próximo de Está.
Exemplos: C2H4: eteno; C3H6: propeno; C4H8: buteno, 2-buteno; C6H12: Hexeno, 2-hexeno (ligação dupla no átomo 2), 3-hexeno (ligação dupla no átomo 3).
Alkynes
Os alcinos contêm uma ligação tripla em seus átomos de carbono. Sua fórmula geral é H = 2n-2, indicando que a molécula conterá dois átomos de hidrogênio com menos de duas vezes o número de átomos de carbono. Ao prefixo que indica o número de carbonos, a desinência -ino é adicionada. Como no caso dos alquenos, menciona-se o carbono que contém a ligação tripla, contado do extremo mais próximo a ele.
Exemplos: C2H2: etino; C3H4: gorjeta; C4H6: butino, 2-butino; C6H12: Hexino, 2-hexeno (ligação tripla no átomo 2), 3-hexino (ligação tripla no átomo 3).
Grupos funcionais
Os grupos funcionais são combinações de átomos que funcionam como um íon e substituem um átomo de hidrogênio na fórmula de um alcano.
Radicais
O alcano sem o átomo de hidrogênio é denominado Radical, e para identificá-lo adiciona-se a desinência -ilo:
Exemplos CH4: metano - CH3+ metilo; C2H6: etano - C2H5+ etilo; C4H10: butano - C4H9+ butilo; C6H14: hexano - C6H13+ hexil.
Combinação de hidrocarbonetos
Um dos casos que podem ocorrer é que dois ou mais hidrocarbonetos se combinam em uma molécula. Os hidrocarbonetos com os quais está combinado são chamados de arborescências. Nestes casos, o hidrocarboneto básico será aquele com a cadeia mais longa, e o número de carbono onde as arborescências são encontradas, seguidas do nome do radical com a desinência -il e, em seguida, o nome do hidrocarboneto base. O número será mencionado tantas vezes quantas as árvores anexadas a ele. Caso as arborescências sejam do mesmo radical em diferentes átomos de carbono, serão mencionados os números separados por vírgulas, seguidos de hífen, o nome do radical, então os números dos átomos onde o outro radical está ligado, se houver, um travessão, o nome do radical e o nome do hidrocarboneto base. Caso existam dois radicais ligados ao mesmo átomo de carbono, o número será mencionado duas vezes. Se forem radicais diferentes, será mencionado uma vez antes do nome de cada radical; se os radicais forem iguais, o número será mencionado duas vezes. Começaremos mencionando primeiro as arborescências mais simples (aquelas com menor quantidade de carbonos) e depois aquelas com maior quantidade.
Exemplo: Uma molécula de pentano, com dois radicais de etano, ligados no carbono 2 e 3:
2,3-etil pentano. Uma molécula de octano, um radical de propano no carbono 6, radicais de metano nos carbonos 4 e 5 e radicais de etano, ligados nos carbonos 2, 3 e 4: 4,5-metil-2,3,4-etil-6- propil -octano.
Grupo funcional de álcool
O mais simples dos grupos funcionais é o álcool, no qual um átomo de hidrogênio é substituído por um grupo hidroxila (OH). Nestes compostos, a terminação -anol é adicionada ao nome do radical. Quando apropriado, o átomo de carbono onde o grupo funcional é encontrado deve ser mencionado:
Exemplos CH3OH: metanol: C2H5OH etanol; C4H9OH butanol ou 2-butanol; C6H13OH hexanol, 2-hexanol (grupo funcional no átomo 2), 3-hexanol (grupo funcional no átomo 3).
Grupo funcional aldeído
Nos aldeídos, o átomo de hidrogênio é trocado pelo grupo funcional -CHO. Para identificá-los, a terminação -anal é adicionada, e o átomo de carbono onde o grupo funcional é encontrado também é mencionado:
Exemplos CH3COH: metanal: C2H5Ethanal COH; C4H9COH butanal ou 2-butanal; C6H13COH hexanal, 2-hexanal (grupo funcional no átomo 2), 3-hexanal (grupo funcional no átomo 3).
Grupo funcional ácido
Em ácidos orgânicos, o átomo de hidrogênio é trocado pelo grupo funcional -COOH. Para identificá-los, a palavra ácido é mencionada e a terminação -anóico é adicionada, e o átomo de carbono onde o grupo funcional é encontrado também é mencionado:
Exemplos CH3COOH: ácido metanóico: C2H5Ácido COOH etanóico; C4H9Ácido butanóico COOH ou ácido 2-butanóico; C6H13COH ácido hexanóico, ácido 2-hexanóico (grupo funcional no átomo 2), ácido 3-hexanóico (grupo funcional no átomo 3).



