20 Exemple de gaz ideal și gaz real
Miscellanea / / July 04, 2021
chimie este ştiinţă care studiază compoziția și transformările care pot apărea în materie, în oricare dintre formele sale. Unul dintre cele mai importante domenii de studiu în chimie este cel al gaze.
conceptul de gaz A fost înființată de chimistul belgian Jan van Helmont. Pentru a explica comportamentul gazelor, au fost dezvoltate diferite ecuații matematice folosind instrumente statistice. Cu toate acestea, a fost necesară simplificarea și modificarea acestor ecuații, deoarece acestea nu au funcționat pentru toate tipurile de gaze, astfel încât au fost definite diferite modele de gaze (gaz ideal Da gaz real, printre alte abordări intermediare). De exemplu: azot, heliu, metan.
În acest sens, au fost stabilite trei legi care să raporteze într-un mod general volumul, temperatura și presiunea gazelor:
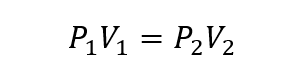
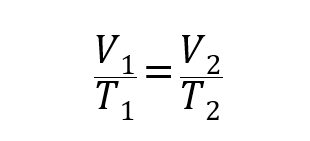
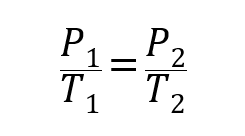
Unde P1, V1 Da T1sunt presiunea inițială, volumul și, respectiv, temperatura gazului și P2, V2 Da T2 sunt finale.
Astfel, raportând cele trei legi, obținem Legea generală a gazelor,
PV / T = C Unde C este o constantă care depinde de cantitatea de gaz.
Exemple de gaze ideale
gaz ideal este un model teoretic care reprezintă un gaz care nu există cu adevărat. Este un instrument pentru a facilita un număr mare de calcule matematice, deoarece simplifică foarte mult comportamentul complex al unui gaz. Acest gaz este considerat a fi format din particule care nu se atrag și nu se resping reciproc și ale căror coliziuni sunt absolut elastice. Este un model care eșuează dacă gazul este supus presiunilor ridicate și temperaturilor scăzute.
ecuație generală gazul ideal rezultă din combinația legilor Boyle-Mariotte, Charles și Gay Lussac cu legea lui Avogadro. Legea lui Avogadro afirmă că, dacă substanțe gazoase diferite sunt conținute în volume egale și supuse la aceeași presiune și temperatură, atunci acestea au aceleași număr de particule. Astfel, ecuația ideală a stării gazului este: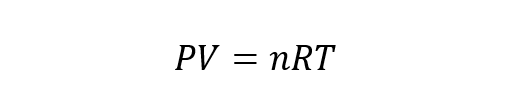
Unde n este numărul de moli ai gazului și R este constanta gazului egală cu 8,314 J / Kmol.
Nu este posibil să se facă o listă specifică a gazelor ideale, deoarece este o gaz ipotetic. Pot enumera un grup de gaze (inclusiv gaze nobile) al căror tratament poate fi aproximat cu cel al gazelor ideal, deoarece caracteristicile sunt similare, atâta timp cât condițiile de presiune și temperatură sunt normal.
- Azot (N2)
- Oxigen (O2)
- Hidrogen (H2)
- Dioxid de carbon (CO2)
- Heliu (El)
- Neon (Ne)
- Argon (Ar)
- Krypton (Kr)
- Xenon (Xe)
- Radon (Rn)
Exemple de gaze reale
gaze reale Sunt cei care au un comportament termodinamic și de aceea nu urmează aceeași ecuație de stare ca gazele ideale. La presiune ridicată și temperatură scăzută, gazele trebuie considerate inevitabil ca fiind reale, întrucât în acest caz interacțiunile dintre particulele lor cresc.
diferență substanțială între gazul ideal și gazul real este că acesta din urmă nu poate fi comprimat la nesfârșit, dar capacitatea sa de compresie este relativă la nivelurile de presiune și temperatură.
Au fost dezvoltate diferite ecuații pentru a explica comportamentul gazelor reale. Una dintre cele mai importante este cea oferită de Van der Waals în 1873, care trebuie aplicată în condiții de presiune ridicată. Ecuația lui Van der Waals este reprezentat ca:
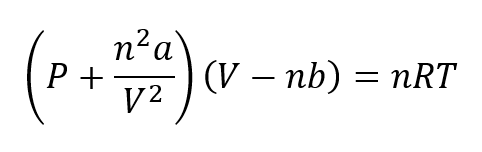
Unde laDa bsunt constante referite la natura fiecărui gaz.
Următoarea listă prezintă câteva exemple de gaze reale, deși puteți adăuga și cele care deja au fost enumerate drept gaze ideale, dar de data aceasta într-un context de presiune ridicată și / sau scăzută temperatura.
- Amoniac (NH3)
- Metan (CH4)
- Etan (CH3CH3)
- Etenă (CH2CH2)
- Propan (CH3CH2CH3)
- Butan (CH3CH2CH2CH3)
Urmărește cu:


