20 Exemple de obligațiuni covalente
Miscellanea / / July 04, 2021
O mulțime de compuși chimici sunt alcătuite din molecule care, la rândul lor, sunt compuse din atomi. Pentru a forma molecule, atomii se unesc formându-se legături chimice.
Legăturile chimice nu sunt la fel: depind practic de caracteristicile electronice ale atomilor implicați, de valorile lor de electronegativitate, printre alți factori. Cele mai frecvente tipuri de legături sunt: legături ionice si legaturi covalente.
Legături covalente se formează între atomi nemetalici ai acestora element chimic, între atomii nemetalici ai diferitelor elemente cu o diferență de electronegativitate mai mică sau egală cu 1,7 și între a metaloid și hidrogen. De exemplu: diclor, oxigen molecular, apă.
Legătura covalentă se formează atunci când doi dintre acești atomi împart electronii ultimului lor nivel de energie pentru a îndeplini Regula octetului, care stabilește că ionii diferitelor elemente chimice găsite în Tabelul periodic tind să-și completeze ultimele niveluri de energie cu 8 electroni, astfel încât moleculele să capete o stabilitate similară cu cea a gaze nobile.
Prin urmare, modul în care aceste substanțe sau compuși chimici ating stabilitatea este prin împărtășirea unei perechi de electroni (câte unul din fiecare atom). În acest fel, perechea partajată de electroni este comună celor doi atomi și, în același timp, îi ține împreună.
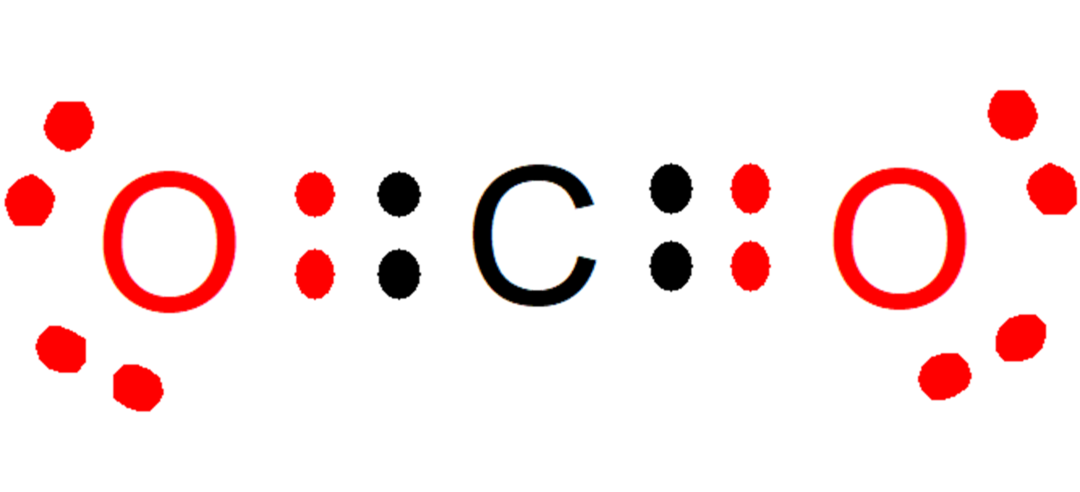
De exemplu, în dioxid de carbon (CO2), fiecare oxigen contribuie cu doi electroni (culoare roșie) la legătura cu carbonul, în timp ce carbonul contribuie cu doi electroni (culoare neagră) la fiecare legătură cu fiecare oxigen. În compusul format, 8 electroni rămân pe fiecare atom și astfel se îndeplinește regula Octetului.
Tipuri de linkuri
Există fundamental trei tipuri de legături covalente, deși este important să se clarifice că nicio legătură nu este absolut covalentă sau absolut ionică. Toate legăturile au un anumit procent de covalentă și ionică, de fapt, legătura ionică este uneori considerată ca o „supraevaluare” a legăturii covalente. În acest sens, pot apărea următoarele tipuri de legături covalente:
Substanțe compuse din molecule covalente
substanțe care conțin molecule covalente poate apărea în orice stare a materiei (solid, lichid sau gazos) și, în general, sunt dirijori slabi ai Fierbinte și a electricitate.
Există substanțe covalente moleculare și substanțe covalente reticulare. covalenți moleculari au puncte de fierbere și de topire scăzute, sunt solubile în solvenți nepolari (cum ar fi benzenul sau tetraclorura de carbon) și sunt moi în stare solidă. rețea covalentă formează rețele cristaline, deci au puncte de topire și fierbere mai ridicate și sunt solide dure, insolubile.
Exemple de legături covalente
Se pot da numeroase exemple de compuși sau substanțe care conțin legături covalente:
- Difluor
- Dibromo
- Diclor
- Diyodo
- Oxigen molecular
- Apă
- Amoniac
- Dioxid de carbon
- Metan
- Propan
- Glucoză
- Azot molecular
- Cuarţ
- Parafină
- Motorină

Urmărește cu: