Exemplu de analiză volumetrică
Chimie / / July 04, 2021
Pe Chimie analitică, Volumetrie este o metodă de analiză care constă din Măsurarea volumului de reactiv necesar pentru a reacționa stoichiometric cu analitul, care este substanța care urmează să fie determinată.
Reacționează stoichiometric se referă la substanțele care interacționează chimic, conform proporție care marchează ecuația chimică deja echilibrat.
Se numește substanța care urmează a fi investigată Analit. Din această substanță, se va lua ca probă un volum cunoscut și exact măsurat, pe care îl vom numi Alicot, conținut într-un balon Erlenmeyer pentru a începe analiza.
Concepte de analiză volumetrică
Analiza volumetrică, fiind un tip de Analiza chimica, duce a implicat o reacție chimică. Această reacție chimică va fi efectuată între eșantion cu o cantitate necunoscută de substanță investigată și o cantitate cunoscută de altă substanță, capabilă să reacționeze cu prima.
Substanțele de reacție vor fi în soluție apoasă, iar volumele de soluții care au interacționat pentru a ajunge la sfârșitul reacției vor fi măsurate, care vor fi vizibile grație unui indicator care va da culoare în interiorul balonului.
În analiza volumetrică, soluția apoasă de Concentrația cunoscută se numește soluție standard, Standard sau Titrant, și va servi ca referință pentru, încheierea reacției, pentru a face calculul care va dezvălui cantitatea de substanță investigată.
Se numește această procedură de reacționare a ambelor soluții Grad chimic o Evaluarea, care este partea fundamentală a analizei volumetrice. Constă în a merge turnând treptat Soluția standard (Titrant) în alicotă (Eșantion), până când indicatorul arată schimbarea cu o diferență de culoare.
A Indicator Este o substanță chimică care este adăugată la Aliquot, care prezintă o colorare și că, atunci când reacția se termină, își va schimba culoarea.
O analiză volumetrică constă dintr-o serie simplă de pași:
1.- Pregătirea soluției standard
2.- Pregătirea probei sau a alicotei
3.- Grad chimic
4.- Măsurarea volumului
5.- Calculul substanței investigate.
Până la punctul în care au făcut-o deja a reacționat pe deplin cele două substanțe, se numește Punct de echivalare.
Ca în orice metodă chimică de analiză, în analiza volumetrică există cerințe pentru rezultate bune:
-Reacția chimică trebuie să fie Selectiv, adică soluția standard va reacționa doar cu proba.
-Reacția chimică trebuie să fie Stoichiometric, adică, respectați proporțiile marcate în ecuația chimică echilibrată.
-Reacția chimică trebuie să fie Cantitativ; se referă la finalizarea 99,9% la punctul de echivalență.
-Trebuie să existe un punctul final detectabil în reacție, care va fi mai bine confirmat de indicator.
Model principal
Tipare primare Sunt substanțe de puritate ridicată a căror concentrație în soluție este calculată direct din cantitatea cântărită și din volumul utilizat de apă.
A) Da, poate fi reacționat cu soluții de lucru, să cunoască concentrațiile acestora din urmă și să le transforme în soluții standard.
Exemple de modele principale sunt:
-Carbonat de sodiu (Na2CO3): Se utilizează pentru standardizarea acizilor, cum ar fi acidul sulfuric.
-Biftalat de potasiu: este standardul principal pentru a prepara soluții standard de baze, cum ar fi hidroxidul de sodiu.
-Clorură de sodiu (NaCl): Se utilizează pentru standardizarea soluțiilor de nitrat de argint.
-Carbonat de calciu (CaCO3): Standard primar pentru EDTA (etilen diamină acid tetraacetic).
Un model primar trebuie să îndeplinească mai multe caracteristici esențiale:
Trebuie să aibă un Puritate înaltă, Stabilitatea atmosferică, Absența apei de hidratare, Cost redus și ușor de obținut, Y Greutate echivalentă mare.
Clasificarea analizei volumetrice
În funcție de speciile chimice cu care lucrați pentru a face o analiză, va fi tipul de volumetrie:
Volumetrie acido-bazică: Funcționează, fie cu un acid, fie cu o bază, pentru a analiza probele care conțin acizi sau baze.
Volumetria precipitațiilor: Numită și Argentometrie, folosește o soluție standard de nitrat de argint pentru a determina câte cloruri sunt într-o probă.
Volumetrie de complexitate: O soluție standard a unui agent de complexare, cum ar fi EDTA, este utilizată pentru a măsura concentrația de duritate, adică carbonat de calciu și magneziu, în apă.
Volumetrie REDOX: Reacția are loc între o substanță oxidantă și o substanță reducătoare.
Indicatori
Dintre numeroșii indicatori utilizați în Volumetrics, trei se remarcă:
1.- Portocaliu de metil: Este nevoie de o colorație portocalie în alicotă, care va fi titrată cu un acid. Când se atinge punctul de echivalență, indicatorul va deveni galben.
2.- Fenolftaleină: Este transparent la început în alicotă, care va fi intitulată cu o bază. Când se atinge punctul de echivalență, indicatorul va deveni roz.
3.- Negru Eriocrom: Este indicatorul utilizat pentru a determina duritatea în apă. La început este purpuriu în alicot, până când este titrat cu un agent de complexare. La sfârșitul reacției, devine albastru.

Instrumentele într-o analiză volumetrică
Într-o analiză volumetrică, vor fi utilizate o serie de instrumente care, dacă nu sunt disponibile, nu pot fi dezvoltate în mod adecvat:
1.- Balon volumetric: Este un recipient ca un bec în partea sa inferioară, turtit în partea de jos, care are o coloană subțire în care se adaugă lichidul. Are un semn pentru a indica unde ar trebui să fie meniscul lichidului, astfel încât să acopere volumul exact. Este folosit pentru a conține soluții standard; datorită acurateței volumului său, se asigură o concentrație cunoscută.

2.- Pipete: Sunt tuburi subțiri gradate care permit măsurarea fiabilă a cantităților exacte de lichid. Sunt disponibile până la 25 de mililitri și permit prelevarea de probe precise.
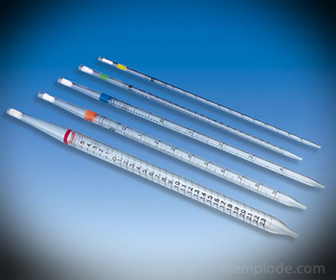
3.- Buretă: Este un tub alungit cu o capacitate de 50 mililitri, care va conține soluția standard. La unul dintre capetele sale are o supapă de reglare a debitului care va scurge Soluția în Alicot.
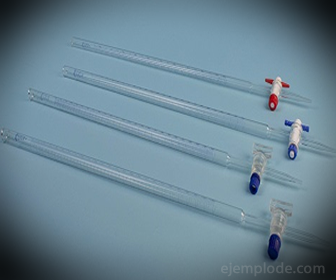
4.- Baloane Erlenmeyer: Sunt recipiente cu o bază plană, de formă conică, care se termină într-o margine cilindrică. Acest design le face adecvate pentru titrări chimice, deoarece nu permit agitarea soluțiilor pentru a le revărsa. Pentru a asigura un rezultat de încredere, vor fi necesare minimum trei dacă se vor efectua teste repetitive.

Calcule într-o analiză volumetrică
Pe măsură ce soluțiile apoase sunt tratate, cantitățile importante pentru o analiză volumetrică sunt concentrarea și volumul.
Ecuația principală a volumetriei se bazează pe patru date principale:
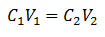
C1= Concentrația probei (necunoscută)
V1= Volumul alicotei, cu care sa lucrat analiza
C2= Concentrația soluției standard utilizate pentru a atinge punctul de echivalență
V2= Volum Soluție standard necesară pentru a ajunge la sfârșitul reacției
Datele sunt substituite în ecuație, lăsând doar concentrația căutată ca necunoscută. Desigur, toate datele trebuie să fie pe aceleași unități.
Exemple de analiză volumetrică
Determinarea clorurilor (Cl-) prin argentometrie, cu azotat de argint.
Determinarea bromurilor (Br-) prin argentometrie, cu azotat de argint.
Determinarea cianurilor (CN-) prin argentometrie, cu azotat de argint.
Determinarea carbonatului de magneziu (MgCO3), prin complexometrie, cu EDTA.
Determinarea carbonatului de calciu (CaCO3), prin complexometrie, cu EDTA.
Analiza acidului sulfuric (H2SW4) cu hidroxid de sodiu (NaOH).
Analiza hidroxidului de sodiu (NaOH) cu acid clorhidric (HCl).
Determinarea antimoniului (III) cu permanganat de potasiu (KMnO4).
Determinarea arsenului (III) cu permanganat de potasiu (KMnO4).
Determinarea titanului (III) cu permanganat de potasiu (KMnO4).
Determinarea molibdenului (III) cu permanganat de potasiu (KMnO4).
Determinarea fierului (II) cu permanganat de potasiu (KMnO4).
Determinarea ionului oxalat cu permanganat de potasiu (KMnO4).



