Exemplu de chimie organică
Chimie / / July 04, 2021
Chimie organica Este partea chimiei generale care se ocupă de studiu și clasificarea funcțională a compușilor chimici al căror element structural este Carbon, prezent din abundență în materie vie; astfel se creează un univers bine diferențiat al Chimiei anorganice, dedicat compușilor chimici clasificați drept minerale.
Atomul de carbon are patru electroni în ultima carcasă a configurației sale electronice. Această caracteristică, împreună cu cea a razei sale atomice, îi permite să fie unită prin legături covalente cu altele atomi ai aceluiași element, în numeroase lanțuri, formând o mare diversitate de compuși chimici grajd.
Puteți verifica Legaturi covalente.
Astfel de compuși chimici, pe lângă atomii de carbon care le conferă structura lor primordială, conțin atomi de hidrogen ca principal complement pentru valența carbonului. În plus, în această diversitate de compuși, există cei cu intervenția atomilor de oxigen, Azot, halogeni, sulf și chiar fosfor, elemente alcaline și alcalino-pământoase și metale ale tranziție. În funcție de cine este implicat în moleculă, aceasta va fi proprietățile fizice și chimice ale substanței finale.
compusi organici sunt prezente pe tot parcursul materie vie; promovează și susține pe toți funcții biologice, spre deosebire de substanțele anorganice sau minerale, care au fost utilizate de oameni în scopuri comerciale, pentru experimentare sau pentru îndeplinirea anumitor sarcini domestice.
Istoria chimiei organice
Înainte de 1828, se făcea deja distincția între chimia organică și chimia anorganică. Materia organică a fost asociată cu o creație prin intermediul unui "forta vitala", și către anorganic cu non-viu, cu mineral. Având în vedere aceste concepții, nu ne-am putea aștepta să obținem compuși organici din materiale anorganice în laborator.
In orice caz, în 1828 Friedrich Wöhler (1800-1882) au reușit să prepare o substanță organică, CO uree (NH2)2, un produs important al metabolismului animalelor, din compuși anorganici. Tratament Cianat de plumb Pb (CNO)2 cu Amoniac NH3 a obține Cianat de amoniu NH4CNO; Acest compus a fost format, într-adevăr, dar când soluția a fost fiartă pentru a cristaliza cianatul de amoniu, a fost transformat în uree.
Această schimbare chimică este un exemplu de Regrupare internă, în care numărul sau clasa de atomi din moleculă nu se schimbă, ci doar ordinea lor în cadrul ei. Aceste tipuri de transformări sunt foarte frecvente în chimia organică.
Descoperirea lui Wöhler a inițiat abandonarea teoriei forței de viață, mai târziu complet aruncat fiind urmat de prepararea multor alți compuși organici din laborator. În ciuda acestui fapt, calificativele organice și anorganice există, deoarece compușii anorganici sunt legați de produsele minerale iar compușii organici, care sunt de fapt compuși de carbon și hidrogen și derivații lor, sunt de tipul produs de organismele vii.
Deși legile chimiei generale se aplică în mod egal ambilor compuși, diferite cauze justifică și fac necesară această diviziune. Astfel, compușii organici și anorganici diferă prin diferite proprietăți, cum ar fi: lor Solubilitate preferat în solvenți organici (eter, alcool, cloroform etc.) și, respectiv, în apă Stabilitate (compușii organici se descompun la temperaturi relativ scăzute) și Natura reacțiilor; pentru compușii anorganici sunt ionici, simpli și practic instantanei, iar pentru compușii organici sunt covalenți, complecși și lenti.
Compusi organici
Se cunosc compuși de carbon cu lanțuri de până la nouăzeci de atomi. lanţuri Pot fi atomi de carbon liniare și ramificate și au legături covalente simple sau au legături duble sau triple. Se știe că peste 2.500 de compuși conțin doar carbon și hidrogen (Hidrocarburi).
Izomerismul compușilor organici
În compușii anorganici, o formulă reprezintă în general un singur compus; astfel, există o singură substanță cu formula H2SW4. Molecula de acid sulfuric conține doi atomi de hidrogen, unul de sulf și patru de oxigen, într-un aranjament specific și unic. În compușii organici este rar ca acest lucru să se întâmple. Astfel, de exemplu, există doi compuși care răspund la formula C2H6Sau, alcool etilic sau etanol și dimetil eter.

Cu cât este mai complexă molecula, adică cu cât este mai mare numărul de atomi de carbon, cu atât este mai mare numărul de izomeri posibili.
Analiza compusului organic
Analiza unui compus organic cuprinde analiza calitativa, analiza cantitativa si Analiza funcțională. În cazul presupunerii că compusul este într-o stare impură, acesta este purificat anterior de Cristalizare, Distilare, Sublimarea, Extracţie, etc. Criteriul de puritate poate fi evaluat pe baza constantelor sale fizice, cum ar fi punctul de topire, punctul de fierbere, densitatea, solubilitatea, forma cristalină, indicele de refracție etc.
analiza calitativa Se verifică investigând prezența elementelor care alcătuiesc compusul, în special carbonul, hidrogenul și azotul și, uneori, halogenii, sulful și fosforul.
analiza cantitativa Se realizează folosind ca bază metodele utilizate pentru analiza calitativă. Punctul de plecare este o anumită cantitate de substanță care suferă arderea, iar dioxidul de carbon este colectat și cântărit. carbon și vapori de apă formați pentru a calcula procentul de carbon și hidrogen din compus. Rezultatele analizei cantitative facilitează calculul formulă empirică, deși formula moleculară poate fi găsită numai după determinarea greutății moleculare a substanței. Dar problema nu este încă rezolvată, deoarece aceeași formulă moleculară poate corespunde unor izomeri diferiți.
Clasificarea compușilor organici
Conform structurii lor, compușii organici sunt împărțiți în compuși alifatic, aromat Da heterociclice. Compușii alifatici sunt înrudiți cu metanul CH4, sunt cu lanț deschis, cu excepția cicloparafinelor și își datorează numele faptului că grăsimile animale și vegetale aparțin acestui grup.
compuși aromatici, lanț închis, strâns legat de benzen, C6H6, și își datorează numele faptului că mulți dintre ei au mirosuri parfumate, plăcute.
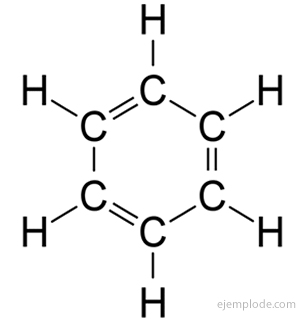
Inel de benzen
compuși heterociclici Sunt compuși cu lanț închis în care există un alt element decât carbonul în inel.
Prin constituția lor, acestea sunt:
Hidrocarburi, care la rândul său, datorită tipului de legături pe care le are, este clasificat ca Alcani, Alchene Da Alchine. În plus, cicloalcanii, benzenul și derivații lor constituiți doar din carbon și hidrogen se află în această categorie.
Compuși heterociclici
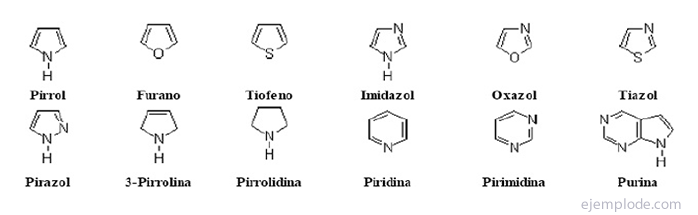
Derivați halogenați:R-X
Compuși nitro:R-NU2
Acizi sulfonici:R-SO3H
Nitrili (OR cianuri de alchil) și izonitrili:R-CN și R-NC. Ele diferă prin modul în care atomul de azot este legat de moleculă.
Alcooli:R-OH
Fenoli: Compuși pe baza unei coloane vertebrale constând dintr-un inel benzenic cu o grupare hidroxil adăugată.

Eteri:R-O-R
Mercaptani: R-SH
Thioethers:R-S-R
Tioacizi:R-COSH
Aldehidele:R-CHO
Cetone:R-CO-R
Acizi carboxilici:R-COOH
Ieși afară:R-COOM (M pentru metal)
Esteri: R-COO-R
Anhidridele: R-CO-O-OC-R
Amine:R-NH2, R-NH-R, 2R-N-R
Glucide tip Aldosa:-CHOH-CHOH-CHO
Glucide de tip cetoză:-CHOH-CO-CH2Oh
Compuși organometalici:R-M-R
Halogenuri de metal-alchil:R-MX (cunoscut și sub numele de reactivi Grignard)