Exemplu de gaze ideale și reale
Fizică / / July 04, 2021
A Gaz ideal este cel ale cărui proprietăți ca Presiunea, temperatura și volumul acoperite, ei pastreaza întotdeauna o proporție sau relație constantă între ei. Cu alte cuvinte, comportamentul său urmează Legea gazului ideal, care este reprezentată după cum urmează:
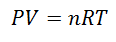
Pentru a ajunge la această formulă, pornim de la La Legea generală a statului gazos, care descrie că există o relație constantă între proprietățile gazului în orice moment al unui proces. Proprietățile despre care se vorbește sunt Presiune în sistemul în care este gazul, Volum care ocupă gazul și Temperatura de gaz.
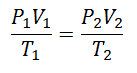
S-a decis mai devreme sau mai târziu să se formeze o expresie mai simplă, oferind constanței o scrisoare care să însoțească expresia:
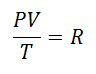
A fost numit Constanta de gaz universala la factorul R, iar valoarea sa este următoarea:
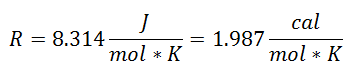
Și întrucât Constantul universal de gaz se aplică pentru fiecare mol de gaz, Numărul de moli de gaz ca încă un factor, pentru a acoperi toată substanța prezentă în sistem în timpul procesului. Vom avea deja ecuația finală în această formă:
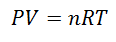
Ecuația de mai sus este Legea gazelor idealeși se aplică gazelor care sunt la o temperatură între moderată și ridicată. Astfel, se poate calcula oricare dintre variabile, determinându-le pe celelalte.
Diferența dintre gazele ideale și gazele reale
Această lege ideală a gazelor naturale nu se aplica pentru gazele care sunt la temperaturi scăzute sau aproape de punctul în care devin lichide.
Temperaturile scăzute duc la a mai puțină mișcare a particulelor gaz, iar acestea se vor stabili mai mult, ocupând un volum diferit decât atunci când au fost complet dispersate.
În plus, din același motiv, aceștia ar exercita o Presiune inegală în întregul sistem. Proporționalitatea va începe să eșueze și formula nu va avea aceeași valabilitate pentru calcule.
În acest caz, ar trebui folosite ecuații reale de gaze.
A Gaz real este cel ale cărui proprietăți nu respectă relaționarea exactă ca și în Legea gazelor ideale, astfel se modifică modul de calcul al acestor proprietăți.
Ecuații de stat pentru gaze reale
1.- Ecuația virială:
Pentru un gaz care rămâne la Temperatura constantă, relația dintre presiune și volum sau presiune și volumul specific (volumul ocupat de fiecare unitate de masă a gazului).
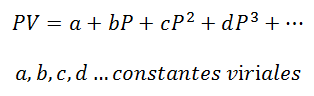
Constantele viriale sunt caracteristici ale fiecărui gaz, cu valori specifice care depind de temperatură.
Se pot face numai calcule de presiune și volum; Temperatura este determinată anterior prin respectarea procesului. Pentru aceste calcule, variabilele ecuației viriale sunt șterse:
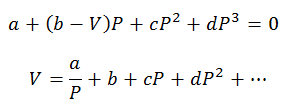
Constantele viriale pentru rezolvarea ecuațiilor sunt obținute din tabele specializate.
2.- EcuațieVan der Waals pe:
Ecuația Van der Waals este o altă expresie utilizată pentru a calcula proprietățile unui gaz real și, ca și ecuația virială, necesită și constantele sale:

Constantele sunt, de asemenea, interogate în tabele.
3.- EcuațieLeu rosuch-Kwong:
Această ecuație funcționează foarte bine pentru a face calcule cu gaze la aproape orice temperatură și presiuni medii, dar fără a fi prea mari, cum ar fi sute de atmosfere.
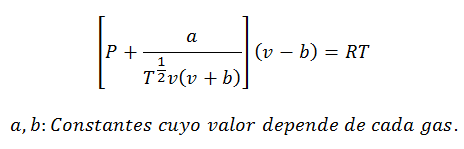
Constantele sunt, de asemenea, interogate în tabele.
Puteți șterge presiunea, temperatura și volumul pentru a vă face calculele. Rămân degajări:
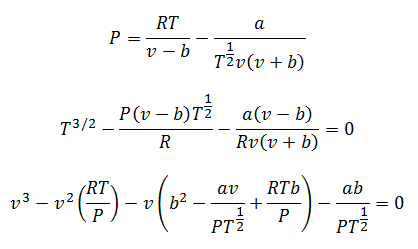
4.-Ecuația Berthelot:
Este posibil să se calculeze oricare dintre variabilele cu această ecuație. Numai că are două moduri diferite: Pentru presiuni scăzute și pentru presiuni ridicate.
Pentru presiuni scăzute:

Pentru presiuni ridicate:
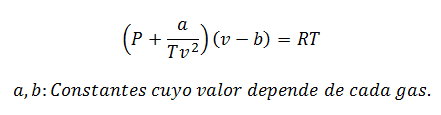
Constantele sunt, de asemenea, interogate în tabele.
5.-Ecuația factorului de compresibilitate
Această ecuație este o variantă mai simplă a Legii gazelor ideale; se adaugă doar factorul „z”, numit Factorul de compresibilitate. Acest factor este obținut din graficul factorului de compresibilitate generalizat, în funcție fie de temperatură, de presiune sau de volumul specific, în funcție de ceea ce este disponibil.
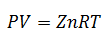
Exemple de gaze ideale și reale
Ca personaj ideal sau real Depinde de condițiile de presiune, temperatură în care se află gazul, Nu este posibil să se stabilească o listă limitată, deci este prezentată o listă de gaze, care, desigur, poate fi găsită în idealitate și realitate.
- Amoniac
- Agent frigorific R134 (DiFluoroDiCloro Etan)
- Dioxid de carbon
- Monoxid de carbon
- Oxigen
- Azot
- Hidrogen
- Dioxid de azot
- Trioxid de dinitrogen
- Pentoxid de dinitrogen
- Heptoxid de dinitrogen
- Dioxid de sulf
- Trioxid de sulf
- Clor
- Heliu
- Neon
- Argon
- Krypton
- Xenon
- Metan
- Etan
- Propan
- Butan



