Как образуются кислоты, основания и соли?
Разное / / July 04, 2021
Есть несколько теорий для определения кислоты и базы, среди которых Аррениусы, Бренстед-Лоури и Льюис.
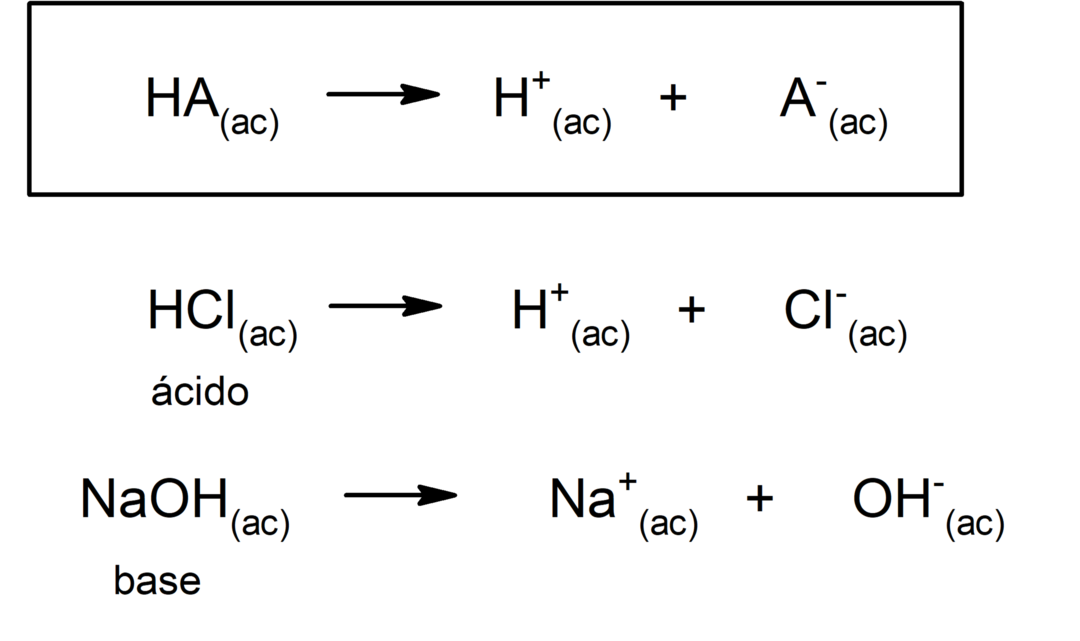
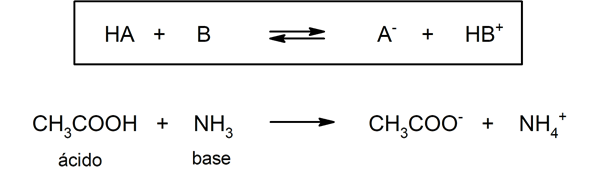
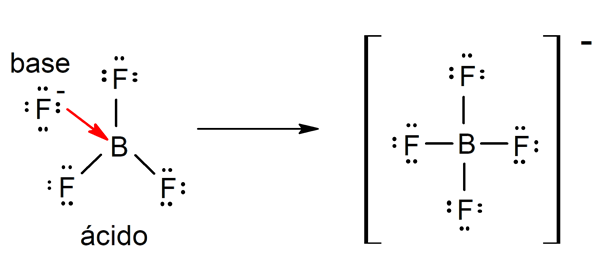
Тип кислоты окскислоты обычно формируются реакция между неметаллическим оксидом и водой, а кислоты типа гидрокислоты формируются комбинацией неметалл водородом в водном растворе. Например:серная кислота (H2ЮЗ4) это оксикислота и соляная кислота (HCl(ac)) это гидрокислота.
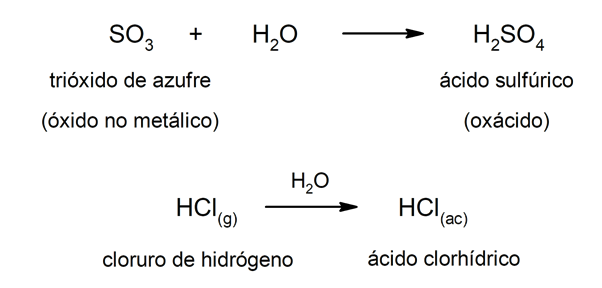
С другой стороны, основания могут образовываться в результате реакции между оксид металла И вода. Например: гидроксид магния (Mg (OH)2).
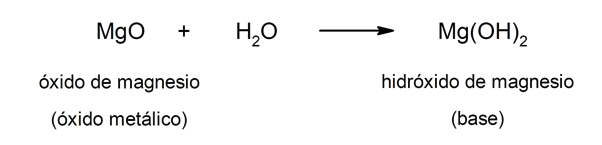
Общая характеристика кислот и оснований
В общем, кислоты кислый и едкий. Базы также разъедающий, горький на вкус, едкий при контакте с кожей и имеет мыльный оттенок. С другой стороны, кислотные растворы имеют pH менее 7, в то время как щелочные растворы имеют pH более 7.
Кислотная и щелочная сила
В склонность кислоты диссоциация и понижение pH часто называют «силой кислоты». Кислота сильна, когда она может полностью диссоциировать в водном растворе, и слабая, когда ее диссоциация происходит частично. Примеры сильных кислот - хлорная (HClO
4), серная (H2ЮЗ4), иодистоводородный (HI), бромистоводородный (HBr), соляной (HCl) и азотный (HNO3). С другой стороны, уксусная кислота (CH3COOH), цитрусовые (C6ЧАС8ИЛИ ЖЕ7) и бензойной (C6ЧАС5COOH) слабые.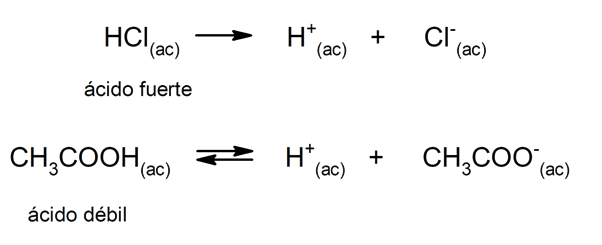
Точно так же их можно рассматривать как сильные основы те, которые полностью диссоциируют в водном растворе, и слабые, когда их диссоциация происходит частично. Примеры сильных оснований: гидроксид калия (КОН), натрия (NaOH), лития (LiOH) и магния (Mg (OH).2). С другой стороны, аммиак (NH3) - слабая база.
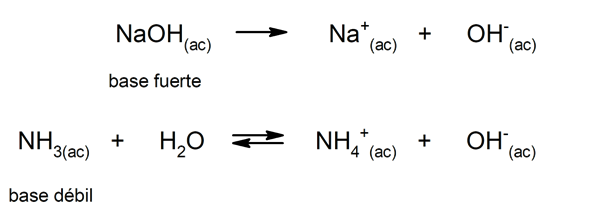
Как образуются соли?
В Вы выходите представляют собой ионные соединения различной сложности, распространенные по природе и обычно образующиеся за счет комбинации кислот с основаниями в реакции нейтрализации, которая вызывает высвобождение Воды. Они также могут образовываться в результате реакции между металлом и кислотой, металла и неметалла или реакции между различными солями.
Соли можно разделить на:
Распространение и важность
Кислоты чрезвычайно важны как в промышленность как в природа. Например, соляная кислота является частью нашей пищеварительной системы и необходима для разложения питательных соединений, присутствующих в еда. Дезоксирибонуклеиновая кислота, более известная как ДНК, составляет хромосомы, в которых содержится генетическая информация, необходимая для их кодирования. живые существа размножайтесь и развивайтесь. Борная кислота - важный компонент в стекольной промышленности.
В карбонат кальция Это очень распространенная соль в различных типах известняковых пород. По высокой доле температуры (900 ° C) из карбоната кальция, оксида кальция или негашеной извести. Добавление воды к негашеной извести дает гидроксид кальция, называемый гашеной известью, который является основой. Эти материалы они используются в строительстве.
Следуйте с:
