Определение молекулярной геометрии
Разное / / January 11, 2022
Концептуальное определение
Именно структура молекулы определяет трехмерное расположение составляющих ее атомов в пространстве.

Инженер-химик
Молекулярная геометрия в настоящее время определяется на основе Теория отталкивания электронных пар валенсийского слоя (TRPECV). Эта теория позволяет предсказать поведение химический веществ (особенно ковалентных) и помогает понять распределение электроника, приводящая к геометрия принадлежащий молекула. Это, в свою очередь, позволяет нам понять многие свойства, которые приобретают вещества.
Эта Теория основана на ряде фундаментальных столпов, которые мы рассмотрим, а затем попытаемся понять их значение. применение упражняться. Во-первых, связанные и несвязанные (валентные) электроны мыслится как море электронов, обладают одинаковым типом заряда, они отталкиваются друг от друга, поэтому всегда будут располагаться как можно дальше от центрального атома молекула.
Во-вторых, это «море» электронов или «электронное облако» образует области высокой плотности электронов, которые состоят из связей, где электроны являются общими или в парах электронов не являются общими. В свою очередь, образующиеся связи могут быть одинарными, двойными и даже тройными.
Наконец, для принять решение молекулярной геометрии очень полезно иметь структуру Льюиса, где будет подсчитываться количество электронных плотностей вокруг центрального атома, и это даст индикация от названия его геометрии и формы, которую молекула принимает в трехмерном пространстве.
Следует отметить, что эти плотности будут расположены как можно дальше друг от друга, чтобы принять наиболее стабильную структуру и где меньше отталкивание. Так сначала идентифицируется электронная геометрия, а затем молекулярная геометрия.
Шесть уровней плотности
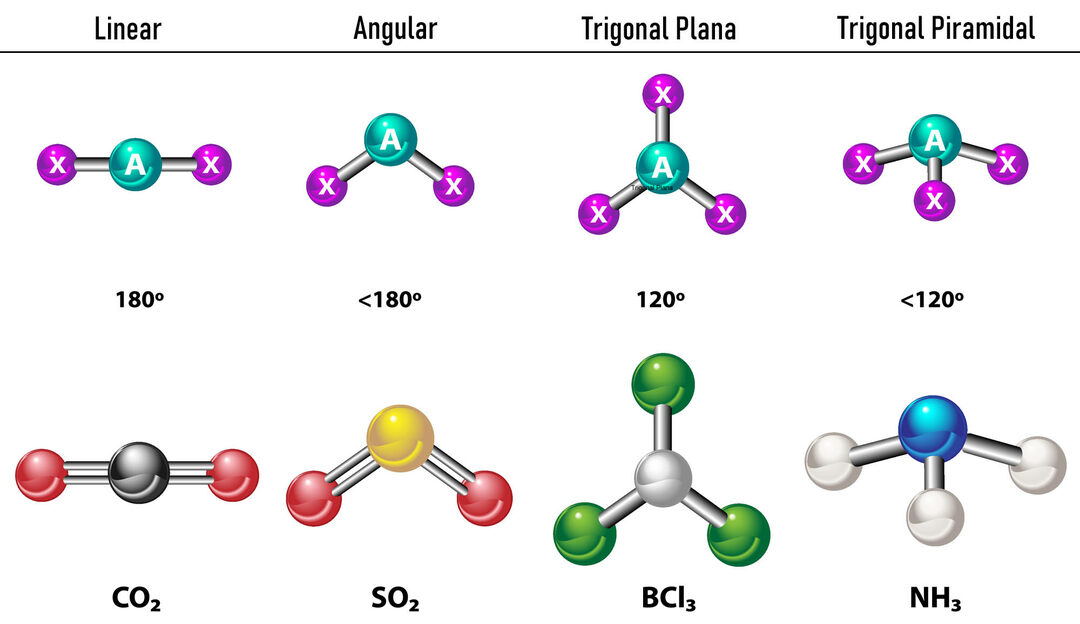
В случае, когда вокруг центрального атома две электронные плотности, связи будут располагаться на максимальном расстоянии друг от друга. между ними, то есть на 180º друг от друга, и, следовательно, их электронная геометрия линейна и молекулярно также линейна.
В случае, когда вокруг центрального атома три плотности электронов, возможны два варианта: три связи или две связи и одна несвязанная пара. Если связей три, электронная геометрия Тригональная квартира, с углами 120º между связями и молекулярной геометрией носит то же название. Теперь, если есть несвязанная пара, они сильнее отталкивают друг друга. интенсивность поэтому связанные заряды имеют тенденцию сжимать валентные углы. Угол между свободной парой и каждой связью составляет 120º, а электронная геометрия представляет собой тригональную плоскость, а молекулярная геометрия — угловую.
В случае, когда вокруг центрального атома имеется четыре плотности электронов, электронная геометрия является тетраэдрической. Если все четыре пары электронов связаны, их молекулярная геометрия по названию совпадает с их электронной геометрией, а валентный угол равен 109,5°. Теперь, если одна из пар свободна, валентный угол становится меньше (107º) и молекулярная геометрия имеет тип Треугольная пирамида. Наконец, если две пары являются свободными, а две связаны, валентный угол равен 104,5º, а молекулярная геометрия называется Угловой.
Когда плотность электронов вокруг центрального атома равна пяти, это называется Тригональная бипирамида его электронная геометрия. Если все нагрузки связаны, то между экваториально расположенными звеньями углы 120°С, а между осевыми и экваториальными 90°. Теперь молекулярную геометрию также называют тригональной бипирамидой, в то время как, имея четыре связанные пары и одну свободную пару, молекулярная геометрия искажается, образуя хорошо известную "рокер», Там имя, которое он приобретает, Искаженный тетраэдр. Тогда как, если две из пяти пар электронов свободны, а три из них связаны, он имеет Т-образную геометрию и своим названием обязан именно своей структуре. Наконец, если наоборот, три свободные пары и два связанных заряда, молекулярная геометрия линейна.
Наконец, вокруг центрального атома имеется шесть плотностей электронов, и образуется октаэдр, отсюда и его название в электронной геометрии. Точно так же молекулярная геометрия называется, если все ее пары связаны. Если у вас есть пять связанных пар и одна свободная пара, молекулярная геометрия является пирамидой с квадратным основанием. Если у вас есть четыре связанные пары и две свободные пары, молекулярная геометрия Квадратная квартира.
Рисунок: Сладкая природа
Темы молекулярной геометрии


