Определение атомной структуры
Разное / / January 13, 2022
определение понятия
Так устроен атом. Когда мы говорим об атомах, мы имеем в виду мельчайшие частицы, способные сохранять свойства определенного элемента.

Инженер-химик
В соответствии с Периодическая таблица, существует примерно 118 различных видов атомов, которые, сгруппировавшись вместе, образуют молекулы. Структуру атома изучали разные ученые, пока не пришли к тому, что мы сейчас принимаем за критерий. общее, состоящее в том, что атом состоит из двух хорошо дифференцированных зон: ядерной зоны и дополнительной зоны ядерный.
Ядерная зона образована положительно заряженными (протонами) и нейтральными зарядами (нейтронами), поэтому она составляет почти 99,99 % атомная масса несмотря на уменьшенный размер на 10-12 см. Частицы внутри удерживаются вместе ядерными силами, очень сильными силами, которые вызывают Ядерная энергия.
Несмотря на наименьшую атомную массу, внеядерная зона занимает 99,99 % массы тела. объем атома, и он заряжен отрицательно, являясь вмещающей зоной для электронов, находящихся в непрерывном движение на неопределенный срок.
Когда атом нейтрален, говорят, что число электронов и протонов равно. Теперь, когда атом теряет или приобретает электроны, оставаясь положительно или отрицательно заряженным, образуются ионные частицы, называемые катионами и анионами. В зависимости от числа приобретенных или потерянных электронов им присваивается название, например, в случае с алюминием, который является металл который образует положительный ион, так как он теряет три электрона, он называется трехвалентным катионом.
Если мы посмотрим на массы субатомных частиц, мы увидим, что они подобны в порядке протонов и нейтроны, в то время как электроны имеют меньшую массу, все они определены в периодической таблице в в Единица измерения от «ума». «ума» означает «единица атомной массы» и определяется как одна двенадцатая часть атомной массы углерода для установления эталонной величины. В свою очередь, он определяется как следующая эквивалентность:
1 а.е.м. = 1,66 х 10-24 грамм
Если мы посмотрим на порядки величины, то поймем, что это крошечная и незаметная для человеческого зрения величина. Так при чтении атомной массы элемента, например, в случае гелия мы видим, что она равна 4,002602 а.е.м. или, что то же самое, 6,64х10-24 грамма.
При определении атомной структуры элемента мы обращаемся к двум известным числам, которые позволяют нам быстро идентифицировать атом, который мы называем. Этими числами являются: атомный номер и массовое число.
Атомный номер или «Z» представляет собой количество протонов, которые атом имеет в своем ядре. Как мы уже говорили, если атом нейтрален, «Z» также соответствует количеству электронов во внеядерной зоне. Благодаря его номеру «Z» мы можем найти его в Периодической таблице, что придаст ему ряд определенных свойств. Что касается массового числа или «А», оно относится к количеству протонов и нейтронов, которые атом имеет в своем ядре. В общем случае оба числа выражаются следующим образом:
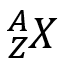
Где X представляет символ из химический элемент.
Хотя для определенного «X» «Z» уникален, «A» может варьироваться из-за существования изотопов.
Изотопы — это атомы одного и того же элемента, различающиеся числом нейтронов. Следовательно, у них может быть одинаковая «Z», то есть одинаковое количество протонов, но не одно и то же «А», поскольку нейтроны меняются от одного к другому.
Примеров изотопов в природе много, наиболее распространены изотопы углерода. Существуют следующие атомные структуры для одного и того же элемента:
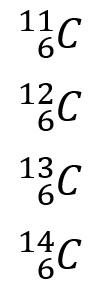
Как видим, в каждом из них количество нейтронов разное. Все виды сохраняют шесть протонов, в то время как у первого есть 5 нейтронов, у второго 6, у третьего 7 и у последнего 8. В зависимости от изотопа определяется использование. Например, изотоп Углерод-13 является наименее доступным в природе, несмотря на то, что он физически стабилен. Углерод-14 — это радиоактивный изотоп, применяемый в этой области, а графит — один из самых полезных изотопов на сегодняшний день.
Темы в атомной структуре


