30 примеров спиртов
Примеры / / November 06, 2023
спирты являются органические химические соединения которые содержат в своей структуре гидроксильную функциональную группу (-ОН), присоединенную к углероду (-С). Группа (- C – OH) называется «карбинолом». Некоторые примеры спиртов: метанол, этанол и 1-пропанол.
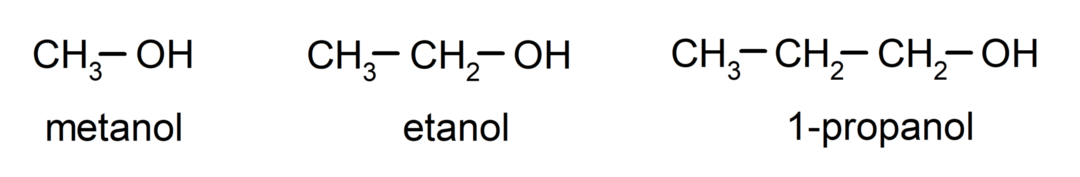
Спирты представляют собой химические соединения, имеющие различное применение в повседневной жизни, поскольку обладают антибактериальными и антисептическими свойствами. С другой стороны, они могут быть опасны для здоровья человека при бесконтрольном приеме внутрь.
Аналогично, не все алкогольные напитки могут употребляться человеком.
- Смотрите также: Амины и кетоны
Виды спиртов
В зависимости от количества атомов углерода, к которым присоединен атом углерода, имеющий присоединенную гидроксильную группу, спирт может быть:
- Первичный спирт. Атом углерода, к которому присоединена гидроксильная группа, также присоединен к одному атому углерода. Например:
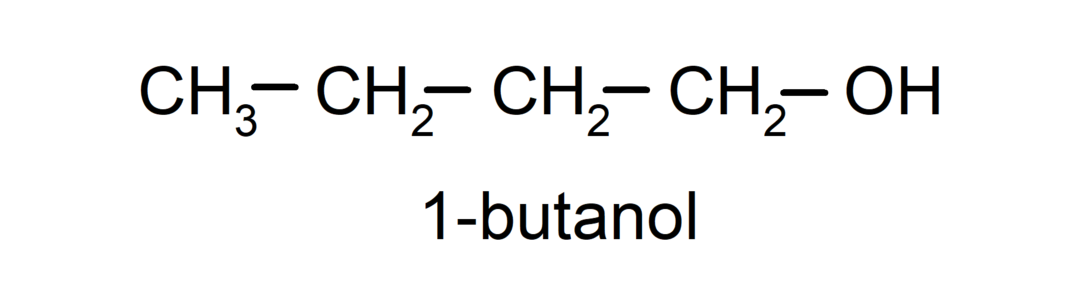
- Вторичный алкоголь. Атом углерода, к которому присоединена гидроксильная группа, также связан с двумя другими атомами углерода. Например:
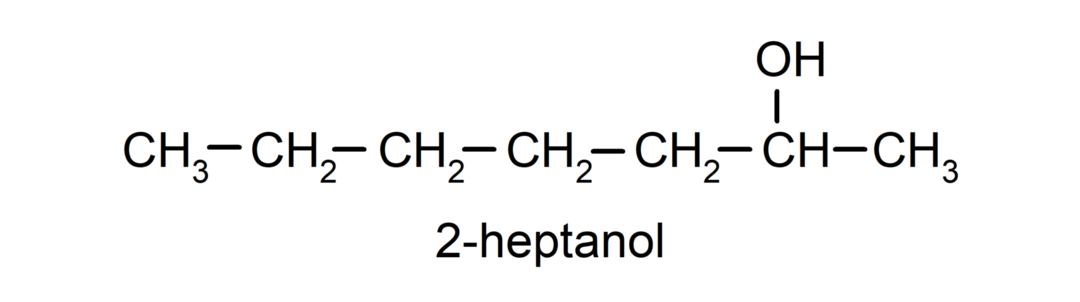
- Третичный спирт. Атом углерода, к которому присоединена гидроксильная группа, также присоединен к трем атомам углерода. Например:
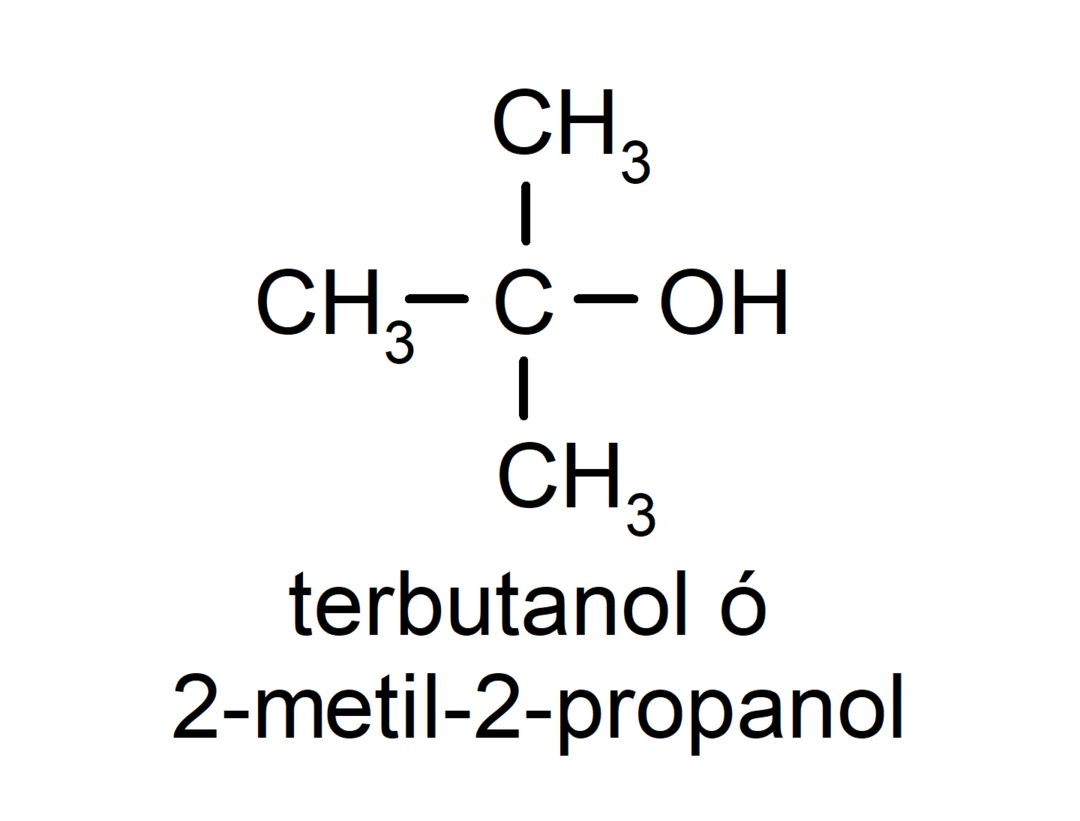
В зависимости от количества гидроксильных групп спирт может быть:
- Диол. В его структуре имеется две гидроксильные группы. Например:
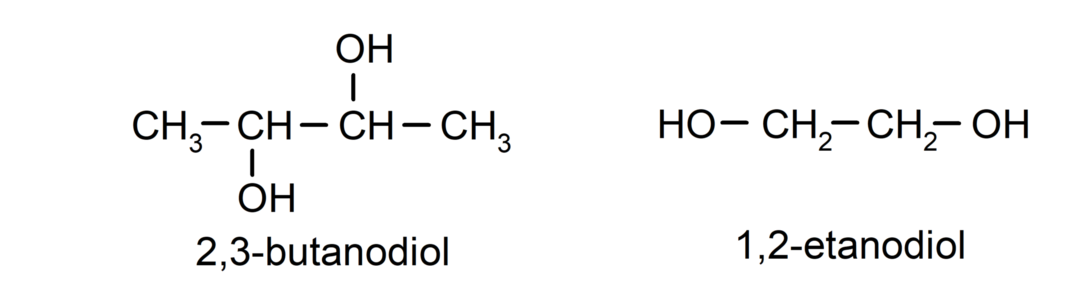
- Триол. В его структуре имеется три гидроксильные группы. Например:
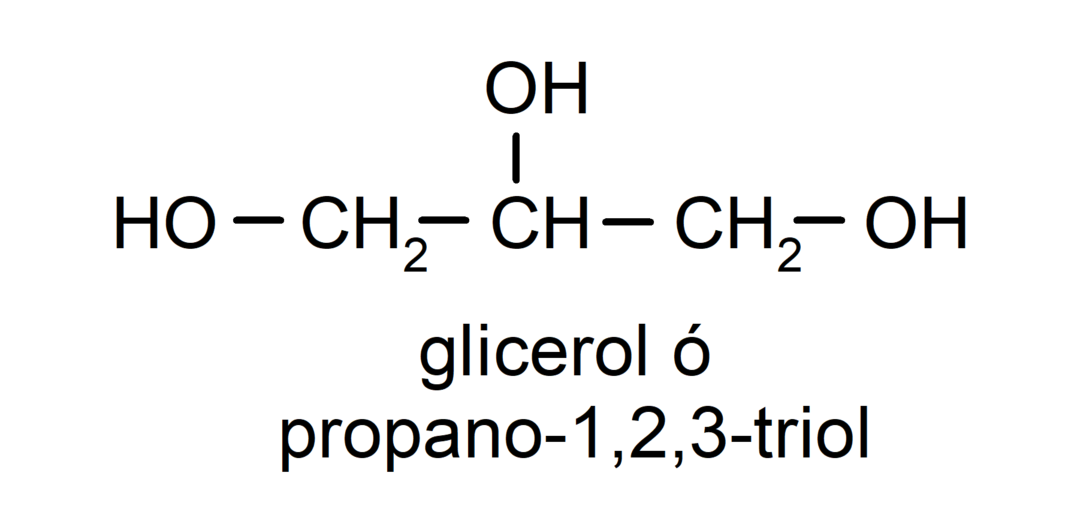
- Полиспирт. В его структуре много гидроксильных групп. Например:
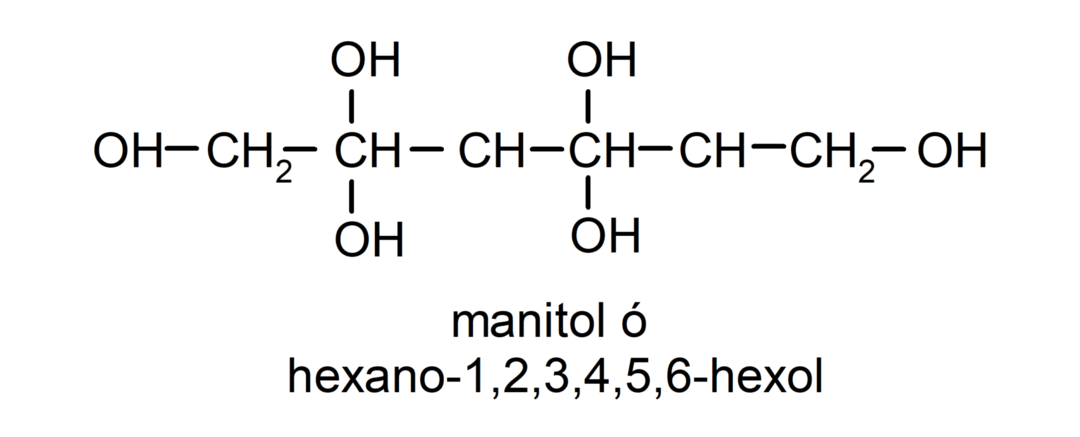
Физические свойства спиртов
Некоторые физические свойства спиртов:
- Точка кипения. Температура кипения спиртов довольно высока из-за наличия гидроксильной группы, позволяющей образовывать водородные связи. Кроме того, чем больше гидроксильных функциональных групп присутствует в углеродной цепи, тем выше Точка кипения спиртов.
- Полярность. Спирты — достаточно полярные соединения.
- Растворимость. Низкомолекулярные спирты растворимы в воде. С другой стороны, чем больше углеродная цепь спиртов, тем ниже их растворимость в воде. Кроме того, чем больше гидроксильных групп имеют спирты, тем выше их растворимость в воде.
- Агрегатное состояние. Большинство спиртов являются жидкими при комнатной температуре (25°C) и имеют характерный запах.
Химические свойства спиртов
Некоторые химические свойства спиртов:
- Спирты ведут себя как кислоты и основания.. Их поведение в качестве кислот можно увидеть в реакциях с активными металлами с выделением газообразного водорода и образованием алкоксидов.

Их поведение в качестве оснований можно увидеть в таких реакциях, как реакция метанола с бромистым водородом с образованием бромида метилоксония.
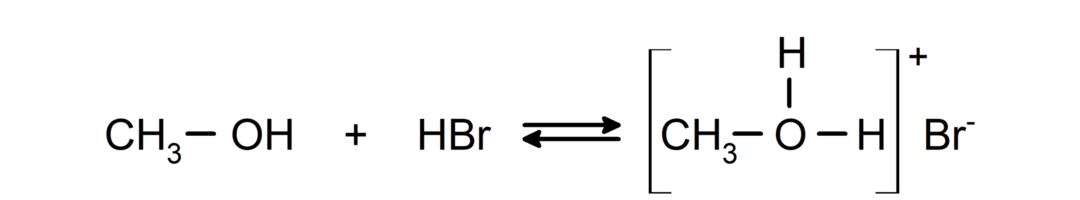
- Спирты вступают в реакции галогенирования.. Они реагируют с галогеноводородами с образованием алкилгалогенидов.
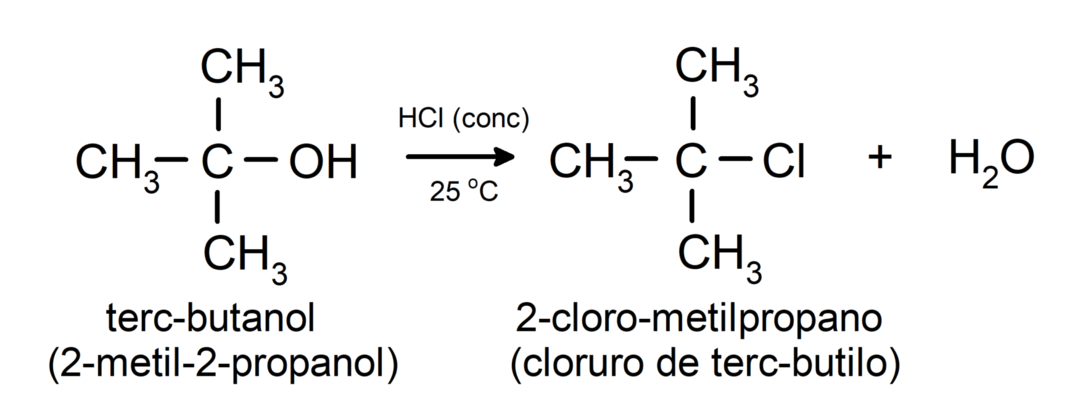
-
Спирты вступают в реакции окисления когда они реагируют с некоторыми окислителями. Продукты реакций окисления зависят от типа реагирующего спирта, т. е. от того, является ли он первичным, вторичным или третичным.
Окисление первичного спирта с образованием альдегида или карбоновой кислоты.
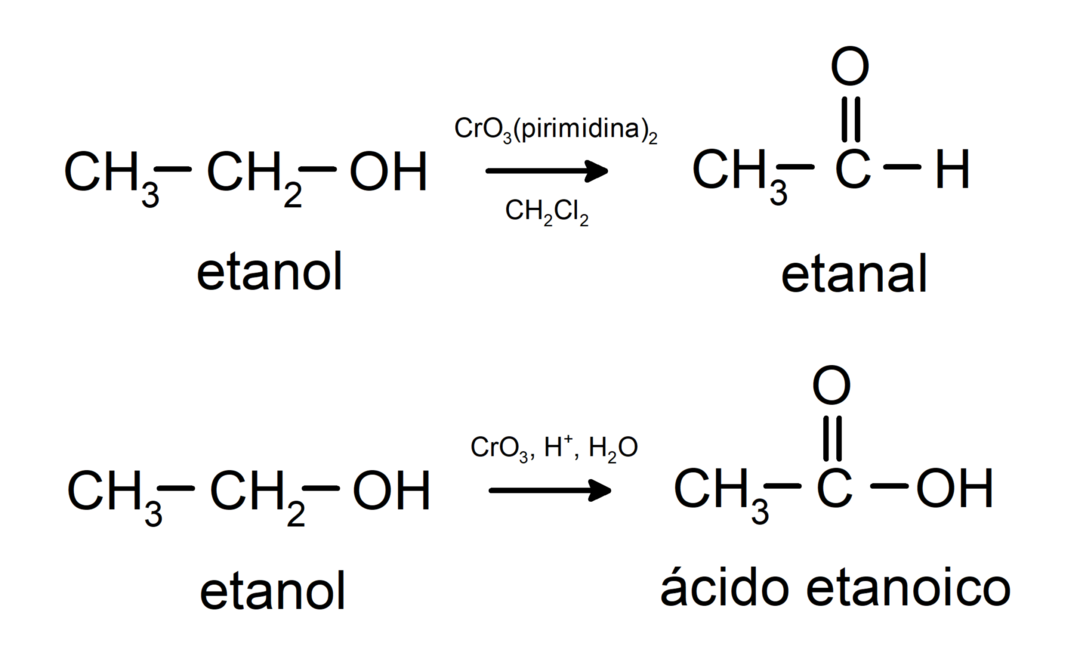
Окисление вторичного спирта с образованием кетона.
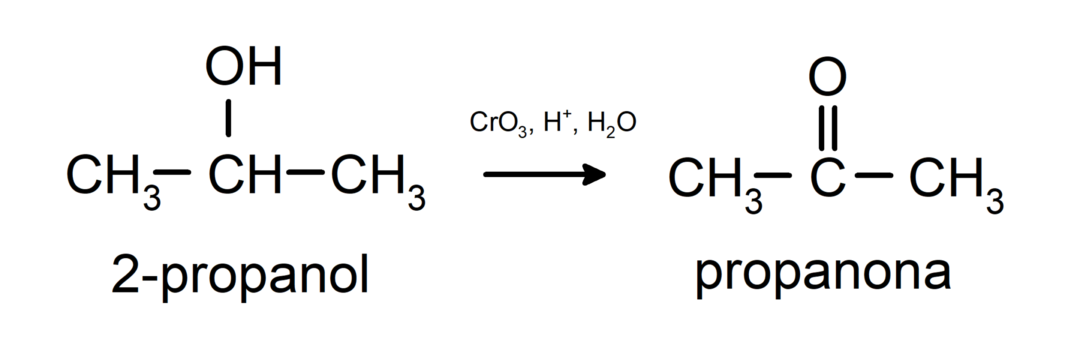
Третичные спирты не окисляются обычными окислителями. С помощью очень сильных окислителей их можно превратить в алкены, которые затем можно окислить.
Спирты, имеющие две гидроксильные группы, расположенные при соседних атомах углерода, окисляются тетраацетатом свинца с образованием двух кетонов.
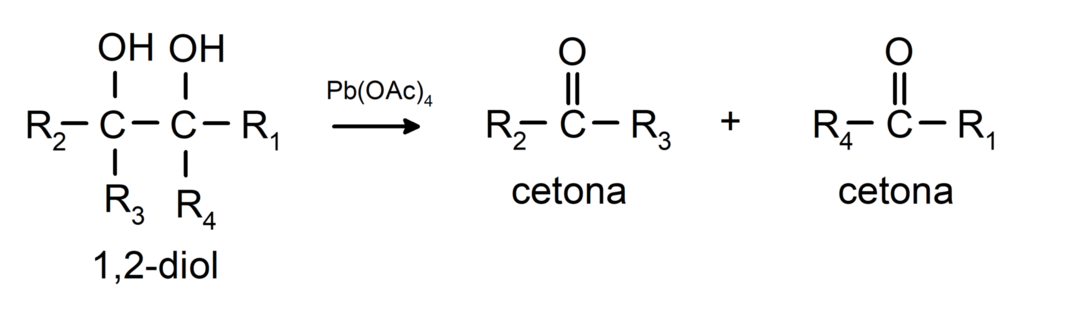
- Спирты вступают в реакцию дегидрирования.. Эти реакции происходят только с первичными и вторичными спиртами, которые при воздействии высоких температур в присутствии катализаторов выделяют водороды.
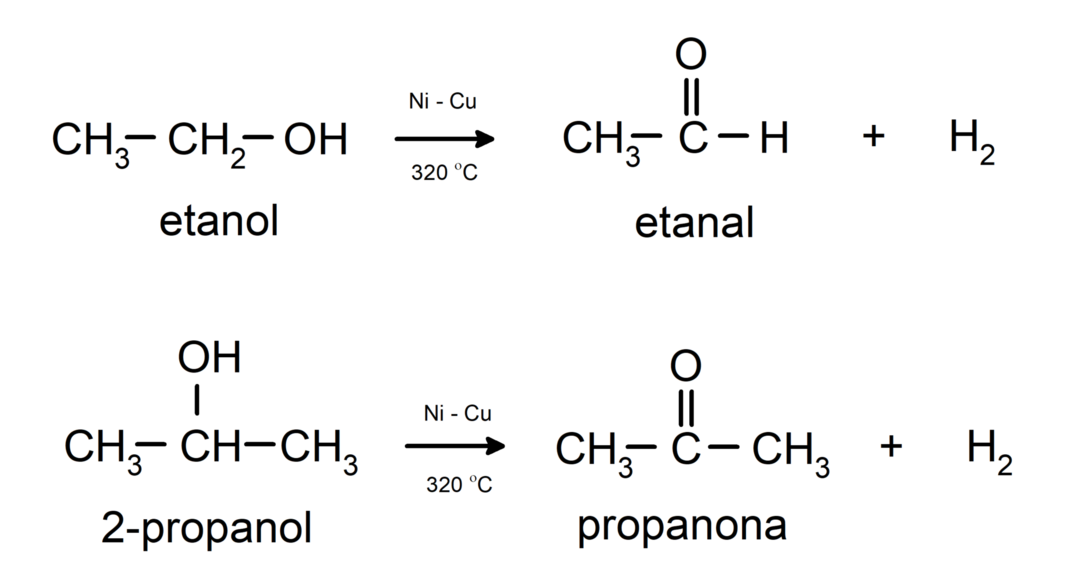
- Спирты подвергаются реакциям дегидратации.. Спирты дегидратируются с образованием соответствующих алкенов. Эта реакция протекает в присутствии кислоты и промежуточных температурах.
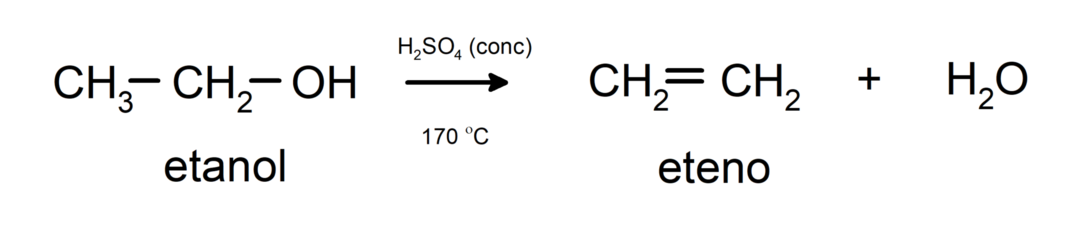
Алкогольная номенклатура
Согласно номенклатуре, установленной ИЮПАК (Международным союзом теоретической и прикладной химии), спирты называют по следующим правилам:
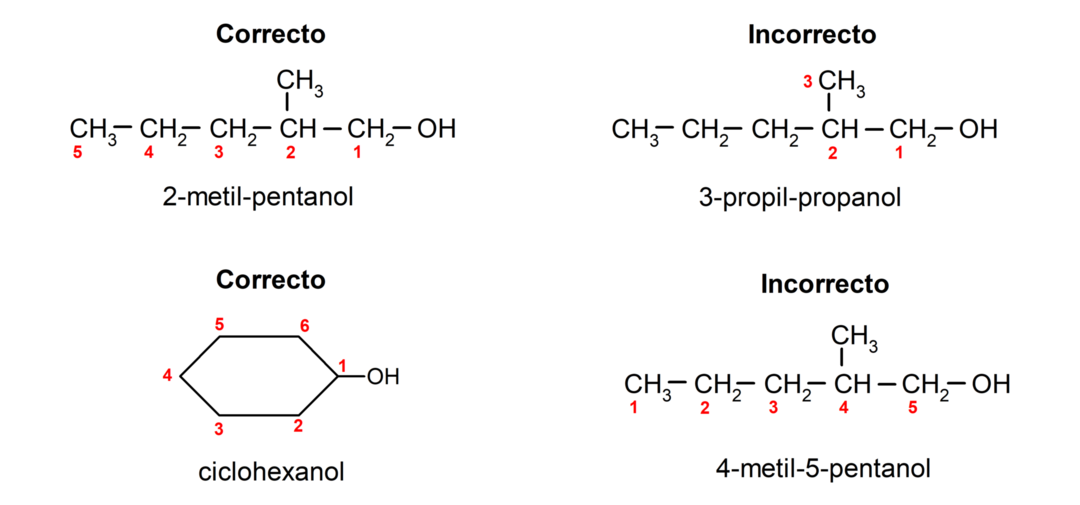
- Положение гидроксильной группы выбирают с учетом того, чтобы она занимала минимально возможный номер в углеродной цепи. Если структура спирта циклическая, то учитывают положение 1 атома углерода, к которому присоединена гидроксильная группа, и для его названия используют префикс цикло-.
- Название спирта пишется с помощью приставок, обозначающих число атомов в углеродной цепи, кроме того ставится суффикс -ол.
- Если структура спирта имеет разветвления, то в качестве основной углеродной цепи выбирают самую длинную цепь, содержащую также гидроксильную группу.
Согласно традиционной номенклатуре, спирты называются путем написания слова «спирт», а затем названия спирта. алкан, соответствующий углеродной цепи, но вместо -анового окончания алкана используется окончание -иллический.
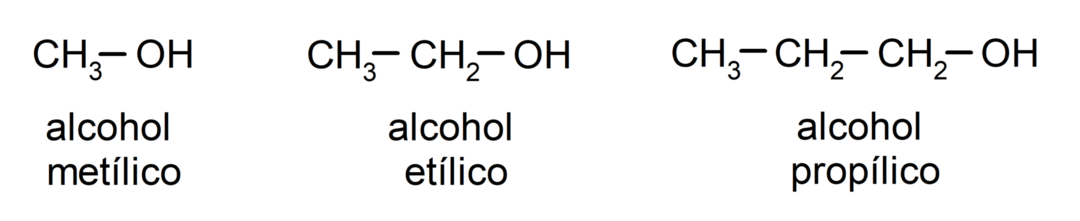
Примеры спиртов
- метанол
- спирт этиловый
- 1-пропанол
- 2-пропанол
- 1-бутанол
- 3-этилгексан-2-ол
- глицерин
- фенол
- 2-метил-2-бутанол
- 1,2-этандиол
- 1,5-гептадиен-3-ол
- 3-метил-2-бутанол
- бензилметанол
- 3-пентанол
- 2-метилфенол
- 1,2-дигидроксифенол
- циклогекснол
- 1-фенилэтанол


Использование спиртов
Наиболее распространенные области применения спиртов:
- Их используют в качестве дезинфицирующих и антисептических средств, поскольку они останавливают рост некоторых микроорганизмов. микроорганизмы или уничтожить их. Для этой цели чаще всего используются этанол и изопропиловый спирт.
- Их используют при синтезе различных химические соединения. Метанол, например, используется для получения метаналя (формальдегида).
- Их используют для производства антифриза. Метанол является одним из наиболее часто используемых для этой цели.
- Их используют в качестве растворителей в фармацевтической промышленности. Этанол является одним из наиболее часто используемых в этом смысле.
- Их используют в качестве растворителей для лаков, красителей и чернил. Для этой цели широко используется метанол.
- Они используются в качестве топлива, и существует важная тенденция к частичной замене использования ископаемое топливо за счет использования биоэтанольного топлива.
- Их используют для изготовления смол. В этом смысле используется фенол.
Опасности употребления алкоголя
Хотя сегодня употребление алкоголя является социально приемлемым, злоупотребление этим веществом порождает зависимость и привыкание.
Этанол – это спирт, присутствующий в алкогольных напитках, который при избыточном употреблении влияет когнитивные способности и может вызвать сердечно-сосудистые заболевания, цирроз печени и рак.
Кроме того, при достижении степени алкогольного опьянения, то есть состояния опьянения, если доза препарата слишком высокое содержание алкоголя может наступить алкогольная кома, которая может привести к параличу дыхания и даже смерти. смерть.
Рекомендации
- Т. К. Гейссман. (1974) «Принципы органической химии», второе издание. Редакция Reverté, S.A. ISBN: 8429171800
- Ахумада-Кортес, Дж. Г., Гамес-Медина, М. Э. и Вальдес-Монтеро, К. (2017). Употребление алкоголя как проблема общественного здравоохранения. Ра Симхай, 13(2), 13-24.
- Моррисон, Р. Т. и Бойд Р. Н. (1998). Органическая химия. Образование Пирсона.
- Вейнингер, С. Дж. и Штермиц Ф. Р. (1988). Органическая химия. Я поменял направление.
Следуйте с:
- Этиловый спирт
- Топливо
- органическая химия



