Пример ароматических соединений
Химия / / July 04, 2021
Химики сочли полезным разделить все органические соединения на два широких класса: соединения Алифатический и соединения Ароматика. Ароматические соединения - это бензол и соединения с аналогичным химическим поведением. Ароматические свойства - вот что отличает бензол от алифатических углеводородов. Молекула бензола представляет собой кольцо определенного типа. Существуют и другие соединения, также имеющие форму кольца, которые, по-видимому, структурно отличаются от бензола, но ведут себя аналогичным образом.
Оказывается, эти другие соединения напоминают бензол по своей основной электронной структуре, поэтому они также ведут себя как ароматические соединения.
Алифатические углеводороды (алканы, алкены, алкины и их циклические аналоги) реагируют главным образом добавление, в нескольких ссылках и замещение свободных радикалов, в других точках алифатической цепи.
С другой стороны, подчеркивается, что ароматические углеводороды имеют тенденцию к гетеролитическое замещение. Более того, эти же реакции замещения характерны для ароматических колец, где бы они ни появлялись, независимо от того, какие другие функциональные группы может содержать молекула. Эти последние группы влияют на реакционную способность ароматических колец и наоборот.
Молекула бензола
Бензол известен с 1825 года, и его химические и физические свойства известны лучше, чем свойства любого другого органического соединения. Несмотря на это, только в 1931 г. была предложена удовлетворительная структура для этого вещество, и потребовалось до 15 лет, чтобы оно стало широко использоваться среди химических веществ. органический. Сложность заключалась в ограниченности развития, достигнутой к тому времени структурной теорией. Окончательная структура была достигнута путем допущения нескольких важных фактов:
Бензол имеет молекулярную формулу C6ЧАС6. Известно, что бензол из-за его элементного состава и молекулярной массы содержит шесть атомов углерода и шесть атомов водорода. Проблема заключалась в том, чтобы знать расположение таких атомов.
В 1858 году Август Кекуле предположил, что атомы углерода могут быть связаны вместе, образуя цепочки. Позже, в 1865 году, он предложил ответ на проблему бензола: эти карбонатные цепи иногда могут быть замкнуты, образуя кольца.
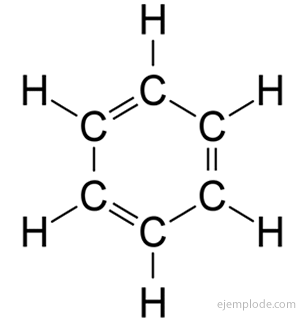
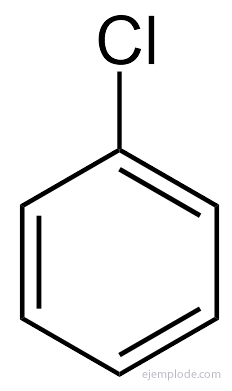
Бензол дает только монозамещенный продукт C6ЧАС5Y. Например, когда атом водорода заменяется бромом, получается только одна конфигурация бромбензола C.6ЧАС5Br; аналогично также получают хлорбензол C6ЧАС5Cl или нитробензол C6ЧАС5НЕТ2, так далее. Этот факт налагает серьезные ограничения на структуру бензола: весь его водород должен быть точно эквивалентны, то есть все они должны быть соединены с углеродом, который, в свою очередь, все равно связаны. В CH не может быть водорода.3, и другие в CH2, и другие в CH. Конечная структура монозамещенного должна быть такой же, как при замещении любого водорода в бензоле.
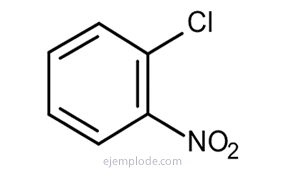
Бензол дает три изомерных дизамещенных продукта: C6ЧАС4Y2 или C6ЧАС4И З. Есть только три изомерных DiBromoBenzenes, C6ЧАС4Br2, три ChloroNitroBenzenes C6ЧАС4ClNO2, так далее. Этот факт еще больше ограничивает конструктивные возможности.
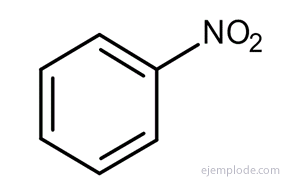
Бензол претерпевает реакции замещения, а не реакции присоединения. Бензольная структура Кекуле соответствует структуре, которую мы назвали бы циклогексатриеном. Из-за этого он должен легко реагировать путем присоединения, как и аналогичные соединения, циклогексадиен и циклогексен, что является характеристикой структуры алкенов. Но это не тот случай; в условиях, когда алкены реагируют быстро, бензол не реагирует или реагирует очень медленно. Вместо реакций присоединения бензол легко подвергается ряду реакций, все из которых подмена, как Нитрация, то Сульфирование, то Галогенирование, то Алкилирование Фриделя-Крафтса, то Ацилирование из Friedel-Crafts. В каждой из этих реакций атом или группа заменяются одним из атомов водорода бензола.
Стабильность бензола обусловлена чередующимися двойными связями, а также резонансной энергией в тот, в котором двойные связи меняют свое положение между атомами углерода, сохраняя такое же чередование структурный. Является энергия резонансной стабилизации отвечает за набор свойств, называемых Ароматические свойства.
Реакция присоединения превращает алкен в более стабильное насыщенное соединение. Но в случае бензола добавка делает его менее стабильным, разрушая кольцевую систему, поддерживаемую и стабилизируемую резонансом. Последней молекулой будет циклогексадиен. Именно из-за этого стабильность бензола приводит только к реакциям замещения.
Свойства ароматических соединений
Помимо веществ, содержащих бензольные кольца, есть много других, которые считаются ароматическими, хотя внешне они почти не похожи на бензол.
С экспериментальной точки зрения ароматические соединения - это вещества, молекулярные формулы которых предполагают высокая степень ненасыщенности, несмотря на то, что они устойчив к реакциям присоединения так характерно для ненасыщенных соединений.
Вместо этого эти ароматические соединения часто подвергаются реакциям электрофильного замещения аналогичен бензолу. Наряду с этим сопротивлением сложению и, вероятно, из-за него, есть свидетельства необычная стабильность, например, низкая теплота гидрирования и сгорания.
Ароматические вещества цикличны, обычно представляющие собой кольца из пяти, шести и семи атомов, и их физическое исследование показывает, что они имеют плоские или почти плоские молекулы. Его протоны имеют тот же тип химического сдвига в спектрах ЯМР, что и у бензола и его производных.
С теоретической точки зрения, чтобы вещество было ароматическим, его молекула должна иметь циклические облака делокализованных π-электронов выше и ниже плоскости молекулы; Кроме того, эти π-облака должны содержать всего (4n + 2) π-электронов; это означает, что делокализации недостаточно для достижения особой стабильности, которая характеризует ароматическое соединение.
Номенклатура производных бензола (ароматические соединения)
В случае многих из этих производных, особенно монозамещенных, достаточно добавить название группа заместителей для слова Бензол, такая как, например, хлорбензол, бромбензол, йодобензол, Нитробензол.
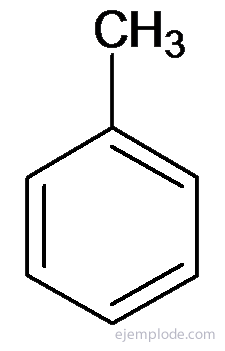
Другие производные имеют специальные названия, которые могут не совпадать с названием группы заместителя. Например, метилбензол известен только как толуол; Аминобензол в виде анилина; Гидроксибензол в виде фенола и т. Д.
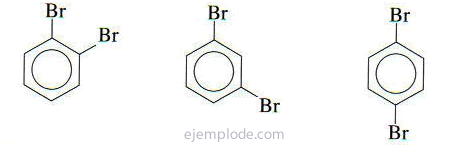
Если к бензольному кольцу присоединены две группы, необходимо не только определить, что они собой представляют, но также указать их относительное расположение. Три возможных изомера дизамещенных бензолов характеризуются приставками орто, мета и пара, сокращенно о-, м-, п-. Например: о-диБромобензол, м-диБромобензол, п-диБромобензол.
Если одна из двух групп относится к типу, который дает молекуле особое имя, соединение называется производным этого особого вещества. Например: нитротолуол, бромфенол и т. Д.
Примеры ароматических соединений
Толуол или метилбензол
Этилбензол
Изопропилбензол
Тринитро-толуол или тротил
Анилин или Аминобензол
Бензойная кислота
Глутаминовая кислота или параамино-бензойная кислота
Толуолсульфоновая кислота
Фенол или гидроксибензол
Бромфенол
Трихлорбензол
Бензол фениловый эфир
Йодобензол
Бромбензол
