50 Príklady aldehydov a ketónov
Príklady / / November 06, 2023
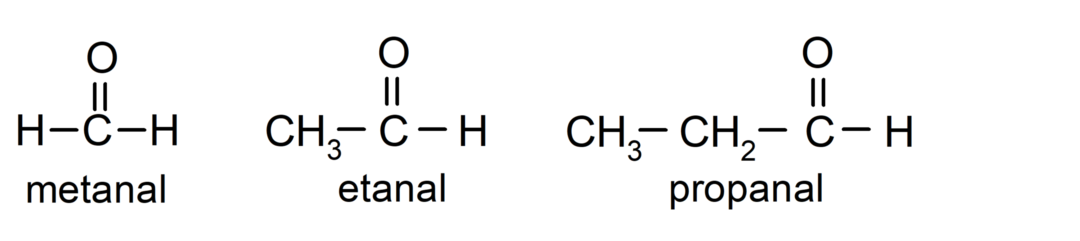
The aldehydy sú Organické zlúčeniny ktoré majú vo svojej štruktúre karbonylovú funkčnú skupinu (= C = O), ktorá je spojená s uhlíkovým reťazcom a atómom vodíka. Napríklad: metanál (nazývaný aj formaldehyd), etanál (nazývaný aj acetaldehyd) a propanal (nazývaný tiež propaldehyd).
The ketóny Sú to organické zlúčeniny, ktoré majú vo svojej štruktúre karbonylovú skupinu viazanú na dva atómy uhlíka. Napríklad: propanón (nazývaný aj acetón), butanón a 2-pentanón.
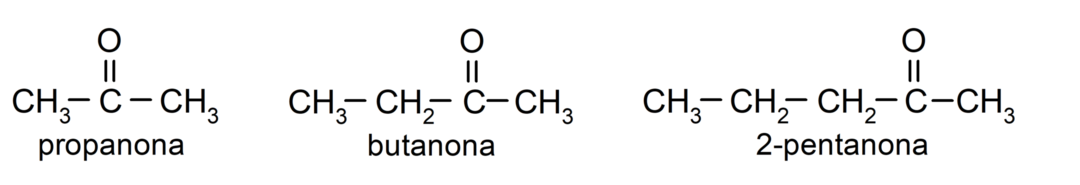
Rozdiely medzi aldehydmi a ketónmi
Hlavné rozdiely medzi aldehydmi a ketónmi sú:
- Aldehydy majú vo svojej štruktúre karbonylovú funkčnú skupinu umiestnenú na jednom terminálnom konci, zatiaľ čo ketóny majú karbonylovú skupinu umiestnenú v nekoncových polohách svojich štruktúru.
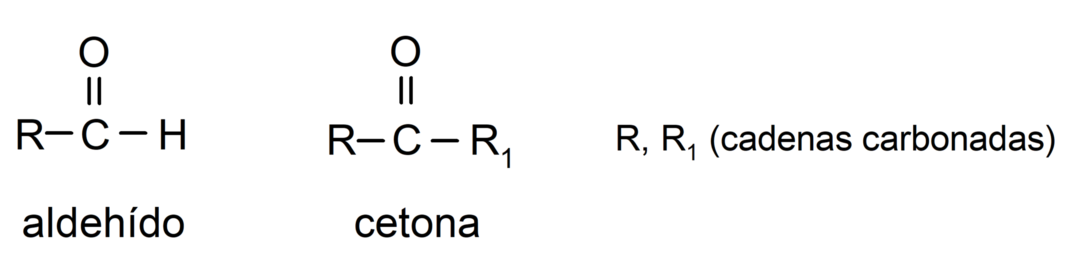
- Aldehydy sa oxidujú reakciou s Tollensovým činidlom za vzniku kovového striebra. Oxidujú aj proti Benediktovmu činidlu a vytvárajú oxid meďnatý. Ketóny nie sú oxidované ani jedným z činidiel.
- Aldehydy sa redukujú na primárne alkoholy, zatiaľ čo ketóny sa redukujú na sekundárne alkoholy.
Fyzikálne vlastnosti
Fyzikálne vlastnosti aldehydov
Fyzikálne vlastnosti aldehydov sú veľmi rôznorodé, pretože závisia od zloženia uhlíkového reťazca, ktorý je spojený s karbonylovou skupinou.
Niektorí sú:
- Aldehydy, ktoré sú najviac rozpustné vo vode, sú tie, ktoré majú menšiu veľkosť, ako je methanal a etanal.
- Prchavé aldehydy majú štipľavý a dokonca dráždivý zápach.
- Karbonylová skupina im dáva polaritu.
- Zvyčajne majú vyššie teploty varu ako chemické zlúčeniny s podobnou molekulovou veľkosťou.
Fyzikálne vlastnosti ketónov
Fyzikálne vlastnosti ketónov závisia od toho, ako sa tvorí uhlíkový reťazec, ktorý je spojený s karbonylovou skupinou.
- Mnohé ketóny majú príjemnú vôňu.
- Jeho rozpustnosť vo vode závisí od veľkosti uhlíkového reťazca pripojeného ku karbonylovej skupine. Čím menší je uhlíkový reťazec, tým bude ketón rozpustnejší vo vode.
- Karbonylová skupina im dáva výraznú polaritu.
- Majú pomerne vysoké body varu v porovnaní s chemickými zlúčeninami porovnateľnej veľkosti molekúl.
Chemické vlastnosti
Chemické vlastnosti aldehydov
Medzi chemickými vlastnosťami aldehydov môžeme nájsť:
Oxidujú sa za vzniku zodpovedajúcej karboxylovej kyselinyto znamená, že vytvorená kyselina bude mať rovnaký počet uhlíkov v uhlíkovom reťazci ako aldehyd ktoré to vyvolalo. Napríklad:
- Oxidácia Tollensovým činidlom (amoniakálny komplex striebra v zásaditom roztoku, [Ag (NH3)2]+) z etanálu produkuje kyselinu etánovú a kovové striebro.
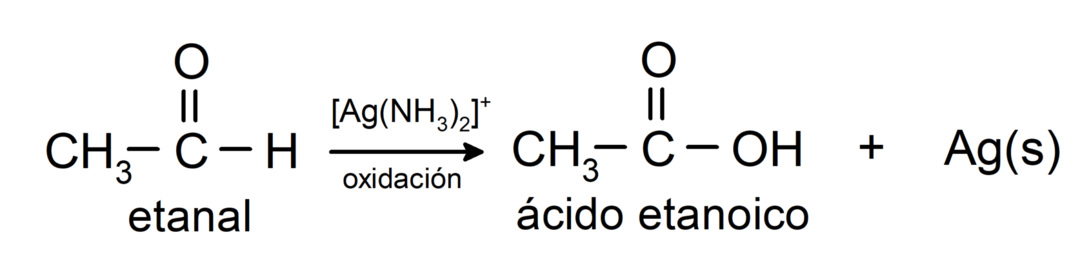
- Oxidáciou Benediktovým činidlom (alkalický roztok síranu meďnatého) etanálu vzniká kyselina etanová a oxid meďný.
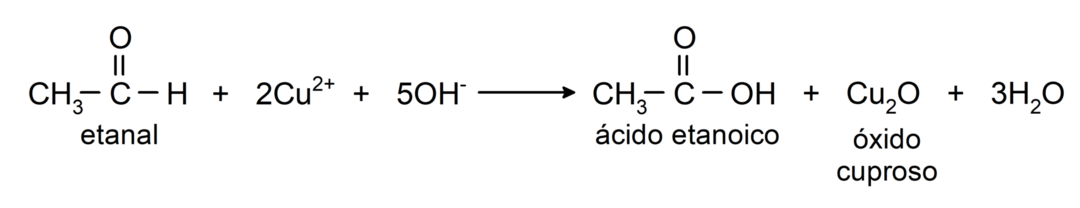
Podstupujú nukleofilné adičné reakcieto znamená pridanie nukleofilu ku karbonylovej skupine. Napríklad:
- Pridanie kyseliny kyanovodíkovej za vzniku kyanohydrínov alebo kyanohydrínov.
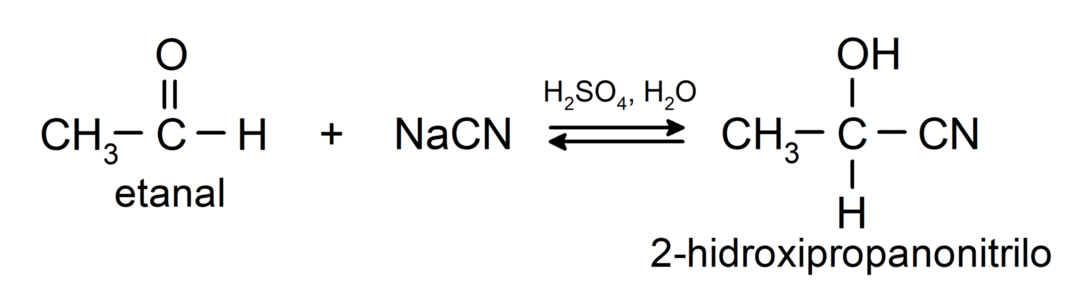
- V prítomnosti bezvodých kyselín sa ku karbonylovej skupine aldehydov pridávajú alkoholy za vzniku acetálov a poloacetálov.
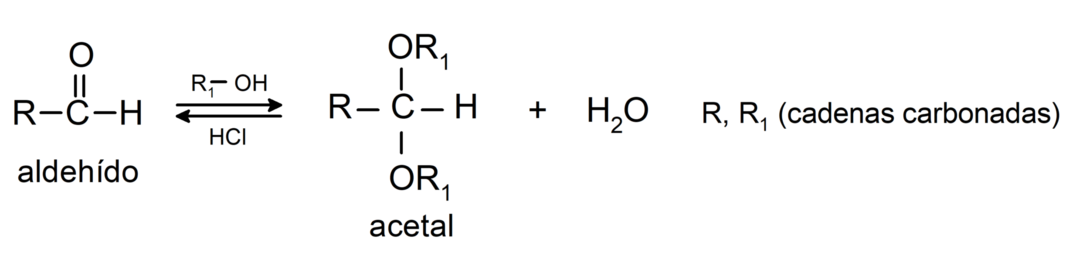
Podstupujú aldolové kondenzačné reakcie. Pri týchto reakciách dochádza k spojeniu dvoch aldehydov v prítomnosti hydroxidu sodného (NaOH) a chemická zlúčenina výsledný sa nazýva aldol. Napríklad:
- Kondenzačná reakcia etanálu v prítomnosti zriedeného NaOH.
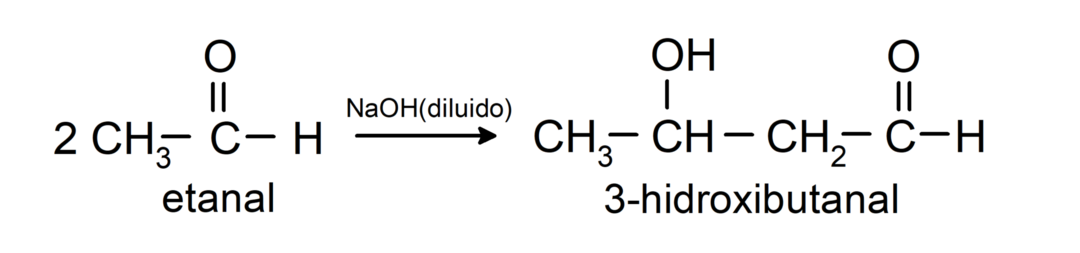
Redukujú sa na primárne alkoholy. Aldehydy možno redukovať na primárne alkoholy katalytickou hydrogenáciou alebo redukciou borohydridom sodným (NaBH).4) a lítiumalumíniumhydrid (LiAlH4).
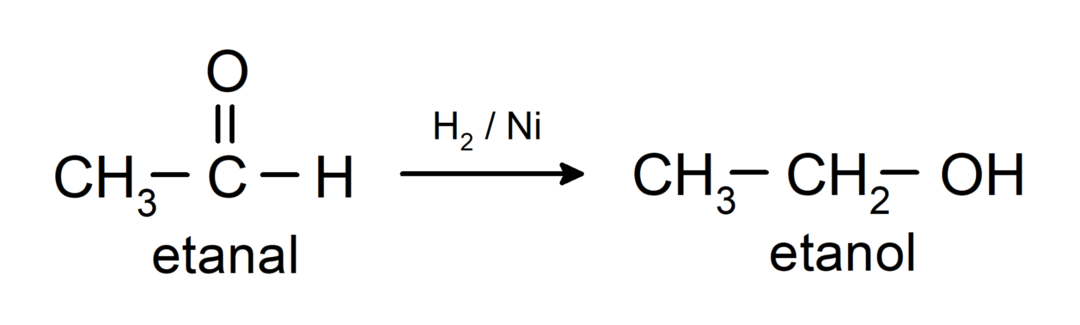
Chemické vlastnosti ketónov
Medzi chemické vlastnosti ketónov môžeme nájsť:
Podstupujú nukleofilné adičné reakcie. Napríklad:
- Pridanie kyseliny kyanovodíkovej za vzniku kyanohydrínov alebo kyanohydrínov.
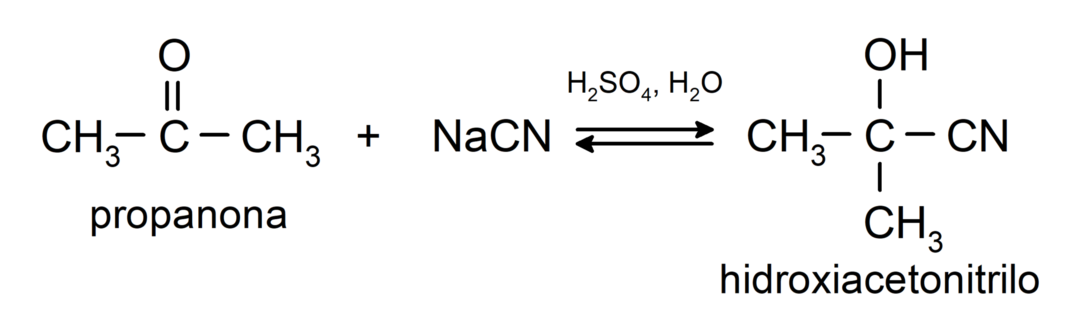
Pridávajú alkohol (v prítomnosti bezvodých kyselín) na karbonylovú skupinu ketónov za vzniku ketálov a hemiketálov. Napríklad:
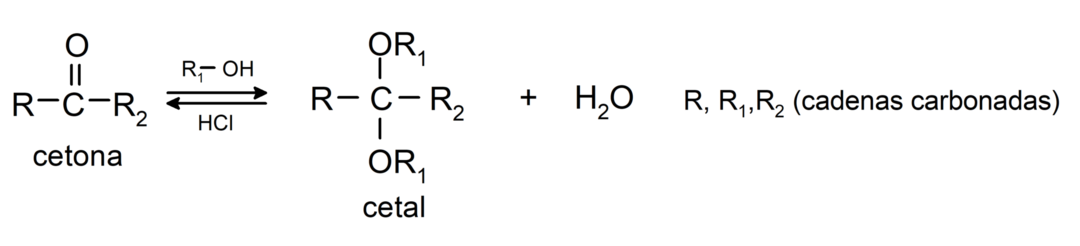
Podstupujú halogenačné reakcie. Ketóny, ktoré majú alfa vodík (α) reagovať nahradením tohto vodíka halogénmi (chlór (Cl), bróm (Br), jód (I), fluór (F)) v prítomnosti kyslých alebo zásaditých katalyzátorov. Substitúcia sa vyskytuje takmer výlučne v uhlíku α, teda uhlík, ktorý sa naviazal na vodík α. Napríklad:
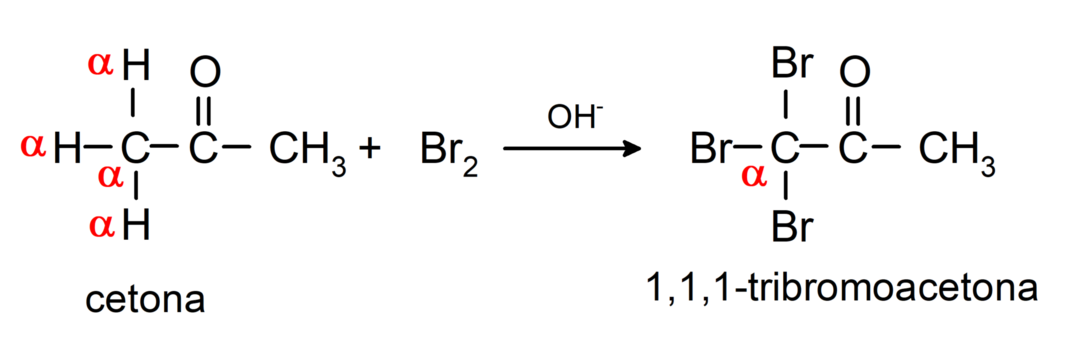
Redukujú sa na sekundárne alkoholy katalytickou hydrogenáciou alebo redukciou borohydridom sodným (NaBH4) a lítiumalumíniumhydrid (LiAlH4). Napríklad:
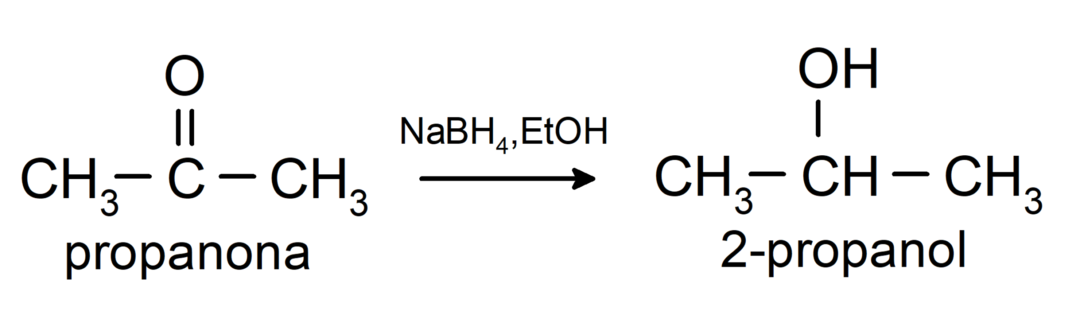
Ketóny nie sú oxidované Tollensovým a Benediktovým činidlom.
Nomenklatúra aldehydov
Podľa pravidiel stanovených Medzinárodnou úniou čistej a aplikovanej chémie (IUPAC), Aldehydy sú pomenované pomocou predpôn, ktoré označujú počet uhlíkov v reťazci. sýtené oxidom uhličitým. Nie je potrebné špecifikovať polohu karbonylovej skupiny, pretože je vždy v polohe jedna na jednom konci molekuly. Okrem toho je na konci názvu aldehydu napísaná prípona -al. Napríklad:
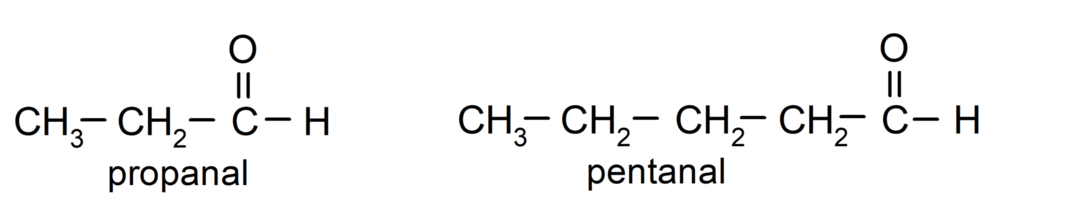
Ak je aldehyd tvorený niekoľkými uhlíkovými reťazcami, to znamená, že má vetvy, ako hlavný reťazec sa vyberie uhlíkový reťazec s najväčším počtom atómov uhlíka. Ostatné reťazce sú pomenované ako substitučné skupiny a poloha každého substituenta je zvolená tak, aby zaberal v reťazci čo najmenší počet. Okrem toho sa atómy uhlíka začínajú počítať od konca, ktorý má karbonylovú skupinu. Napríklad:
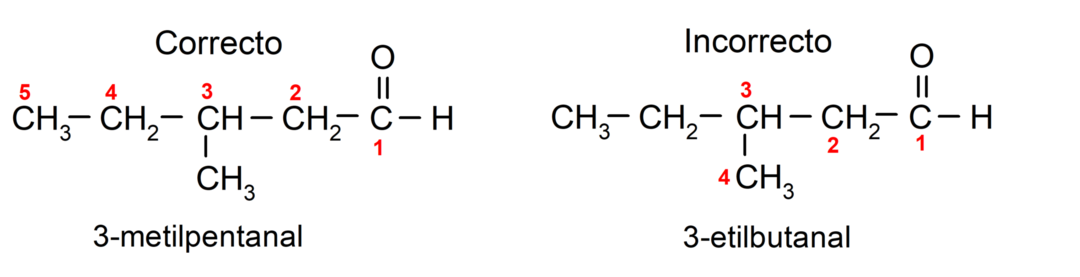
Aldehydy, ktoré majú dve karbonylové skupiny, sú pomenované pomocou prípony -dial. Napríklad:
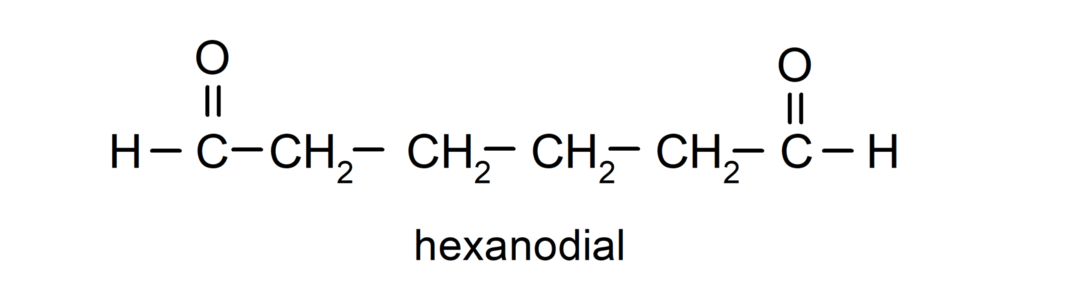
Ketónová nomenklatúra
Podľa Medzinárodnej únie čistej a aplikovanej chémie (IUPAC) sú ketóny pomenované pomocou predpôn, ktoré označujú počet uhlíkov v uhlíkovom reťazci.
Na druhej strane sa názov acetónu píše pomocou prípony -one, pred ktorou je číslo, ktoré označuje polohu karbonylovej skupiny v uhlíkovom reťazci. Umiestnenie karbonylovej skupiny by malo byť zvolené tak, aby zodpovedalo najnižšiemu možnému číslovaniu. Napríklad:
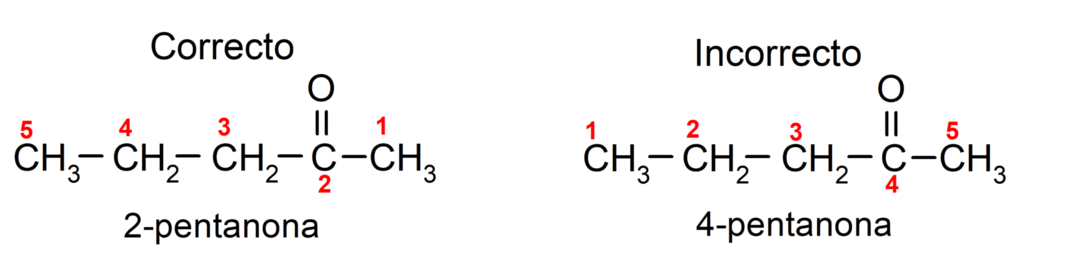
Ak chcete pomenovať ketón, ktorý sa skladá z niekoľkých uhlíkových reťazcov, to znamená s vetvami, vyberieme ako hlavný reťazec uhlíkový reťazec s najväčším počtom atómov uhlíka, ktorý obsahuje skupinu karbonyl. Zvyšné reťazce sú pomenované ako substitučné skupiny. Napríklad:
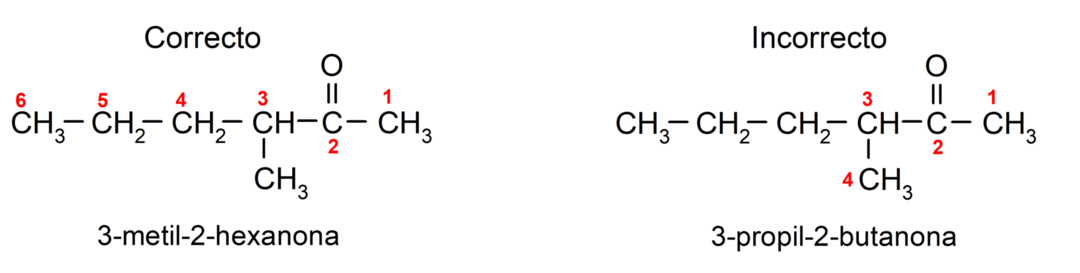
Existujú ketóny, ktoré majú dve karbonylové skupiny, nazývajú sa dióny. Napríklad:
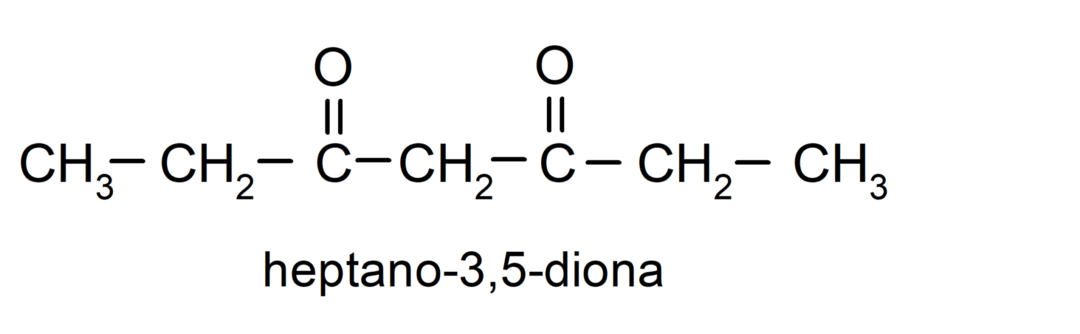
Príklady aldehydov
- metán (formaldehyd)
- etanol (acetaldehyd)
- propanal (propaldehyd)
- butanal
- pentanal
- hexanal
- 3-brómcyklopentánkarbaldehyd
- cyklohexánkarbaldehyd
- benzaldehyd
- 4,4-dimetylpentanal
- 2-hydroxybutanal
- 2-hydroxy-2-metylbutanal
- 2,3-dimetylpentanal
- pentanedial
- 4-hydroxy-3-metoxybenzaldehyd
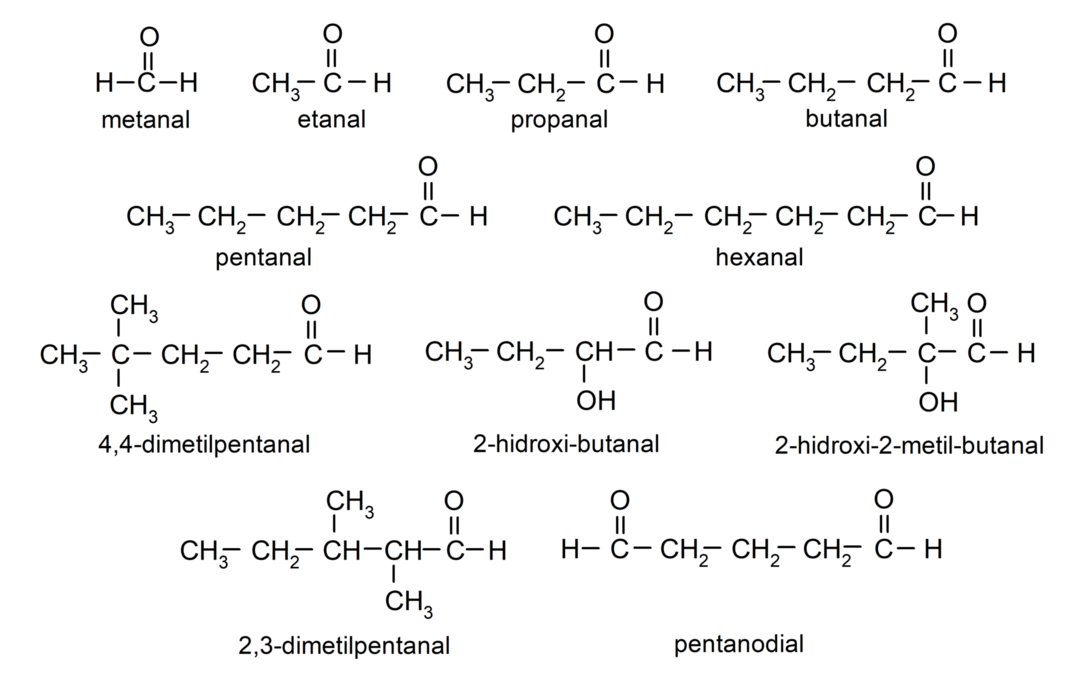
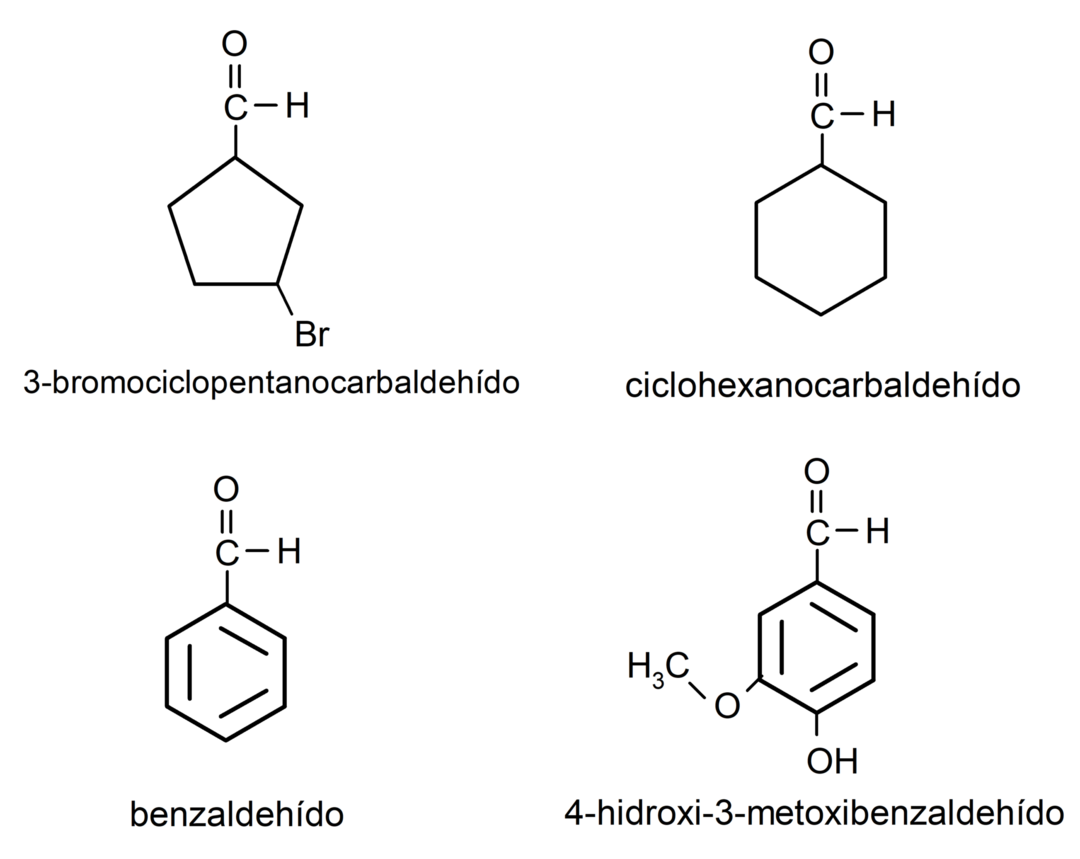
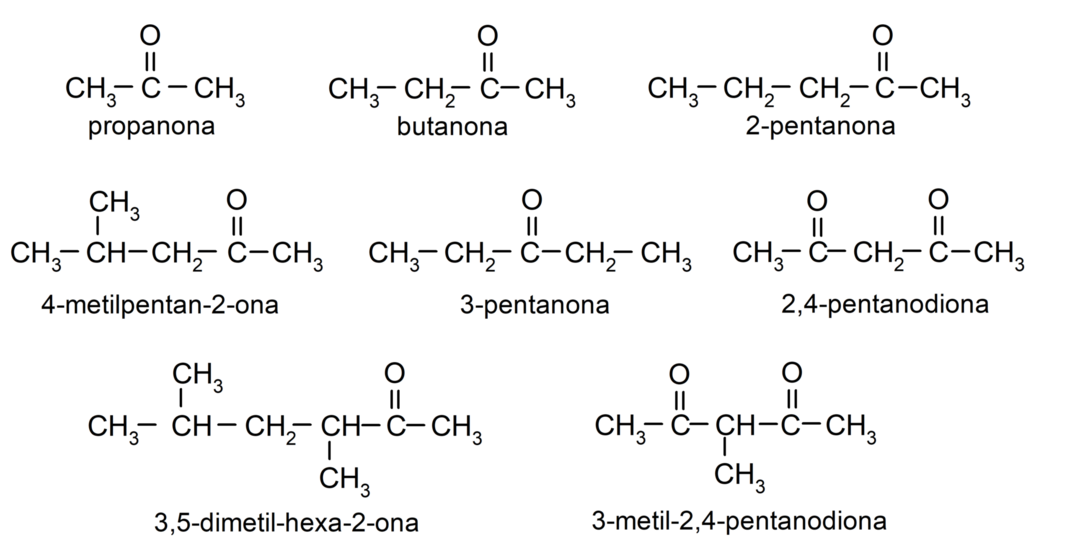
Príklady ketónov
- propanón (acetón)
- butanón
- 2-pentanón
- 4-metylpentán-2-ón
- 3-metylcyklohexanón
- cyklohexylmetylketón
- 3,4-dimetylhexán-2-ón
- etylfenylketón
- 2,4-pentándión
- cyklohexanón
- 3-pentanón
- 3-metyl-2,4-pentándión
- 1-fenylpropanón
- cyklopentanón
- difenylketón
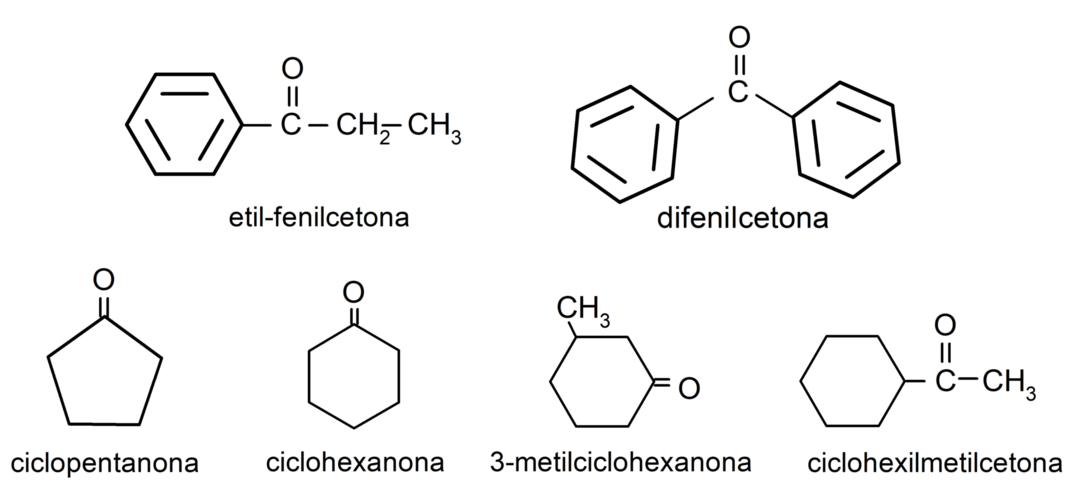
Využitie aldehydov v každodennom živote
Niektoré použitia aldehydov sú:
- Používajú sa na výrobu rozpúšťadiel, farieb, parfumov, živíc a esencií.
- Používajú sa ako konzervačné látky v kozmetických výrobkoch, biologických vzorkách a mŕtvolách. Na tieto účely sa najviac používa formaldehyd.
- Vyrábajú sa z nich plasty, ktoré umožňujú výmenu kovových dielov v automobilovom priemysle.
- Používajú sa ako príchute do niektorých potravín.
- Používajú sa ako dezinfekčné prostriedky.
- Používali sa na výrobu niektorých výbušnín, ako napríklad pentaerytritol tetranitrát (TNPE).
Použitie ketónov v každodennom živote
Niektoré použitia ketónov sú:
- Používajú sa pri výrobe rozpúšťadiel. Najmä acetón je široko používaný na odstraňovanie farieb a lakov.
- Používajú sa pri výrobe niektorých gúm a mazív.
- Používajú sa na výrobu farieb, lakov a lakov.
- Používajú sa na výrobu liekov a kozmetiky.
Aldehydová a ketónová toxicita
- Aldehydy. Kontakt s aldehydmi spôsobuje podráždenie pokožky, očí a dýchacích ciest. Okrem toho sa expozícia aldehydom spája s chorobami, ako je rakovina, kontaktná dermatitída a pečeňové a neurodegeneratívne ochorenia. Napríklad formaldehyd považuje WHO (Svetová zdravotnícka organizácia) za karcinogénnu zlúčeninu.
- ketóny. Opakovaná expozícia ketónom môže spôsobiť poškodenie centrálneho nervového systému. To môže viesť k strate pamäti, slabosti, bolestiam svalov a kŕčom. Navyše, ak sa pokožka dostane do kontaktu s ketónmi, dochádza k suchu a praskaniu. Na druhej strane, ak sú ketóny vdýchnuté, dochádza k podráždeniu dýchacích ciest a kašľu.
Referencie
- Llorens Molina, JA. (2018). “Aldehydy a ketóny: Niekoľko príkladov.” http://hdl.handle.net/
- Gabriel Pinto Cañón, Manuela Martín Sánchez, José María Hernández Hernández, María Teresa Martín Sánchez (2015) “Tollensovo činidlo: od identifikácie aldehydov po ich použitie v nanotechnológii. Historické aspekty a didaktické aplikácie.„Zv. 111 č. 3. Kráľovská španielska spoločnosť pre chémiu.
- William Bauer, Jr. (2000) «Kyselina metakrylová a deriváty» v Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. DOI: 10.1002/14356007.a16_441.
- „Odhaľujú nový mechanizmus toxicity v skupine karcinogénnych zlúčenín pochádzajúcich zo stravy a životného prostredia“ (2022) In: www.conicet.gov.ar Dostupné v: https://www.conicet.gov.ar/ Prístup: 20. júna 2023.
Nasledujte s:
- Alkoholy
- Cukry
- Alkány