20 príkladov amínov
Príklady / / November 06, 2023
The amíny sú organické chemické zlúčeniny deriváty amoniaku (NH3), kde bol aspoň jeden z vodíkov amoniaku nahradený alkylovou alebo arylovou skupinou, čo vedie k vytvoreniu aminoskupiny (-NH2-NH-, -N=). Napríklad:metylamín, etylamín a propylamín.

Alkylová skupina je substituent, ktorý vzniká, keď sa vodík odstráni z nasýteného uhľovodíka. Týmto spôsobom sa uhlík, z ktorého bol tento vodík oddelený, môže viazať na iný atóm. Napríklad: metyl (CH3 -) a etyl (CH3 – CH2 -).
Arylová skupina je substituent odvodený od aromatického kruhu, ako je benzén. Napríklad: fenyl (C6h5 -)
- Pozri tiež: Amidy
Druhy amínov
Amíny možno klasifikovať podľa počtu atómov vodíka viazaných na dusík, ktoré boli nahradené alkylovými alebo arylovými funkčnými skupinami.
Podľa tohto kritéria existujú:
- primárne amíny. Vznikajú vtedy, keď je len jeden z atómov vodíka amoniaku nahradený alkylovou alebo arylovou skupinou. Napríklad: etylamín a 1-pentylamín.
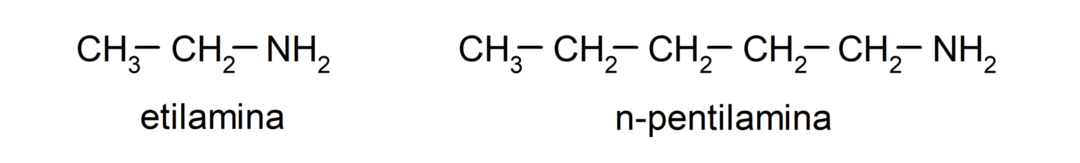
- sekundárne amíny. Vznikajú vtedy, keď sú dva z vodíkových atómov amoniaku nahradené alkylovou alebo arylovou skupinou. Napríklad: dietylamín a etylmetylamín.
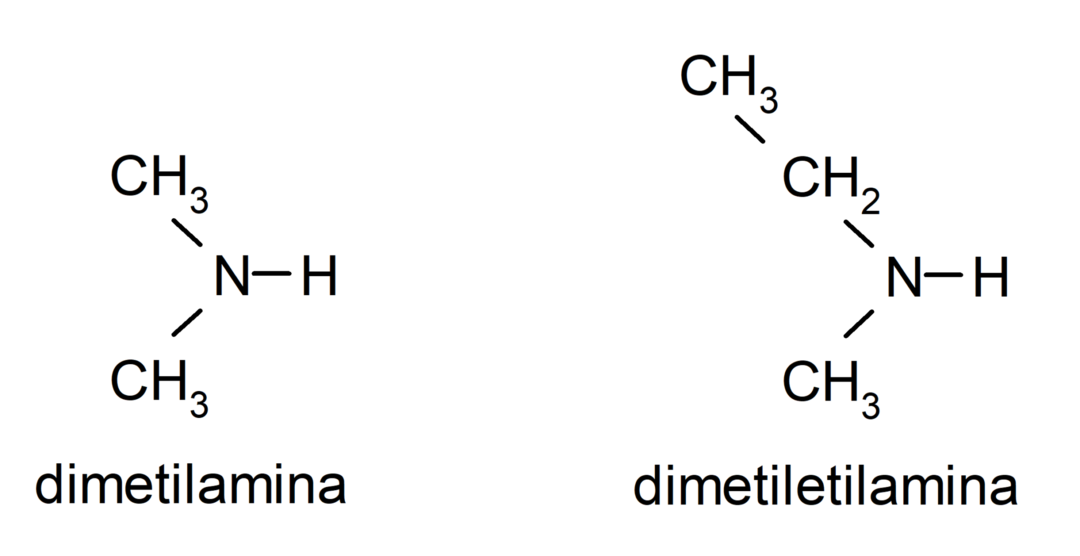
- Terciárne amíny. Vznikajú, keď sú tri atómy vodíka amoniaku nahradené alkylovou alebo arylovou skupinou. Napríklad: trimetylamín a dimetyletylamín.
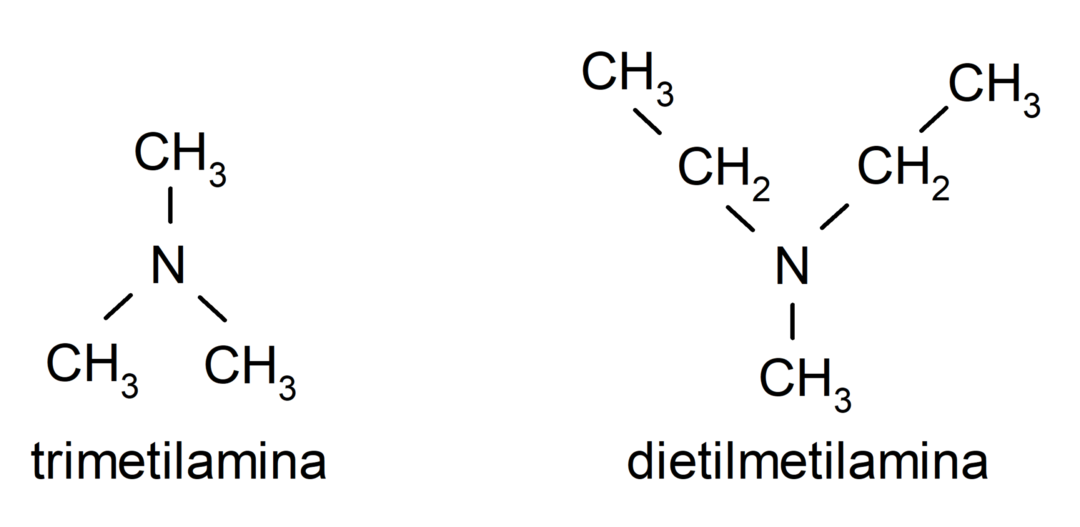
Amíny sú tiež klasifikované na základe typu skupiny, ktorá je pripojená k dusíku. Podľa tohto kritéria existujú:
- Alifatické amíny. Majú alkylové substituenty. Napríklad: butylamín a dietylamín.

- aromatické amíny. Majú arylové substituenty. Napríklad: fenylamín (anilín) a difenylamín.
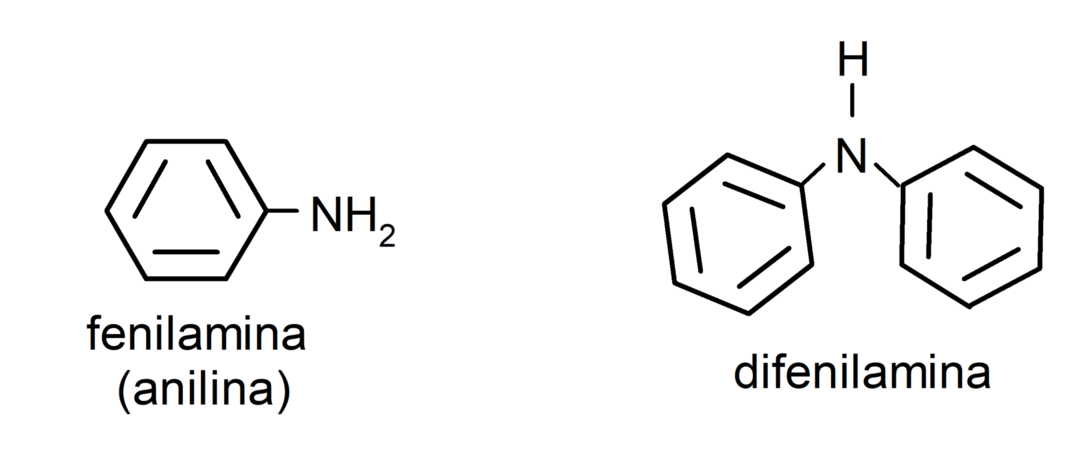
Názvoslovie amínov
Podľa IUPAC (International Union of Pure and Applied Chemistry) sú amíny pomenované podľa nasledujúcich pravidiel:
Pre najjednoduchšie amíny je pomenovaný každý zo substituentov vodíkových skupín viazaných na amoniakový dusík. Potom sa slovo „amín“ umiestni na koniec mena.
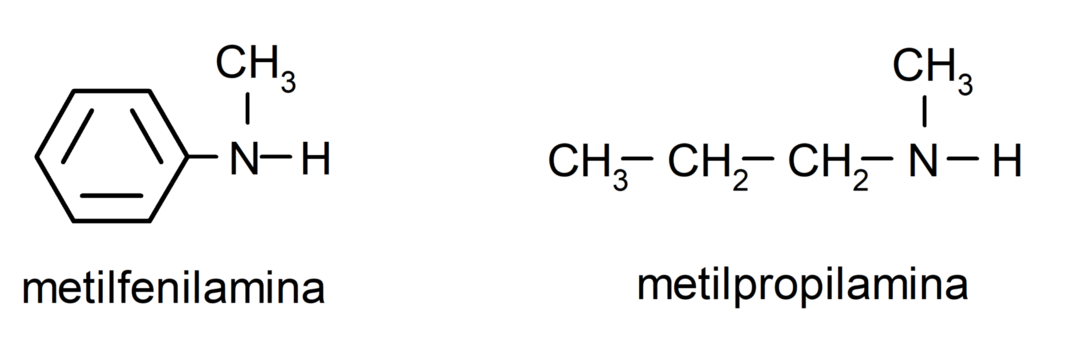
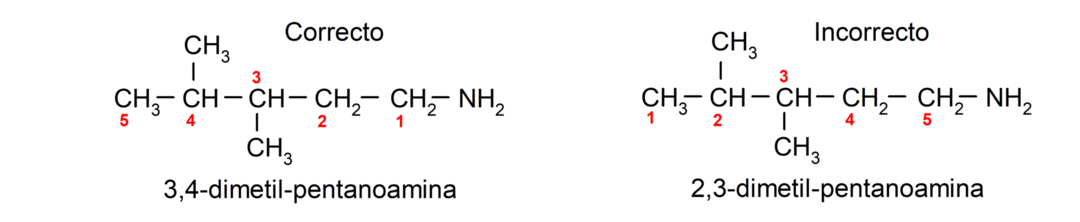
Pre amíny, ktoré obsahujú niekoľko uhlíkových reťazcov (ktoré majú zase iné substituenty), je uhlíkový reťazec, ktorý obsahuje aminoskupinu, vybraný ako hlavný. Ďalej je poloha aminoskupiny zvolená tak, aby zaujímala najmenšiu polohu v uhlíkovom reťazci a v Na základe tejto polohy sa volia aj substituenty tak, aby zaujímali čo najmenšiu polohu v reťaz.
Nakoniec sú pomenované pomocou názvu zodpovedajúceho alkánu, alkénu alebo alkínu pre hlavný reťazec a je umiestnená amínová prípona.
Ak uhlíkový reťazec obsahuje niekoľko aminoskupín, vyberajú sa v polohe, ktorú zaberajú, v najmenšej kombinácii číslovania ich polôh. Okrem toho je uvedený názov zodpovedajúceho alkánu, alkénu alebo alkínu, za ktorým nasleduje výraz, ktorý označuje počet aminoskupín, za ktorým nasleduje prípona „amín“.

Fyzikálne vlastnosti amínov
Fyzikálne vlastnosti amínov do značnej miery závisia od toho, koľko vodíkov pripojených k dusíku bolo substituovaných a akým typom substituentov boli substituované.
- Rozpustnosť. Vo všeobecnosti sú amíny rozpustnejšie vo vode ako zodpovedajúce nasýtené uhľovodíky. Okrem toho sú amíny s dlhými uhlíkovými reťazcami menej rozpustné vo vode ako amíny s krátkymi uhlíkovými reťazcami. Na druhej strane aromatické amíny nie sú rozpustné vo vode.
- Bod varu. Teplota varu amínov je vyššia ako u alkánov s rovnakým počtom atómov uhlíka.
- Vôňa. Väčšina amínov má nepríjemný zápach. Napríklad putrescín zapácha ako hnijúce mäso a trimetylamín ako hnijúca ryba.
Chemické vlastnosti amínov
Niektoré chemické vlastnosti amínov sú:
- Sú to základné chemické zlúčeniny, to znamená, že podstupujú reakcie, pri ktorých prijímajú protóny podľa Brønsted-Lowryho teórie. Napríklad:
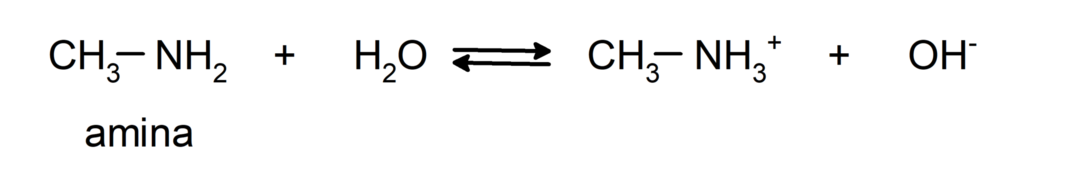
- Predstavujú neutralizačné reakcie s kyselinami, v ktorých vznikajú amínové soli. Napríklad:

Príklady amínov
- metylamín
- etylamín
- propylamín
- dimetylamín
- etylmetylamín
- fenylamín (anilín)
- difenylamín
- metylpropylamín
- bután-1,4-diamín
- spermín
- kadaverín
- 3,5-dimetylanilín
- metylanilín
- amfetamín
- piperazín


Biologická funkcia amínov
Amíny sú prítomné v mnohých živé bytosti a vykonávať rôzne funkcie. Niektoré amíny, ako je adrenalín, norepinefrín, serotonín a dopamín, sú neurotransmitery.
Aminoskupina je jednou z funkčných skupín, ktoré tvoria aminokyseliny, ktoré sú základnými jednotkami bielkoviny. Okrem toho dusíkaté bázy, ktoré tvoria DNA a RNA, obsahujú aminoskupiny.
Použitie amínov
Niektoré použitia amínov sú:
- Používajú sa na výrobu agrochemických a farmaceutických zlúčenín.
- Používajú sa ako katalyzátory pri výrobe polyuretánov.
- Vďaka svojmu tlmiacemu účinku sa používajú na inhibíciu korózie vo vodnom prostredí.
- Používajú sa na čistenie plynov v elektrárňach a rafinériách.
- Používajú sa na výrobu čistiacich prostriedkov.
- Používajú sa na výrobu produktov osobnej starostlivosti, pretože zlepšujú penivosť v mydlách a šampónoch.
Toxicita amínov
Vdychovanie amínov vo vysokých koncentráciách spôsobuje otravu, ktorá následne spôsobuje zvýšený krvný tlak a kŕče. Ďalej kontakt s alifatickými amínmi v plynné skupenstvo spôsobuje podráždenie očí a dýchacích ciest. Niekoľko amínov spôsobuje pri kontakte s pokožkou popáleniny.
Aromatické amíny sú veľmi toxické, ale keďže sú oveľa menej prchavé ako alifatické amíny, kontakt s nimi sa dá lepšie kontrolovať.
Referencie
- Pérez, C. R. C. a Jiménez-Colmenero, F. (2010). Biogénne amíny: Toxikologický význam. Electron. J. Biomed., 3, 58-60.
- Fernández García, M., & Álvarez González, M. Á. (2005). Biogénne amíny v potravinách.
Nasledujte s:
- Alkoholy
- Aldehydy
- Etylalkohol
- organická chémia


