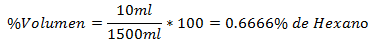Príklad koncentrácie: molarita, molárnosť, normálnosť a percento
Chémia / / July 04, 2021
The Koncentrácia je definované ako Množstvo alebo podiel určitej látky prítomnej v roztoku. Riešením je a homogénna zmes (viditeľná jedna fáza), ktoré môžu byť pevné, kvapalné alebo plynné, takže Koncentrácia môže byť vyjadrená rôznymi spôsobmi.
Je potrebné definovať, že Riešenie obsahuje dve hlavné zložky: Rozpustená látka a rozpúšťadloKoncentrácia sa všeobecne zameriava na vyjadrenie toho, koľko rozpustenej látky je zmiešané v celom riešení. Avšak Koncentrácia môže vyjadrovať množstvo alebo podiel ktoréhokoľvek z nich.
Vyjadrenie koncentrácie
V chémii možno množstvo látky prítomnej v roztoku vyjadriť niekoľkými rôznymi spôsobmi: Molarita, molárnosť, normálnosť, hmotnostné percento, objemové percento.
Z týchto piatich jednotiek je možné všetky použiť na tuhé, kvapalné a plynné roztoky. Ale napríklad Molality je pre Solid Solutions najpoužívanejší.
Príklady jasnosti
The Molarita označuje, koľko mólov látky je v každom litri kompletného roztoku. Je to najbežnejšie používaná jednotka v chémii pre kvapalné roztoky pri objemovej analýze. Je to označené písmenom „M“.
Ak poznajú gramy rozpustenej látky, sú vydelené molekulovou hmotnosťou rozpustenej látky. Tak sa získajú móly rozpustenej látky prítomné v roztoku.
Potom sa móly rozpustenej látky rozdelia na litre roztoku a získajú sa tak jednotky molarity: Móly rozpustenej látky / liter disolúcie.
1. - Na roztok 0,5 litra hydroxidu horečnatého [Mg (OH)2], a ak je molekulová hmotnosť hydroxidu horečnatého 58 g / mol. Máte ho 36 gramov.
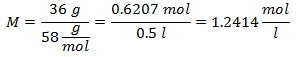
2. - Na 1 liter roztoku hydroxidu vápenatého [Ca (OH)2], a ak je molekulová hmotnosť hydroxidu vápenatého 74 g / mol. Máte ho 42 gramov.

3. - Pre roztok 3 litrov chloridu sodného (NaCl) a ak je molekulová hmotnosť chloridu sodného 58 g / mol. Máte ho 28 gramov.
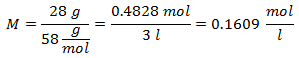
4. - Na roztok 5 litrov chloridu vápenatého (CaCl2), a ak je molekulová hmotnosť chloridu vápenatého 110 g / mol. Máte ho 13 gramov.
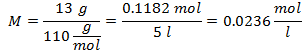
5. - Na roztok 10 litrov síranu sodného (Na2SW4), a ak je molekulová hmotnosť síranu sodného 142 g / mol. Máte ho 96 gramov.
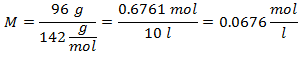
Príklady Molality
The Molalita označuje, koľko mólov rozpustenej látky je na 1000 gramov rozpúšťadla v Riešení. Je to najbežnejšie používaná jednotka v chémii pre tuhé roztoky. Je to označené písmenom „m“.
Ak poznajú gramy rozpustenej látky, sú vydelené molekulovou hmotnosťou rozpustenej látky. Tak sa získajú móly rozpustenej látky prítomné v roztoku.
Potom sa krtky rozpustenej látky upravia na každých 1 000 gramov roztoku, ktoré sa stanovia ako základ výpočtu, a tým sa získajú jednotky molality: Moly rozpustenej látky / 1 000 g Solventný
1. - Na roztok s 1 000 g minerálneho rozpúšťadla a 36 gramami hydroxidu horečnatého [Mg (OH)2], a ak je molekulová hmotnosť hydroxidu horečnatého 58 g / mol.

2. - Na roztok 2 000 g minerálneho rozpúšťadla a 42 gramov hydroxidu vápenatého [Ca (OH)2], a ak je molekulová hmotnosť hydroxidu vápenatého 74 g / mol.
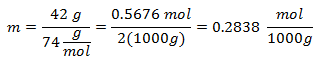
3. - Pre roztok 3 000 g minerálneho rozpúšťadla a 28 gramov chloridu sodného (NaCl) a ak je molekulová hmotnosť chloridu sodného 58 g / mol.
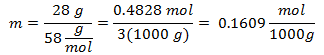
4. - Na roztok 5 000 g minerálneho rozpúšťadla a 13 gramov chloridu vápenatého (CaCl2), a ak je molekulová hmotnosť chloridu vápenatého 110 g / mol.
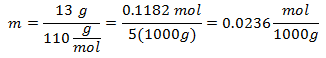
5. - Na roztok 10 000 g minerálneho rozpúšťadla a 96 gramov síranu sodného (Na2SW4), a ak je molekulová hmotnosť síranu sodného 142 g / mol.
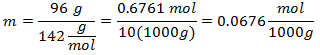
S množstvami rozpúšťadiel sa zaobchádza ako s násobkami 1 000 g, aby sa ponechalo 1 000 gramov ako referencia a nezahrnuli ich, čo má vplyv na výpočet.
Príklady normality
The Normálnosť označuje počet ekvivalentov látok v každom litri úplného roztoku. Normálnosť je ďalšou jednotkou, ktorá sa v chémii pre kvapalné roztoky najbežnejšie používa pri objemovej analýze. Je to označené písmenom „N“.
Ekvivalent je jednotka, ktorá je výsledkom vydelenia gramov rozpustenej látky (g) a jej ekvivalentnej hmotnosti (malá). Ekvivalentná hmotnosť (Peq) je výsledkom delenia molekulovej hmotnosti (PM) aktívnou Valenciou (*), ktorú je ľahšie sledovať v prípade kyselín a zásad. Napríklad aktívna Valencia kyseliny chlorovodíkovej (HCl) je 1; aktívna Valencia hydroxidu vápenatého [Ca (OH)2] je 2, kvôli vodíkovým (H +) a hydroxylovým (OH-) iónom, ktoré každý z nich predstavuje.
Potom sa ekvivalenty rozpustených látok vydelia litrami riešenia, a tak sa získajú jednotky normality: solute ekvivalenty / liter roztoku.
1. - Na roztok 0,5 litra hydroxidu horečnatého [Mg (OH)2], a ak je molekulová hmotnosť hydroxidu horečnatého 58 g / mol. Máte ho 36 gramov.
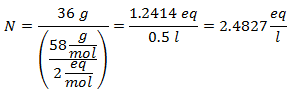
2. - Na 1 liter roztoku hydroxidu vápenatého [Ca (OH)2], a ak je molekulová hmotnosť hydroxidu vápenatého 74 g / mol. Máte ho 42 gramov.
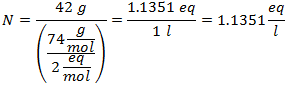
3. - Pre roztok 3 litrov chloridu sodného (NaCl) a ak je molekulová hmotnosť chloridu sodného 58 g / mol. Máte ho 28 gramov.
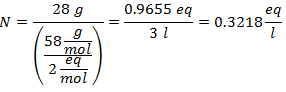
4. - Na roztok 5 litrov chloridu vápenatého (CaCl2), a ak je molekulová hmotnosť chloridu vápenatého 110 g / mol. Máte ho 13 gramov.
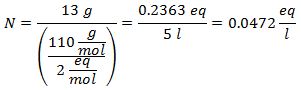
5. - Na roztok 10 litrov síranu sodného (Na2SW4), a ak je molekulová hmotnosť síranu sodného 142 g / mol. Máte ho 96 gramov.
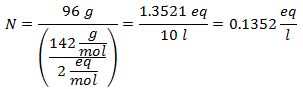
Príklady hmotnostných percent
The Percento hmotnosti je vyjadrením koncentrácie, ktorá je výsledkom rozdelenia Množstvo v gramoch rozpustenej látky medzi gramami celkového roztoku. Získaním desatinného množstva sa vynásobí 100 a vyjadrí sa symbolom „%“. Táto jednotka sa všeobecne používa na meranie koncentrácií v tuhých alebo zrnitých zmesiach.
1. - Zmes 1 300 g celkom obsahuje 13 g uhličitanu vápenatého. Percento hmotnosti je:
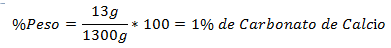
2. - Zmes 100 g celkovo obsahuje 26 g cukru. Percento hmotnosti je:
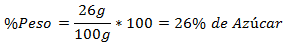
3. - Celková zmes 250 g obsahuje 60 g chloridu sodného. Percento hmotnosti je:
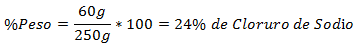
4.- Zmes 800 g celkovo obsahuje 150 g hydroxidu vápenatého. Percento hmotnosti je:
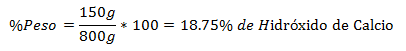
5. - Zmes celkom 1 500 g obsahuje 10 g hydrogenuhličitanu sodného. Percento hmotnosti je:
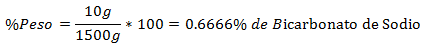
Príklady objemového percenta
The Percento v objeme je vyjadrením koncentrácie, ktorá je výsledkom rozdelenia množstvo v jednotkách Objemu rozpustenej látky vydelené Objemom celkového roztoku. Získaním desatinného množstva sa vynásobí 100 a vyjadrí sa symbolom „%“. Táto jednotka sa všeobecne používa na meranie koncentrácií v zmesiach kvapalných alebo plynných zložiek.
1.- Zmes 1300 ml obsahuje 130 ml etanolu. Percento objemu je:
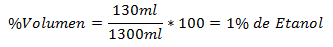
2.- Zmes 100 ml obsahuje 26 ml glycerínu. Percento objemu je:
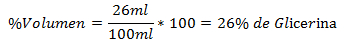
3.- Celková zmes 250 ml obsahuje 60 ml etyléteru. Percento objemu je:
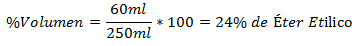
4.- Zmes 800 ml obsahuje 150 ml glykolu. Percento objemu je:
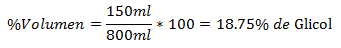
5.- Zmes 1 500 ml obsahuje 10 ml hexánu. Percento objemu je: