50 Primeri rešitev
Miscellanea / / July 04, 2021
The rešitve so ena od vrst mešanice ki obstajajo. Komponente, ki tvorijo raztopino, ne reagirajo kemično, čeprav je fizikalne lastnosti teh komponent mogoče spremeniti, ko postanejo del raztopine. Na primer: dim, amalgam, kava z mlekom.
Da bi bila zmes rešitev, mora biti homogena Y. uniformo, to pomeni, da mešanih komponent ni mogoče razlikovati s prostim očesom in da je poleg tega delež med topljeno snovjo (snovjo, ki se pojavlja v manjši količini) in topilo (snov, ki se pojavi v večji količini) ostane približno nespremenjena v katerem koli volumnu, ki ga vzamemo iz raztopine. Delež topljene snovi v raztopini ali topilu je tako imenovan "koncentracija" in običajno lahko isto raztopino pripravimo z uporabo različnih koncentracij topljene snovi.
Raztopine lahko nastanejo med snovmi, ki so pred mešanjem v kateri koli od različnih agregacijskih stanj. Rešitve obstajajo v skoraj vseh agregatnih stanjih. Na splošno je agregacijsko stanje raztopine določeno z agregacijskim stanjem topila. Na primer:
Običajno je za prisotnost molekul raztopljene snovi v topilu spremeni lastnosti samega topila. Na primer, tališče in vrelišče dveh spojin se spremenita, ko se te spojine pomešajo, prav tako pa tudi njihova sestava. gostote in barv.
Francoski znanstvenik Roult preučeval to vedenje komponent v rešitvah in predlagal tudi njegov glavni zakon (Roultov zakon), ki navaja, da je parcialni parni tlak vsake komponente v parni mešanici, ki obdaja idealno raztopino iz tekočine enak je parcialnemu tlaku vsake čiste komponente, pomnoženemu z molskim deležem v raztopini. Za idealno rešitev se šteje tista raztopina, pri kateri so kemične vrste zelo podobne, zato ni upoštevano nobeno spreminjanje energije medsebojnih interakcij. Temeljna enačba Roultovega zakona je:
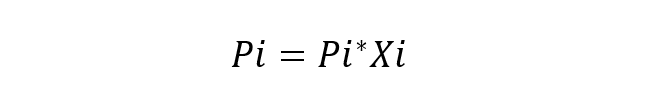
Kje:
- Pi je delni tlak komponente jaz v plinasti zmesi, ki obdaja raztopino.
- Pi * je tlak komponente jaz
- Xi je molski delež komponente jaz v raztapljanju.
Očitno so ljudje stalno v stiku z rešitvami. The zrak je raztapljanje elementov v plinastem stanju: večinsko sestavo poda dušik (78%), ostalo pa zaseda 21% kisik in 1% drugih komponent, čeprav se lahko ti deleži nekoliko razlikujejo.
Primeri rešitev
Naslednji seznam vključuje štirideset primerov raztopin, ki poudarjajo agregacijsko stanje, v katerem je vsaka od njih topljena v določenem topilu.
- Zrak (plin v plinu). Sestava plinov, kjer je dušika največ.
- Dim (trdna snov v plinu). Zrak stara zaradi videza dima iz ognja. Je raztopina, v kateri zrak deluje kot topilo.
- Zlitine med kovinami (trdno v trdnem). Duralumin je zlitina, sestavljena iz aluminija, bakra, mangana, magnezija in silicija.
- Prah iz atmosferskega zraka (trdna snov v plinu). Prisotnost trdnih snovi (razgrajenih skoraj do nedeljive enote, vendar na koncu trdnih snovi) v plinu je primer raztapljanja v tem smislu.
- Jeklo (trdno v trdnem). Zlitina med železom in ogljikom, z veliko večjim deležem prvega.
- Gazirane pijače (plin v tekočini). Gazirane pijače raztapljajo pline v tekočini.
- Amalgam (tekočina v trdnem). So zlitine živega srebra, raztopljene v nekaterih kovin kot zlato ali srebro.
- Rafinirano zemeljsko olje (tekočina v tekočini). Kombinacija elementov, ki ga sestavljajo (večina je ogljik), povzroči raztapljanje tekočin.
- Butan v zraku (plin v plinu). Butan je a kemična spojina plinast, ki ga lahko shranimo v epruvetah, pripravljen za uporabo kot gorivo.
- Kisik v oceanski vodi (plin v tekočini). Oksigenacija morske vode omogoča razvoj vodnega življenja.
- Pijače z vsebnostjo alkohola (tekočina v tekočini). Ljudje jih zelo uživajo na praznovanjih. Običajno so raztopine etanola in sadnih sokov v nadzorovanih koncentracijah alkohol.
- Kava z mlekom (tekočina v tekočini). Tekočina z večjo vsebnostjo prejme malo od druge, kar pomeni preoblikovanje njene barve in okusa.
- Smog (plini v pline). Vnos plinov, ki niso značilni za ozračje, povzroči preoblikovanje zraka, ki negativno vpliva na družbe, ki jo dihajo: bolj koncentrirana, bolj škodljiva bo.
- Sol v vodi (trdno v tekočini). Široko uporablja za kuhanje.
- Kri (tekočina v tekočini). Večina komponent je plazma (tekočina), v njej pa se pojavijo drugi elementi, med katerimi izstopajo rdeče krvne celice.
- Amoniak v vodi (tekočina v tekočini). Ta rešitev (ki jo lahko naredimo tudi iz plina v tekočino) deluje v mnogih čistilnih napravah.
- Zrak s sledovi vlage (tekočina v plinu). Zaradi povečane količine je v zraku prisotna vodna para temperatura.
- Sokovi v prahu (trdno v tekočini). Prašek se raztopi v vodi in ustvari raztopino v barvi soka v prahu.
- Vodik v paladiju (plin v trdnem stanju). Vodik se v nekaterih kovinah zelo dobro raztopi.
- Virusi v zraku (trdna snov v plinu). Tako kot atmosferski prah so zelo majhne enote trdne snovi, ki jih prevaža plin.
- Živo srebro v srebru (tekočina v trdnem). Je eden od tako imenovanih "amalgamov".
- Čaj (trdno v tekočini). Trdna snov v zelo majhnih dimenzijah (graniti ovojnice) se raztopi na vodi.
- Kraljevska voda (tekočina v tekočini). Gre za sestavo kisline ki omogoča raztapljanje različnih kovin, med katerimi se pojavlja zlato.
- Bronasta (trdno v trdnem). Je zlitina med bakrom in kositrom.
- Limonada (tekočina v tekočini. Čeprav je velikokrat mešanica med trdno in tekočino, je v njej dejansko tekočina, na primer limonin sok.
- Peroksid (tekočina v tekočini). Je raztopina vodikovega peroksida (H2ALI2) v vodi. Uporablja se za razkuževanje ran in v kozmetični industriji.
- Medenina (trdno v trdnem). Je zlitina med trdnimi delci bakra in cinka.
- Ledeno hlajenje (trdno v tekočini). Led vstopi v tekočino in jo ohladi, medtem ko se raztopi. Če se vnese v vodo, je to poseben primer, ko gre za isto snov.
- Fiziološka raztopina (tekočina v tekočini). Voda deluje kot topilo, številne tekoče snovi pa kot topilo.
- Smutiji (trdne snovi v tekočinah). S postopkom mletja nastane kombinacija trdnih snovi v tekočinah.
Sledite z:

