50 Primeri aldehidov in ketonov
Primeri / / November 06, 2023
The aldehidi so organske spojine ki imajo v svoji strukturi karbonilno funkcionalno skupino (= C = O), ki je vezana na ogljikovo verigo in atom vodika. Na primer: metanal (imenovan tudi formaldehid), etanal (imenovan tudi acetaldehid) in propanal (imenovan tudi propaldehid).
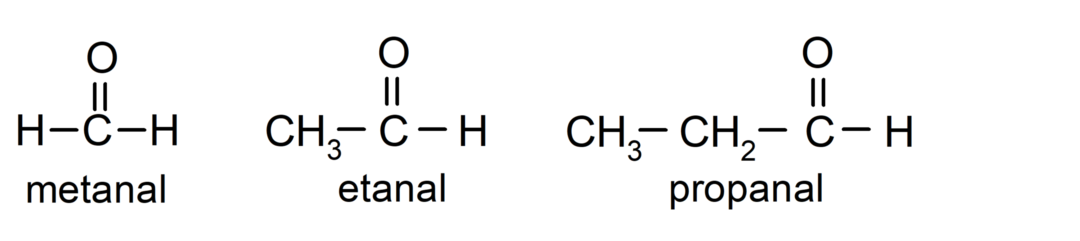
The ketoni So organske spojine, ki imajo v svoji strukturi karbonilno skupino, vezano na dva ogljikova atoma. Na primer: propanon (imenovan tudi aceton), butanon in 2-pentanon.
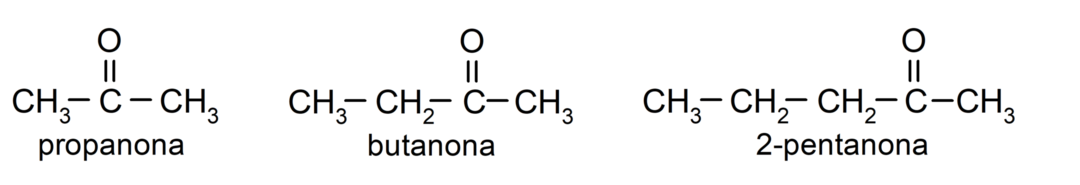
Razlike med aldehidi in ketoni
Glavne razlike med aldehidi in ketoni so:
- Aldehidi imajo v svoji strukturi karbonilno funkcionalno skupino, ki se nahaja na enem končnem koncu, medtem ko imajo ketoni karbonilno skupino na nekončnih položajih struktura.
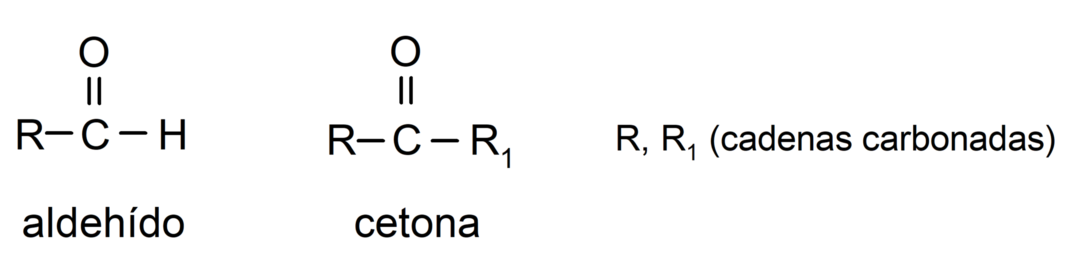
- Aldehidi se oksidirajo z reakcijo s Tollensovim reagentom in tvorijo kovinsko srebro. Prav tako oksidirajo proti Benedictovemu reagentu in tvorijo bakrov oksid. Ketoni se ne oksidirajo z nobenim reagentom.
- Aldehidi se reducirajo v primarne alkohole, ketoni pa v sekundarne alkohole.
Fizične lastnosti
Fizikalne lastnosti aldehidov
Fizikalne lastnosti aldehidov so zelo raznolike, ker so odvisne od zgradbe ogljikove verige, ki je vezana na karbonilno skupino.
Nekateri so:
- Aldehidi, ki so najbolj topni v vodi, so tisti, ki so manjši, kot sta metanal in etanal.
- Hlapni aldehidi imajo oster in celo dražeč vonj.
- Karbonilna skupina jim daje polarnost.
- Običajno imajo višja vrelišča kot kemične spojine podobne velikosti molekul.
Fizikalne lastnosti ketonov
Fizikalne lastnosti ketonov so odvisne od tega, kako nastane ogljikova veriga, ki je povezana s karbonilno skupino.
- Mnogi ketoni imajo prijeten vonj.
- Njegova topnost v vodi je odvisna od velikosti ogljikove verige, vezane na karbonilno skupino. Manjša kot je ogljikova veriga, bolj bo keton topen v vodi.
- Karbonilna skupina jim daje izrazito polarnost.
- Imajo dokaj visoka vrelišča v primerjavi s kemičnimi spojinami primerljive velikosti molekul.
Kemijske lastnosti
Kemijske lastnosti aldehidov
Med kemijskimi lastnostmi aldehidov najdemo:
Oksidirajo in tvorijo ustrezno karboksilno kislino, to pomeni, da bo imela nastala kislina enako število ogljikov v ogljikovi verigi kot aldehid ki je povzročilo. Na primer:
- Oksidacija s Tollensovim reagentom (amonijakov srebrov kompleks v bazični raztopini, [Ag (NH3)2]+) iz etanala proizvaja etanojsko kislino in kovinsko srebro.
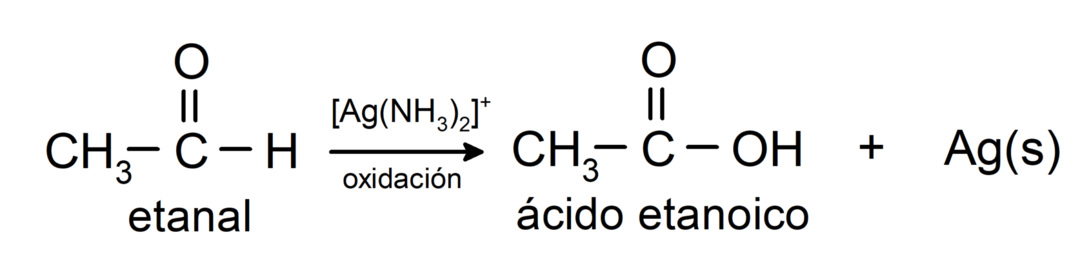
- Pri oksidaciji etanala z Benedictovim reagentom (alkalna raztopina bakrovega sulfata) nastaneta etanojska kislina in bakrov oksid.
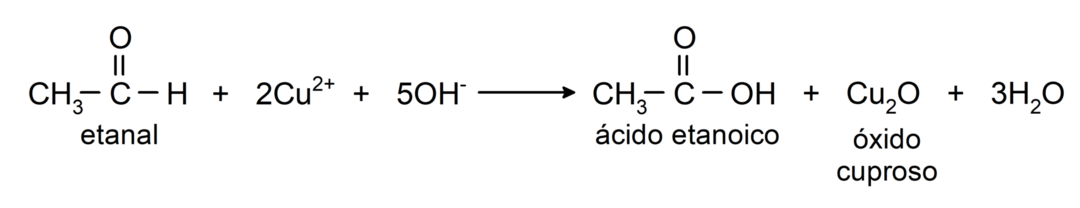
Podvrženi so nukleofilnim adicijskim reakcijam, to je adicija nukleofila na karbonilno skupino. Na primer:
- Adicija cianovodikove kisline za tvorbo cianohidrinov ali cianohidrinov.
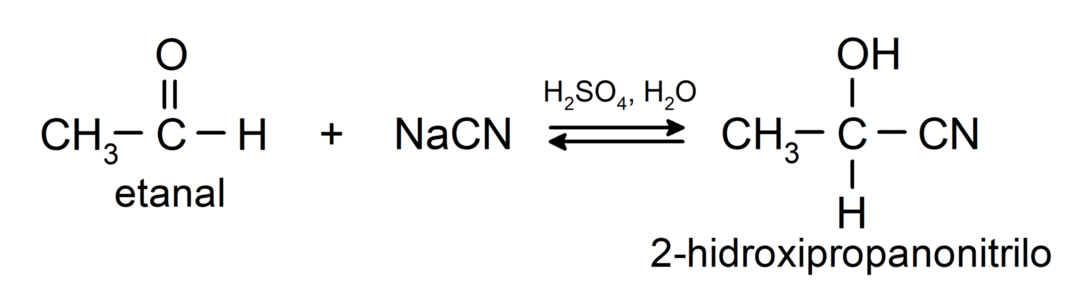
- V prisotnosti brezvodnih kislin se alkoholi dodajo karbonilni skupini aldehidov, da nastanejo acetali in polacetali.
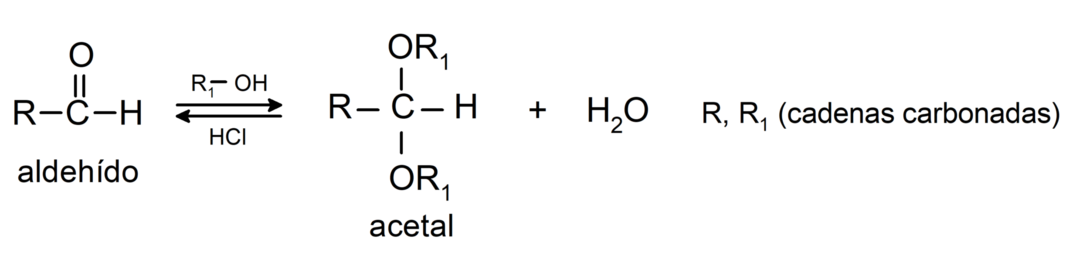
Podvrženi so reakcijam aldolne kondenzacije. Pri teh reakcijah pride do združitve dveh aldehidov v prisotnosti natrijevega hidroksida (NaOH) in kemična spojina nastalo imenujemo aldol. Na primer:
- Reakcija kondenzacije etanala v prisotnosti razredčenega NaOH.
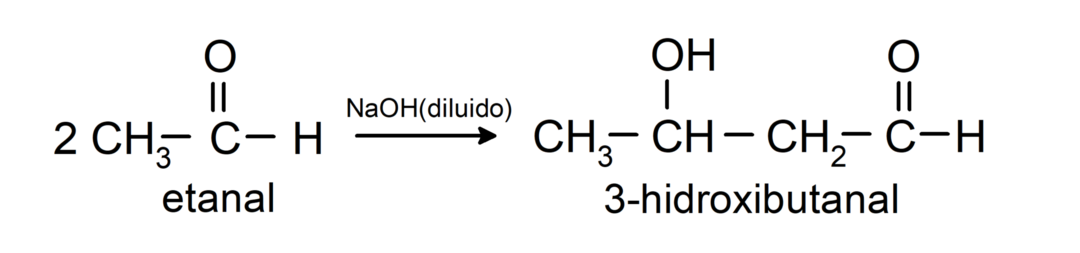
Reducirani so na primarne alkohole. Aldehide lahko reduciramo v primarne alkohole s katalitskim hidrogeniranjem ali redukcijo z natrijevim borohidridom (NaBH).4) in litijev aluminijev hidrid (LiAlH4).
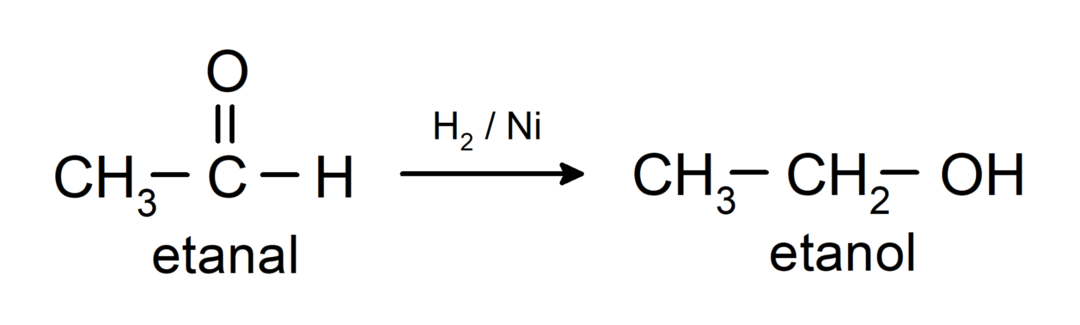
Kemijske lastnosti ketonov
Med kemičnimi lastnostmi ketonov lahko najdemo:
Podvrženi so nukleofilnim adicijskim reakcijam. Na primer:
- Adicija cianovodikove kisline za tvorbo cianohidrinov ali cianohidrinov.
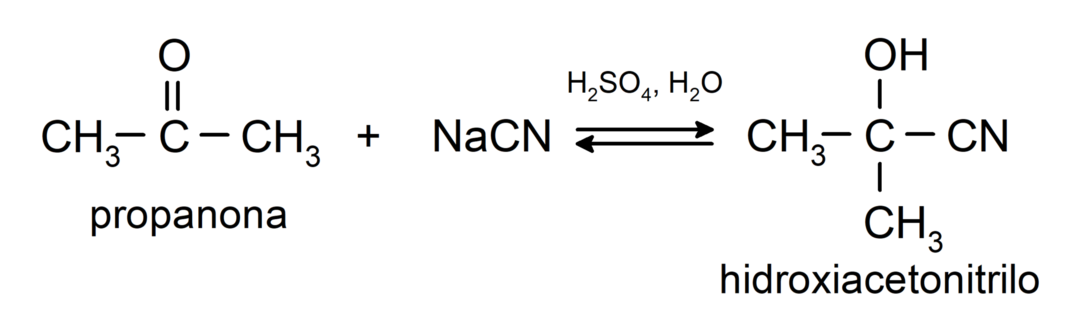
Dodajajo alkohole (v prisotnosti brezvodnih kislin) na karbonilno skupino ketonov, da tvorijo ketale in hemiketale. Na primer:
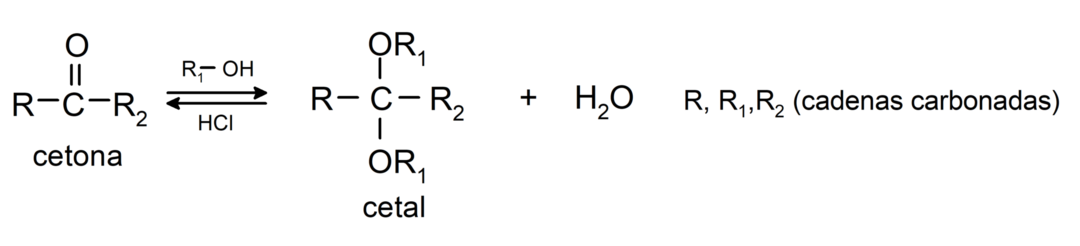
Podvrženi so reakcijam halogeniranja. Ketoni, ki imajo alfa vodik (α) reagirajo z zamenjavo tega vodika s halogeni (klor (Cl), brom (Br), jod (I), fluor (F)) v prisotnosti kislinskih ali bazičnih katalizatorjev. Substitucija poteka skoraj izključno v ogljiku α, to je ogljik, ki je vezan na vodik α. Na primer:
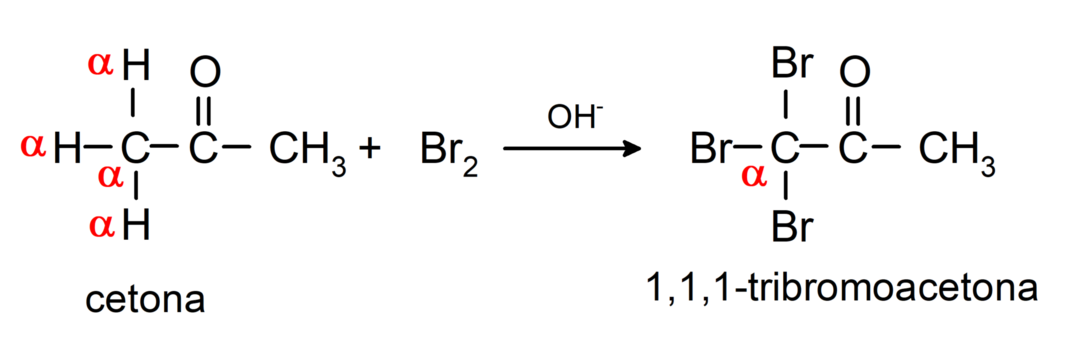
Zmanjšajo se v sekundarne alkohole s katalitskim hidrogeniranjem ali redukcijo z natrijevim borohidridom (NaBH4) in litijev aluminijev hidrid (LiAlH4). Na primer:
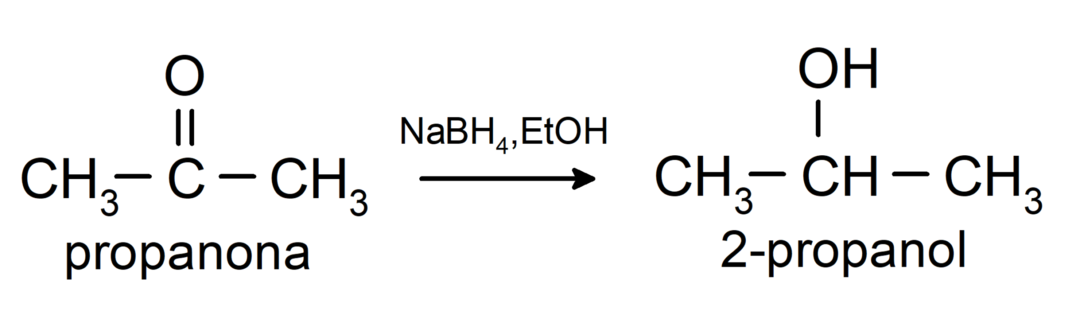
Ketoni se ne oksidirajo s Tollensovim in Benedictovim reagentom.
Nomenklatura aldehidov
V skladu s pravili, ki jih je določila Mednarodna zveza za čisto in uporabno kemijo (IUPAC), Aldehidi so poimenovani s predponami, ki označujejo število ogljikovih atomov v verigi. gazirana. Položaja karbonilne skupine ni treba navesti, saj je vedno na položaju ena, na enem koncu molekule. Poleg tega je pripona -al zapisana na koncu imena aldehida. Na primer:
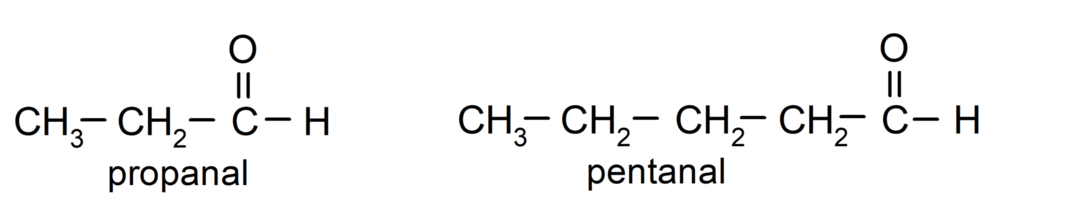
Če je aldehid sestavljen iz več ogljikovih verig, to pomeni, da ima veje, je za glavno verigo izbrana ogljikova veriga z največjim številom ogljikovih atomov. Druge verige so poimenovane kot skupine substituentov, položaj vsakega substituenta pa je izbran tako, da zavzema najmanjše možno število v verigi. Poleg tega se atomi ogljika začnejo šteti od konca, ki ima karbonilno skupino. Na primer:
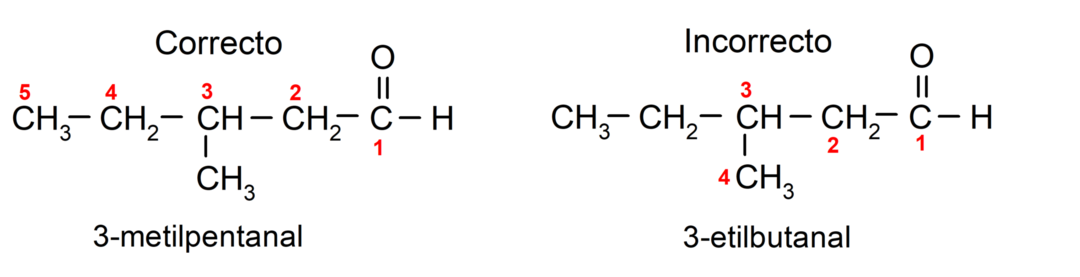
Aldehidi, ki imajo dve karbonilni skupini, so poimenovani s pripono -dial. Na primer:
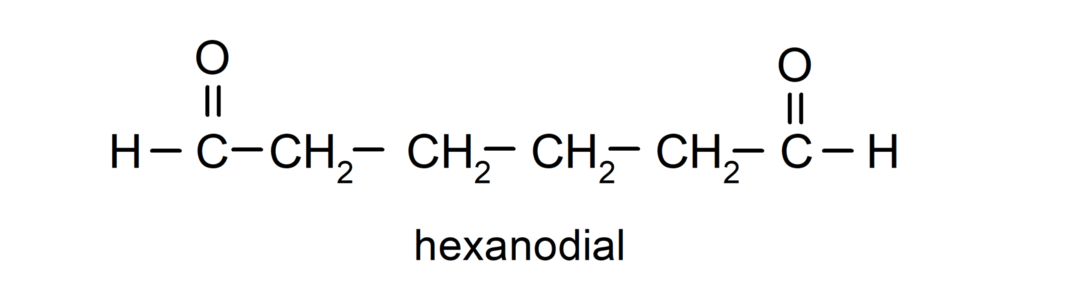
Nomenklatura ketonov
Po Mednarodni zvezi za čisto in uporabno kemijo (IUPAC) so ketoni poimenovani s predponami, ki označujejo število ogljikov v ogljikovi verigi.
Po drugi strani pa je ime acetona zapisano s pripono -one, pred katero je številka, ki označuje položaj karbonilne skupine v ogljikovi verigi. Mesto karbonilne skupine je treba izbrati tako, da ustreza najnižjemu možnemu številčenju. Na primer:
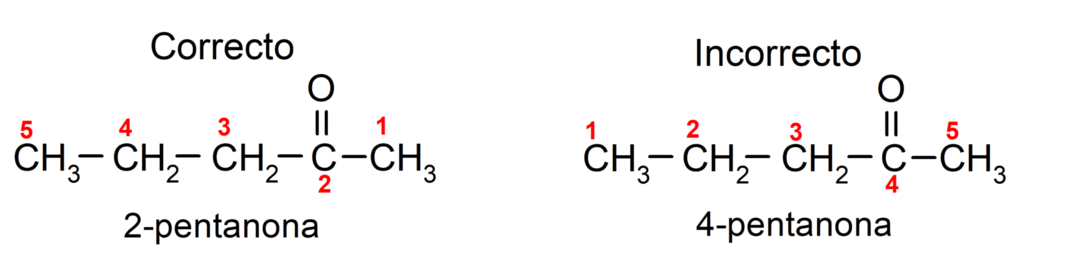
Za poimenovanje ketona, ki je sestavljen iz več ogljikovih verig, torej z vejami, izberemo kot glavna veriga, ogljikova veriga z največjim številom ogljikovih atomov in ki vsebuje skupino karbonil. Preostale verige so poimenovane kot substituentske skupine. Na primer:
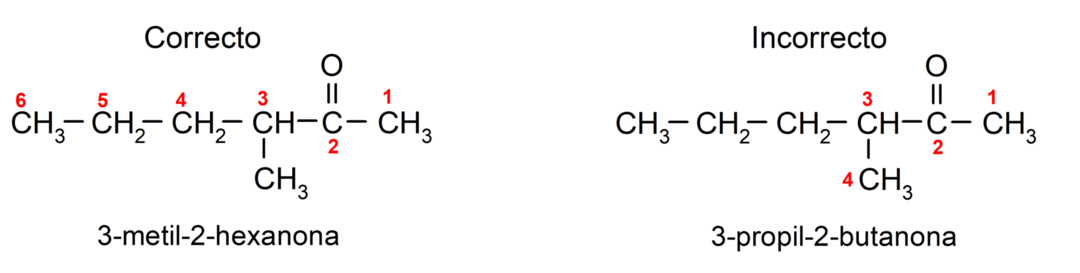
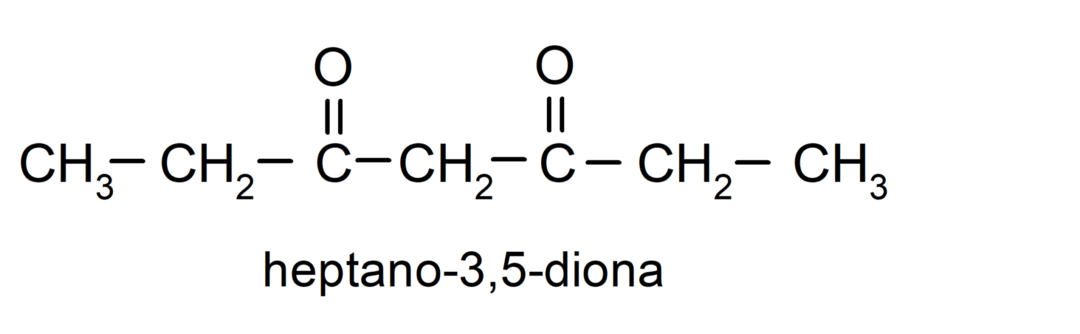
Obstajajo ketoni, ki imajo dve karbonilni skupini, imenujemo jih dioni. Na primer:
Primeri aldehidov
- metanal (formaldehid)
- etanal (acetaldehid)
- propanal (propaldehid)
- butanal
- pentanal
- heksanal
- 3-bromociklopentankarbaldehid
- cikloheksankarbaldehid
- benzaldehid
- 4,4-dimetilpentanal
- 2-hidroksi-butanal
- 2-hidroksi-2-metil-butanal
- 2,3-dimetilpentanal
- pentanedial
- 4-hidroksi-3-metoksibenzaldehid
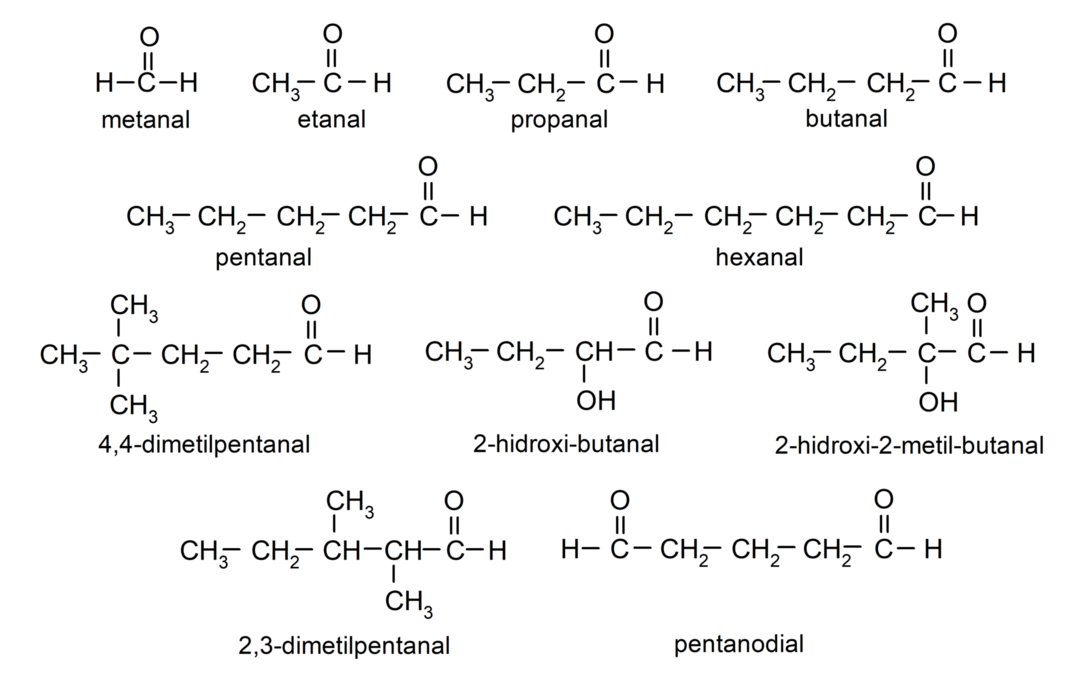
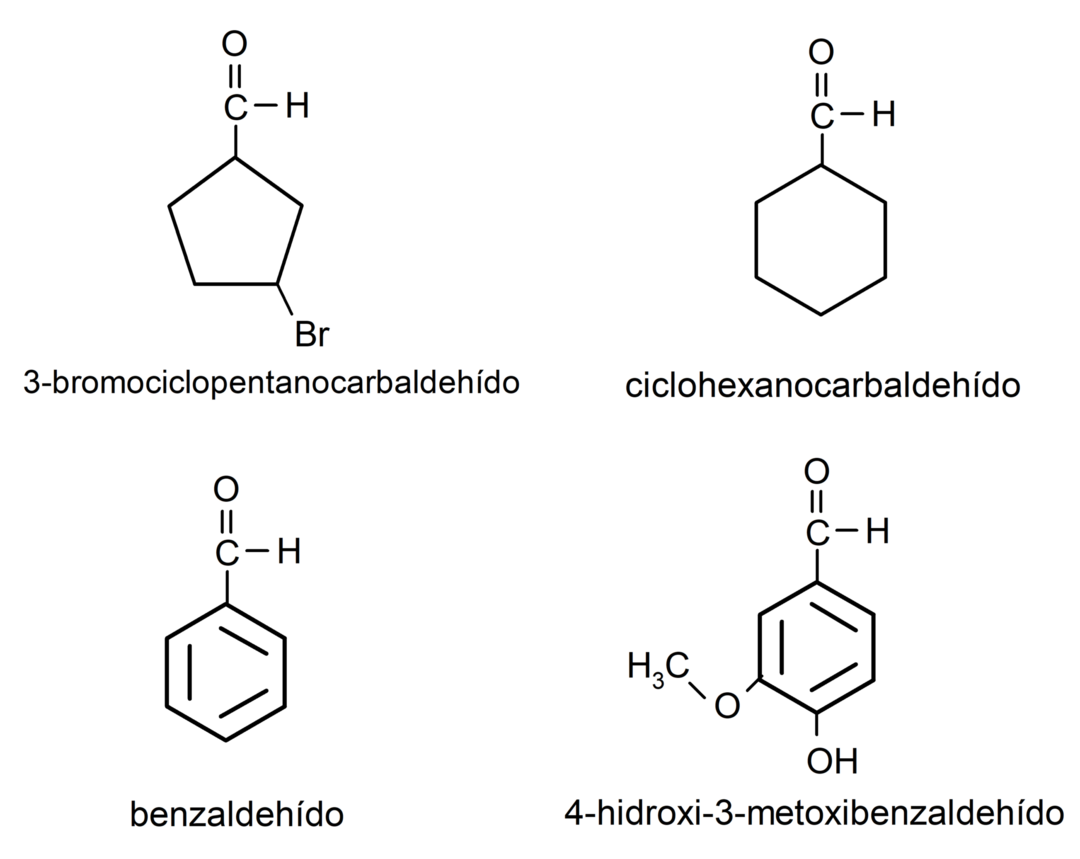
Primeri ketonov
- propanon (aceton)
- butanon
- 2-pentanon
- 4-metilpentan-2-on
- 3-metilcikloheksanon
- cikloheksilmetilketon
- 3,4-dimetil-heksan-2-on
- etil fenil keton
- 2,4-pentandion
- cikloheksanon
- 3-pentanon
- 3-metil-2,4-pentandion
- 1-fenilpropanon
- ciklopentanon
- difenil keton
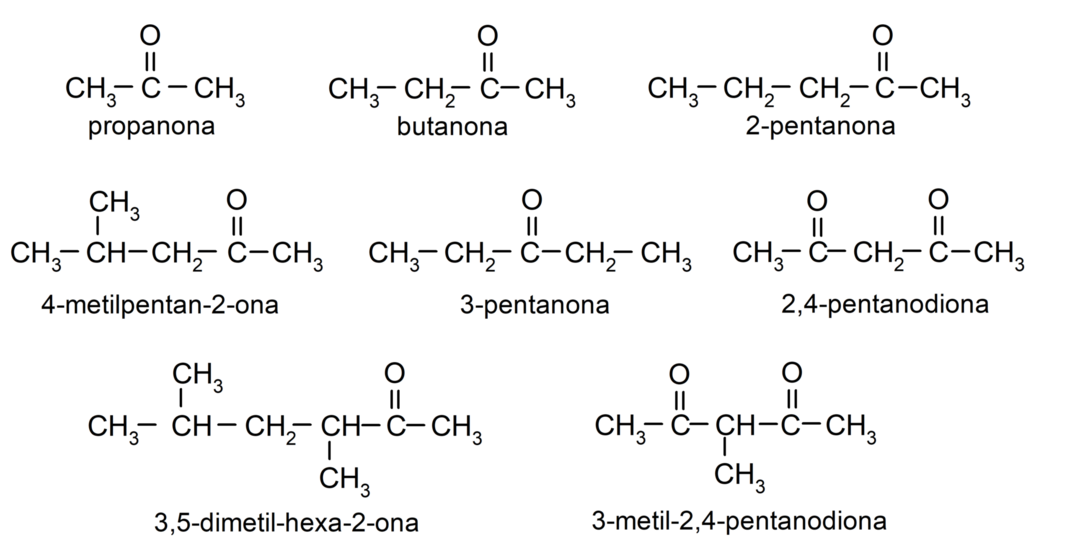
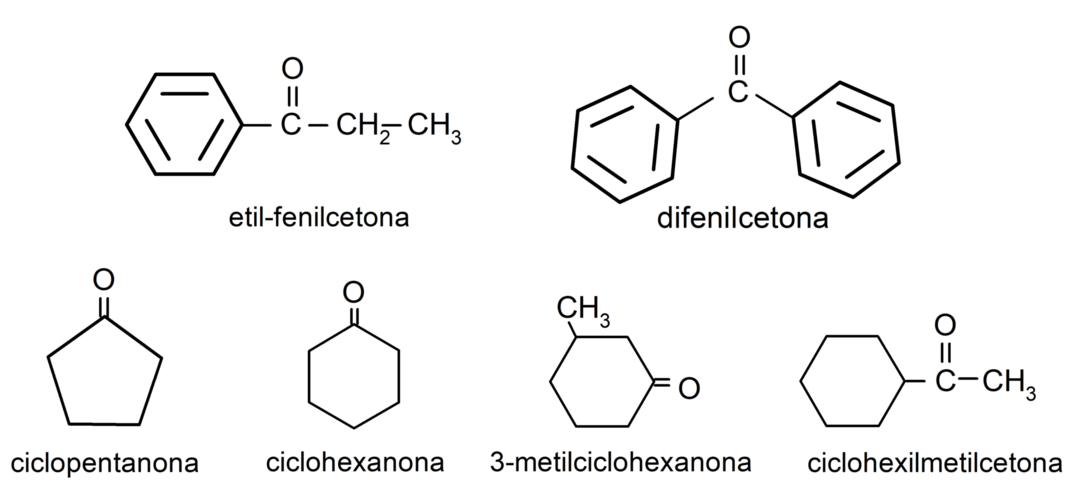
Uporaba aldehidov v vsakdanjem življenju
Nekatere uporabe aldehidov so:
- Uporabljajo se za proizvodnjo topil, barv, parfumov, smol in esenc.
- Uporabljajo se kot konzervansi v kozmetičnih izdelkih, bioloških vzorcih in trupelih. Za te namene se največ uporablja formaldehid.
- Uporabljajo se za proizvodnjo plastike, ki omogoča zamenjavo kovinskih delov v avtomobilski industriji.
- Uporabljajo se kot arome za nekatera živila.
- Uporabljajo se kot razkužila.
- Uporabljali so jih za izdelavo nekaterih eksplozivov, kot je pentaeritritol tetranitrat (TNPE).
Uporaba ketonov v vsakdanjem življenju
Nekatere uporabe ketonov so:
- Uporabljajo se pri proizvodnji topil. Zlasti aceton se pogosto uporablja za odstranjevanje barv in lakov.
- Uporabljajo se pri izdelavi nekaterih gum in maziv.
- Uporabljajo se za proizvodnjo barv, lakov in lakov.
- Uporabljajo se za proizvodnjo zdravil in kozmetike.
Toksičnost aldehidov in ketonov
- Aldehidi. Stik z aldehidi povzroča draženje kože, oči in dihalnih poti. Poleg tega je bila izpostavljenost aldehidom povezana z boleznimi, kot so rak, kontaktni dermatitis ter jetrne in nevrodegenerativne bolezni. Formaldehid, na primer, WHO (Svetovna zdravstvena organizacija) šteje za rakotvorno spojino.
- ketoni. Ponavljajoča se izpostavljenost ketonom lahko povzroči poškodbe centralnega živčnega sistema. To lahko povzroči izgubo spomina, šibkost, bolečine v mišicah in krče. Poleg tega, če koža pride v stik s ketoni, se pojavi suhost in razpoke. Po drugi strani pa ob vdihavanju ketonov pride do draženja dihalnih poti in kašlja.
Reference
- Llorens Molina, JA. (2018). “Aldehidi in ketoni: nekaj primerov.” http://hdl.handle.net/
- Gabriel Pinto Cañón, Manuela Martín Sánchez, José María Hernández Hernández, María Teresa Martín Sánchez (2015) “Tollensov reagent: od identifikacije aldehidov do njihove uporabe v nanotehnologiji. Zgodovinski vidiki in didaktične aplikacije.”Zv. 111 št. 3. Kraljevo špansko kemijsko društvo.
- William Bauer, ml. (2000) «Metakrilna kislina in njeni derivati» v Ullmannovi Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. DOI: 10.1002/14356007.a16_441.
- "Razkrivajo nov mehanizem toksičnosti v skupini rakotvornih spojin, ki izhajajo iz prehrane in okolja" (2022) V: www.conicet.gov.ar Na voljo v: https://www.conicet.gov.ar/ Dostopano: 20. junij 2023.
Sledi z:
- Alkoholi
- Sladkorji
- Alkani



