Primeri endotermnih reakcij
Primeri / / November 09, 2023
A endotermna reakcija To je reakcija, ki absorbira energijo iz medija v obliki toplote. Pri teh reakcijah je potrebno, da se reaktanti pretvorijo v produkte, absorbirajo toploto, zaradi česar imajo produkti večjo energijo kot reaktanti, ki so jih povzročili. Nekateri primeri endotermnih reakcij so: fotosinteza in elektroliza vode.
- Poglej tudi: Kemijske reakcije
Primeri endotermnih reakcij v vsakdanjem življenju
Nekatere glavne endotermne reakcije so:
Proizvodnja ozona v ozračju. Ozon nastaja v ozračju, ko molekularni kisik (O2) absorbira ultravijolično sevanje in razpade. Potem lahko atom kisika (O) sodeluje z drugo molekulo kisika (O2) in tvorijo ozon (O3).

Elektroliza vode. To je postopek, s katerim se uporablja električna energija vodi, da jo loči na dve komponenti, vodik (H) in kisik (O).
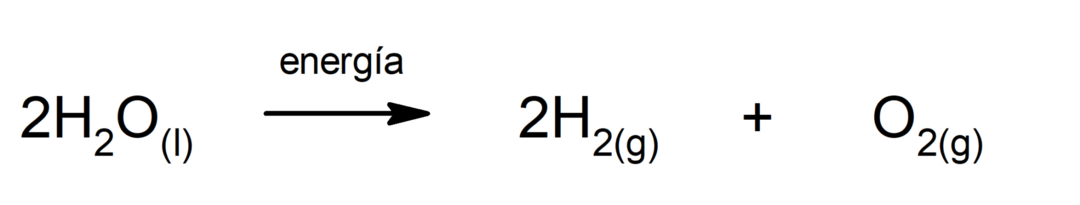
fotosinteza. To je kemična reakcija, s katero se absorbira sončna energija, ogljikov dioksid (CO2) se pretvori v glukozo. Ta reakcija predstavlja glavno pot prehrane rastlin.
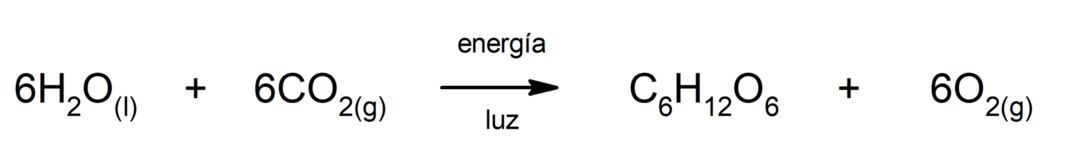
Proizvodnja železovega(II) sulfida. Za potek reakcije med žveplom in železom je potrebno zagotoviti energijo v obliki toplote.
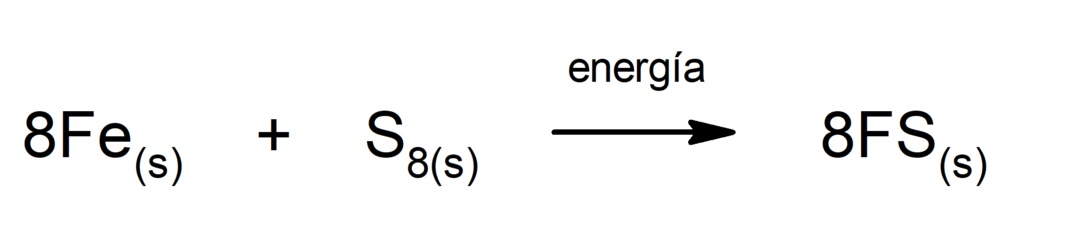
Razgradnja ogljikovega dioksida (CO2). Razgradnja CO2 Pri visokih temperaturah proizvaja ogljikov monoksid (CO) in kisik (O2).
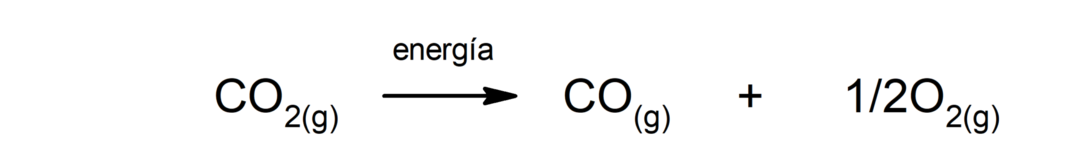
Razgradnja kalcijevega karbonata (CaCO3). Kalcijev karbonat razpade z absorpcijo toplote, da nastaneta kalcijev oksid (CaO) in ogljikov dioksid (CO2).
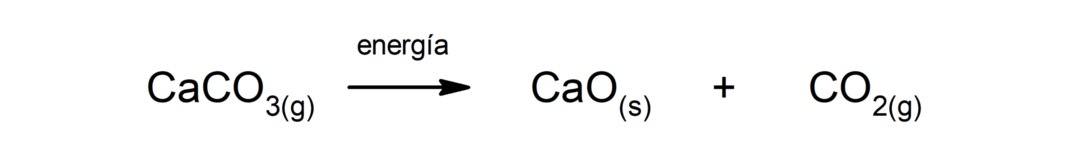
Razlika med endotermno in eksotermno reakcijo
Glavna razlika med endotermnimi in eksotermnimi reakcijami je v tem, da endotermne reakcije absorbirajo toploto, medtem ko eksotermne reakcije sproščajo toploto.
Poleg tega je za endotermne reakcije značilno povečanje entalpije, medtem ko so eksotermne reakcije povezane z zmanjšanjem entalpije.
Entalpija je termodinamična količina, ki določa pretok toplotne energije pri konstantnem tlaku med kemijsko reakcijo. Predstavljena je s črko H, njena variacija pa je eden od glavnih indikatorjev za opredelitev, ali je kemična reakcija endotermna ali eksotermna.
- Če ima kemijska reakcija spremembo entalpije, večjo od nič (ΔH > 0) je endotermna.
- Če ima kemijska reakcija spremembo entalpije manjšo od nič (ΔH < 0) je eksotermna.
Sledi z:
- Fizikalno-kemijski pojavi
- Kemija v vsakdanjem življenju
- Kemija v vsakdanjem življenju
- Organska in anorganska kemija
Reference
- Soto-Córdoba, S. (2016). Endotermne reakcije. Tehnično skladišče Tehnološki inštitut Kostarike.
- Corominas, J. (2017). Kemijske reakcije vsakdanjega življenja. Alembic, (90), 8-26.
- Sánchez, M. T. M. in Sánchez, M. M. (2002). Eksperimentalni študij endotermnih reakcij za študente ESO. Annals of Chemistry of the RSEQ, (4), 36-39.
