20 Примери хемијских појава
Мисцелланеа / / July 04, 2021
Тхе хемијске појаве (или хемијске реакције) су они феномени у којима долази до промена у материји и стварају се нове супстанце назване „производи“, а друге назване „реактанти“ се разлажу. На пример: труљење дрвета, сагоревање папира, компостирање.
Хемијске реакције могу бити спонтано (реакције које се јављају без потребе за енергијом или катализаторима) или не спонтано (реакције којима је потребан допринос енергије, катализатора или неке спољне интервенције). Много пута, да би се реакција појавила, неопходно је да реагенси имају а температура специфично, а пХ подешена вредност притиска итд.
Такође је можда неопходно контролисати брзина на које се јављају хемијске реакције. Тхе катализатори Они су супстанце које се хемијској реакцији додају да би се повећала брзина, док су инхибитори супстанце које успоравају брзину хемијских реакција. Остали фактори који утичу на брзину хемијске реакције су температура, притисак, концентрација реактаната и природа саме реакције.
Може вам послужити:
Врсте хемијских појава
Хемијске реакције могу бити:
Неорганске реакције. Интервенисати неорганска једињења и могу се класификовати према:
- Смисао у коме се реакција јавља.
-
Реверзибилне реакције. Јављају се у оба смера, тако да се производи могу разградити и поново створити реактанте.
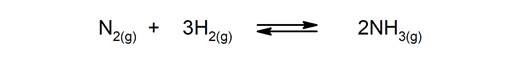
-
Неповратне реакције. Догађају се само у једном правцу.

-
Реверзибилне реакције. Јављају се у оба смера, тако да се производи могу разградити и поново створити реактанте.
- Тип честице која реагује.
-
Киселинско-базне реакције. Долази до преноса јона Х+.

-
Реакције редукције оксидације. Један од реактаната оксидира (повећава његов број оксидација), док је друга смањена (смањује се њен оксидациони број). У тим реакцијама долази до преноса електрона.

-
Киселинско-базне реакције. Долази до преноса јона Х+.
- Брзина реакције.
-
Брзе реакције. Јављају се у врло кратком времену.
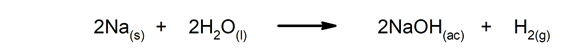
-
Споре реакције Треба им пуно времена да се заврше.
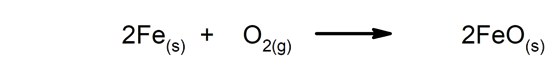
-
Брзе реакције. Јављају се у врло кратком времену.
- Облик енергије коју емитује или апсорбује.
-
Егзотермне реакције. Када се појаве, ослобађају топлоту.
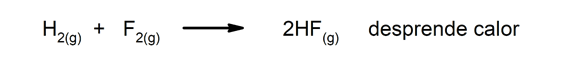
-
Ендотермне реакције. Када се појаве, упијају топлоту.

-
Егзолуминозне реакције. Када се појаве, емитују светлост.

-
Ендолуминасте реакције. Да би им се догодило, потребна им је светлост.

-
Егзотермне реакције. Када се појаве, ослобађају топлоту.
- Тип трансформације.
-
Реакције синтезе или адиције. Две супстанце се комбинују и формирају нову супстанцу.
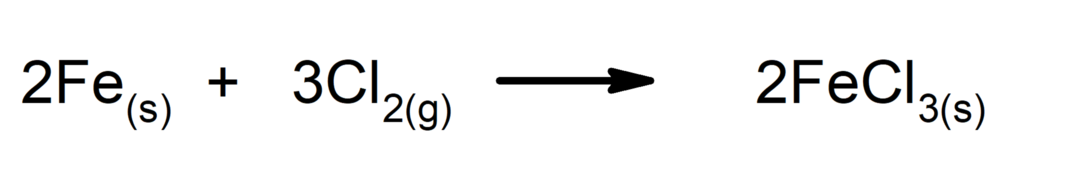
-
Реакције разлагања. Једна или више супстанци се распадају на своје најједноставније састојке.
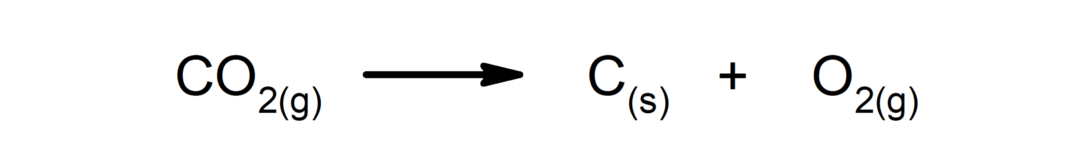
-
Реакције измештања или замене. Један елемент или једињење замењује други у једињењу, ослобађајући га.
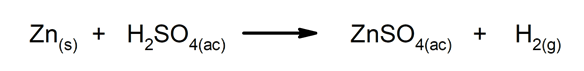
-
Реакције двоструке супституције. Два једињења истовремено размењују елементе или једињења.

-
Реакције синтезе или адиције. Две супстанце се комбинују и формирају нову супстанцу.
Органске реакције. Они су реакције у којима интервенишу органска једињења. Имају мноштво класификација заснованих на типу органског једињења које реагује и врсти реакције којој пролази. Неки примери су:
-
Халогенизација алкана. Водоник је замењен за а алкан халогеном.
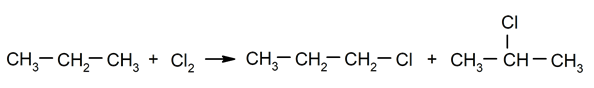
-
Сагоревање алкана. Алкан реагује са кисеоником стварајући угљен-диоксид и воду, ако је сагоревање завршено.
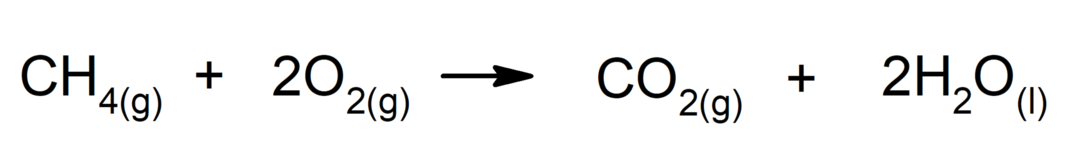
-
Халогенизација алкени. Халогени су супституисани за један или оба водоника угљеника који су укључени у двоструку везу.
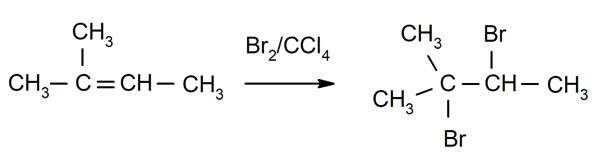
-
Хидрогенирање алкена. Водоници се додају угљеницима који су укључени у двоструку везу да би се створио одговарајући алкан.
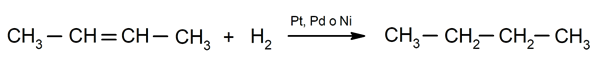
Значај хемијских појава
Многи хемијски феномени одржати живот живих бића, као што је варење код људи и Животиње, фотосинтеза у биљкама и дисање код обе.
Још један веома важан хемијски процес, посебно у животу микроорганизми, је ферментација, који се обично користи у производњи храна попут сирева, јогурта, вина и пива.
Све повећати и раст од а живо биће Укључује хемијске реакције које се у њему одвијају, понекад подстакнуте одређеним условима околине.
Примери хемијских појава
Око нас постоје бројни случајеви хемијских појава или процеса који их укључују:
- Трулеж дрвета
- Сагоревање од папира
- Отпор према антибиотици бактерија
- Млеко које се укисели
- Дезинфекција ране са алкохол
- Употреба воћне соли у борби против горушице
- Гори свећа
- Згрушавања крви
- Умор мишића након интензивног вежбања
- Смрт инсекти инсектицидима
- Добијање рокуефорт сира
- Добијање јабуковаче
- Добијање јогурта
- Компостирање
- Енсилаге
- Добијање биоетанола из меласе
- Натечене лимене конзерве
- Покварено јаје
- Рђавање решетке
- Добијање биодизела из палминог уља
Хемијски феномени у индустрији
Одређени хемијски феномени су такође кључни уиндустрија. За почетак сагоревање угљоводоници (као што су бензин, дизел или керозин) производи Енергија да покрећу машине које се баве безбројним индустријским процесима.
С друге стране, индустрија челика, папир, пластика, грађевински материјали, боје, лекови, производи за агро, итд., заснивају се на разним хемијским појавама попут галванизације, електролизе и многих других други више.
Генерација нови извори енергије (попут биодизела и биоетанола) такође се заснива на овој врсти појаве.
Трансформација енергије
У хемијским појавама уобичајено је да их има трансформација енергије. На пример, када се хемијска енергија садржана у везама одређеног молекула трансформише у електричну енергију или ослобађа као топлота (то се дешава у егзотермним појавама, на пример када се хлороводонична киселина помеша са цинком), долази до трансформације Енергија. Исто се дешава када се светлосна енергија ухвати и трансформише у хемијску енергију.
За неке хемијске процесе потребна је топлота и називају се „ендотермним“. Други захтевају присуство катализатора или кофактора.


