Пример Чарлсовог закона
Стање / / November 13, 2021
Чарлсов гасни закон или закон сталног притиска, је још један од закона о гасу, најавио Геј-Лусак, који је објавио дело Жака Шарла, објављено око 20. године пре.
Чарлсов закон предвиђа понашање масе гаса када притисак остаје константан, а температура и запремина варирају.
Чарлсов закон је наведен на следећи начин:
При константном притиску, запремина гаса је директно пропорционална промени његове температуре.
Стални притисак: односи се на чињеницу да притисак који гас врши на зидове контејнера неће варирати током искуства.
Волуме: то је заузети простор који гас заузима, генерално се сматра контејнером са зидовима који се не деформишу, а чији поклопац ради као клип.
температура: То је повећање или губитак топлоте којем гас пролази током експеримента. Ако се температура повећава, запремина се повећава. Ако се температура смањи, смањује се и запремина.
Алгебарски, Чарлсов закон се изражава следећом формулом:

Где:
В = запремина гаса
Т = температура гаса
к = константа пропорционалности за ту масу гаса.
То значи да је за дату масу гаса, при константном притиску, однос између запремине и варијације температуре, увек ће имати исти однос пропорционалности, представљен константом к:

Дакле, када је константа одређена, можемо израчунати било коју од других вредности из других познатих података:
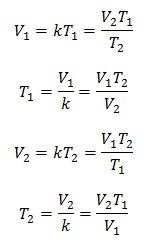
3 примера Чарлсовог закона примењена на проблеме:
Пример 1: Израчунајте нову запремину, ако се у посуди налази маса гаса која заузима запремину од 1,3 литра, на температури од 280 К. Израчунајте запремину када достигнете температуру од 303 К.
В1 = 1,3 л.
Т1 = 280 К
В2 = ?
Т2 = 303 К
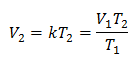
Замена вредности:
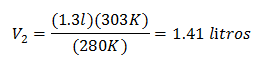
Нова запремина на 303 К је 1,41 литара.
Пример 2. Ако имамо гас који на 10 степени Целзијуса заузима 2,4 литара, израчунајте коначну температуру, ако на крају заузима 2,15 литара.
В1 = 2,4 л
Т1 = 10 ° Ц = 283 К
В2 = 2,15 л
Т2 = ?
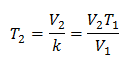
Замена вредности:
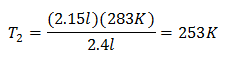
Нова температура је 253 К, што је једнако -20 ° Ц.
Пример 3. Имамо гас чија је почетна температура 328 К, коначна запремина 3,75 л, а константа односа 0,00885.
В1 = ?
Т1 = 328 К
В2 = 3,75 л
Т2 = ?
к = 0,00885
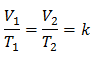
Замена вредности:
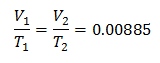
Да бисте сазнали почетни волумен:
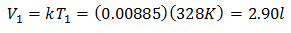
Почетна запремина је 2,90 л.
Да бисте сазнали коначну температуру:
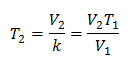
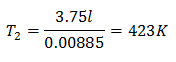
Коначна температура биће 423 К, што је једнако 150 ° Ц.
