50 Примери алдехида и кетона
Примери / / November 06, 2023
Тхе алдехиди су органска једињења који у својој структури имају карбонилну функционалну групу (= Ц = О) која је везана за угљенични ланац и атом водоника. На пример: метанал (који се назива и формалдехид), етанал (такође назван ацеталдехид) и пропанал (који се такође назива пропалдехид).
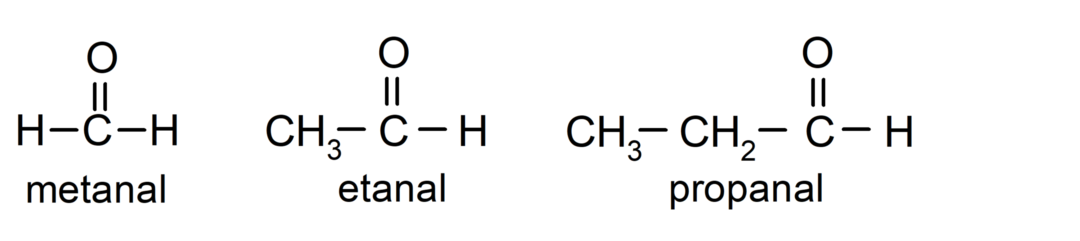
Тхе кетони То су органска једињења која у својој структури имају карбонилну групу везану за два атома угљеника. На пример: пропанон (који се назива и ацетон), бутанон и 2-пентанон.
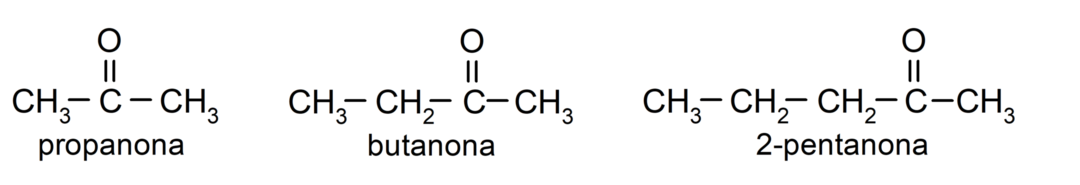
Разлике између алдехида и кетона
Главне разлике између алдехида и кетона су:
- Алдехиди имају у својој структури карбонилну функционалну групу која се налази на једном терминалном крају, док кетони имају карбонилну групу која се налази у нетерминалним позицијама својих структура.
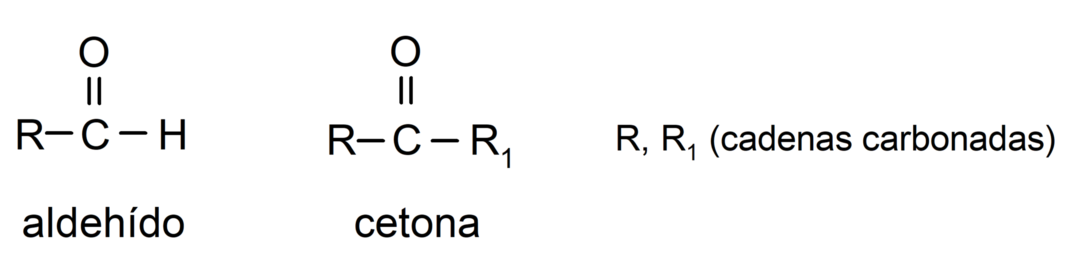
- Алдехиди се оксидују реакцијом са Толенсовим реагенсом, формирајући метално сребро. Они такође оксидирају против Бенедиктовог реагенса, формирајући бакров оксид. Кетони се не оксидују ни са једним реагенсом.
- Алдехиди се редукују у примарне алкохоле, док се кетони редукују у секундарне алкохоле.
Физичка својства
Физичка својства алдехида
Физичка својства алдехида су веома разнолика јер зависе од конституције угљеничног ланца који је везан за карбонилну групу.
Неки су:
- Алдехиди који су најрастворљивији у води су они мање величине, као што су метанал и етанал.
- Испарљиви алдехиди имају оштар и чак иритирајући мирис.
- Карбонилна група им даје поларитет.
- Обично имају више тачке кључања од хемијских једињења сличне молекуларне величине.
Физичка својства кетона
Физичка својства кетона зависе од тога како се формира угљенични ланац који је везан за карбонилну групу.
- Многи кетони имају пријатан мирис.
- Његова растворљивост у води зависи од величине угљеничног ланца везаног за карбонилну групу. Што је угљенични ланац мањи, то ће кетон бити растворљивији у води.
- Карбонилна група им даје изражен поларитет.
- Имају прилично високе тачке кључања у поређењу са хемијским једињењима упоредиве молекуларне величине.
Хемијска својства
Хемијска својства алдехида
Међу хемијским својствима алдехида можемо наћи:
Они се оксидују да би се формирала одговарајућа карбоксилна киселина, односно, формирана киселина ће имати исти број угљеника у ланцу угљеника као и алдехид то је довело до тога. На пример:
- Оксидација Толленсовим реагенсом (комплекс амонијачног сребра у базичном раствору, [Аг (НХ3)2]+) из етанала производи етанску киселину и метално сребро.
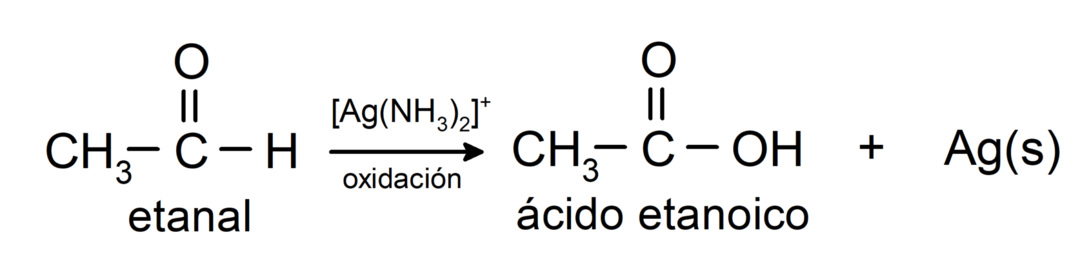
- Оксидацијом са Бенедиктовим реагенсом (алкалним раствором бакар сулфата) етанала настају етанска киселина и бакров оксид.
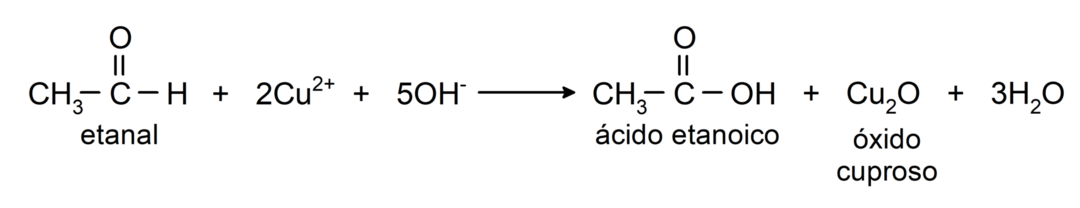
Они пролазе кроз реакције нуклеофилне адиције, односно додавање нуклеофила карбонилној групи. На пример:
- Додавање цијанохидрине да би се формирали цијанохидрини или цијанохидрини.
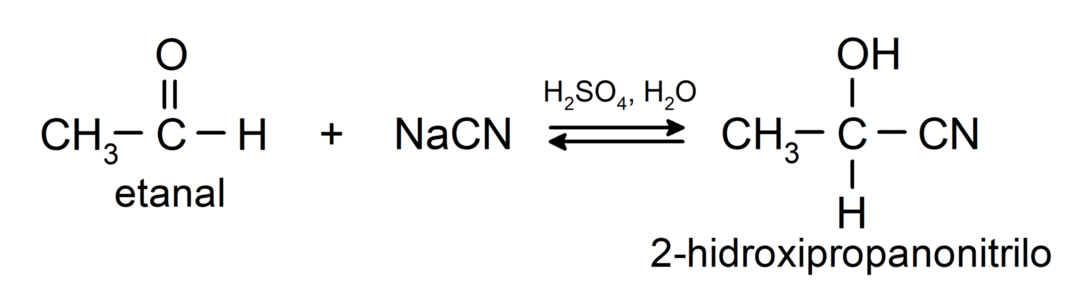
- У присуству анхидрованих киселина, карбонилној групи алдехида се додају алкохоли да би се формирали ацетали и хемиацетали.
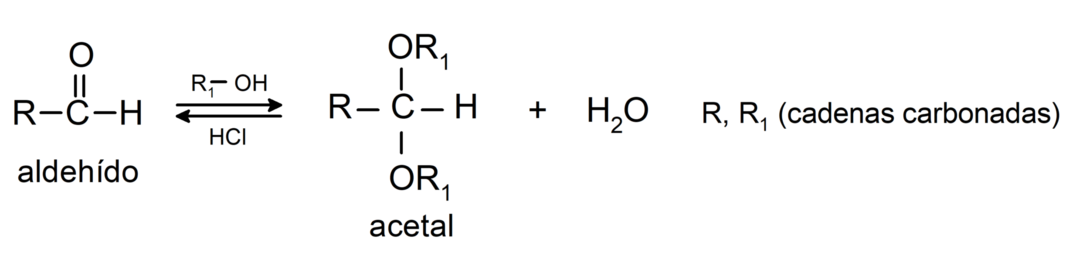
Они пролазе кроз реакције кондензације алдола. У овим реакцијама долази до спајања два алдехида у присуству натријум хидроксида (НаОХ) и хемијско једињење настали се назива алдол. На пример:
- Реакција кондензације етанала у присуству разблаженог НаОХ.
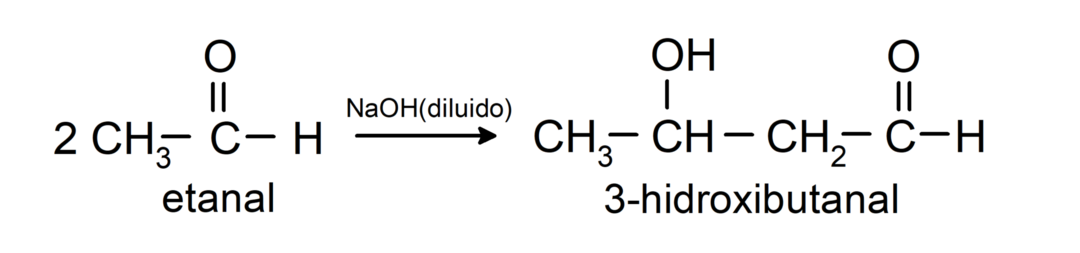
Своде се на примарне алкохоле. Алдехиди се могу редуковати у примарне алкохоле каталитичком хидрогенацијом или редукцијом са натријум борохидридом (НаБХ).4) и литијум алуминијум хидрид (ЛиАлХ4).
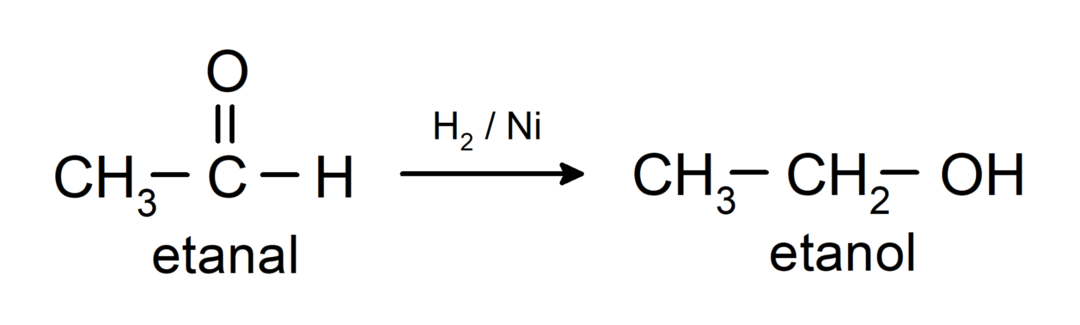
Хемијска својства кетона
Међу хемијским својствима кетона можемо наћи:
Они пролазе кроз реакције нуклеофилне адиције. На пример:
- Додавање цијанохидрине да би се формирали цијанохидрини или цијанохидрини.
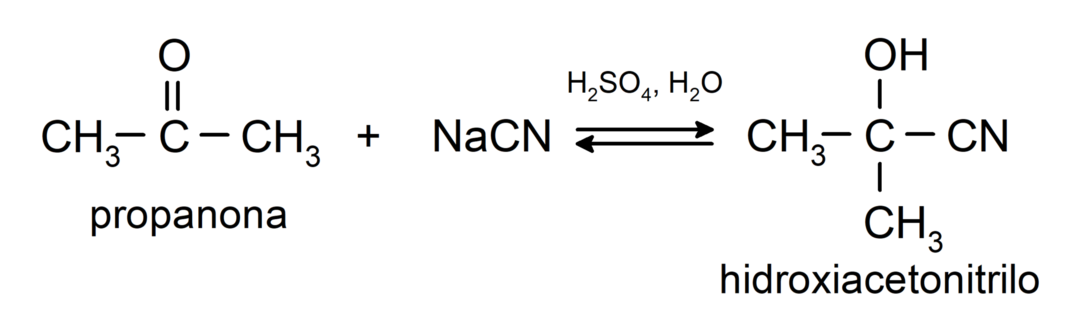
Додају алкохоле (у присуству анхидрованих киселина) на карбонилну групу кетона да би се формирали кетали и хемикетали. На пример:
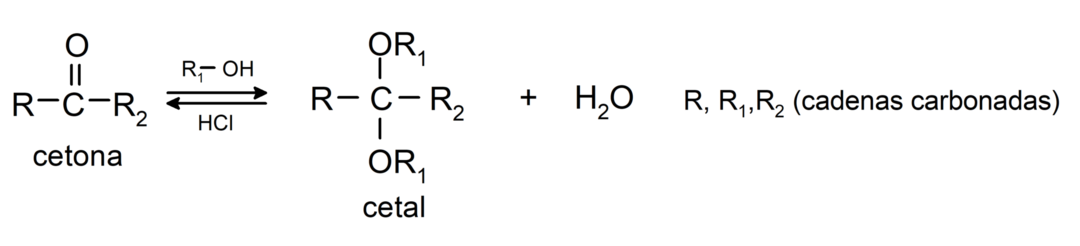
Они пролазе кроз реакције халогенације. Кетони који имају алфа водоник (α) реагују заменом овог водоника халогенима (хлор (Цл), бром (Бр), јод (И), флуор (Ф)) у присуству киселих или базних катализатора. Замена се дешава скоро искључиво у угљенику α, односно угљеник који је везан за водоник α. На пример:
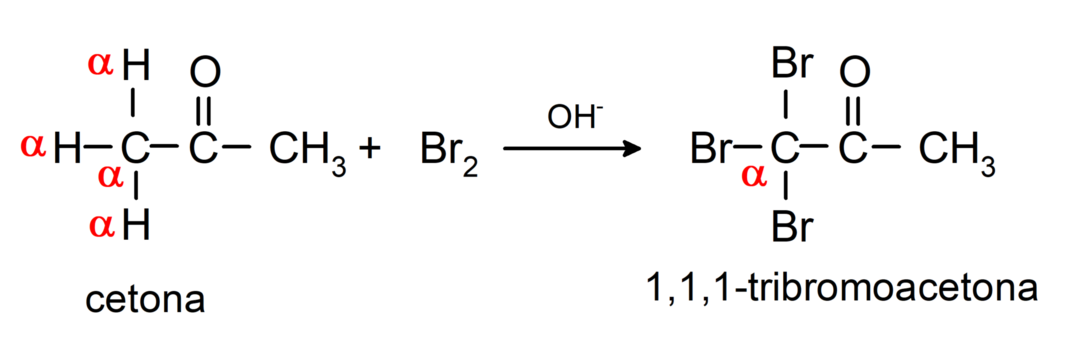
Своде се на секундарне алкохоле каталитичком хидрогенацијом или редукцијом са натријум борохидридом (НаБХ4) и литијум алуминијум хидрид (ЛиАлХ4). На пример:
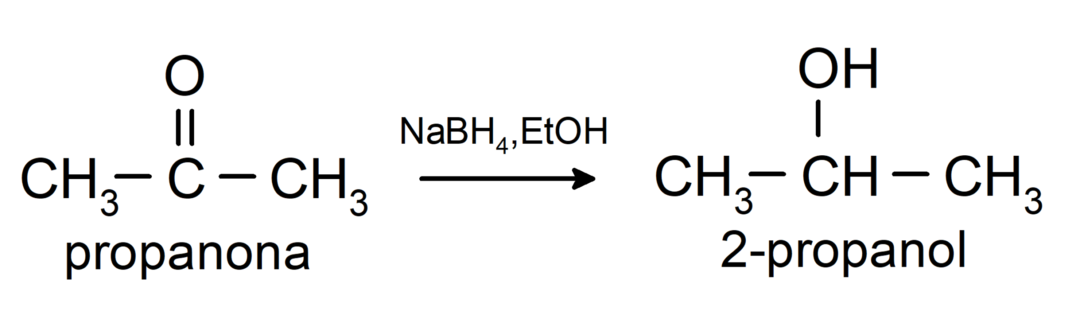
Кетони се не оксидирају Толленсовим и Бенедиктовим реагенсима.
Номенклатура алдехида
Према правилима које је установила Међународна унија за чисту и примењену хемију (ИУПАЦ), Алдехиди се именују помоћу префикса који означавају број угљеника у ланцу. газирана. Није потребно прецизирати положај карбонилне групе, пошто је она увек у позицији један, на једном крају молекула. Додатно, суфикс -ал пише се на крају назива алдехида. На пример:
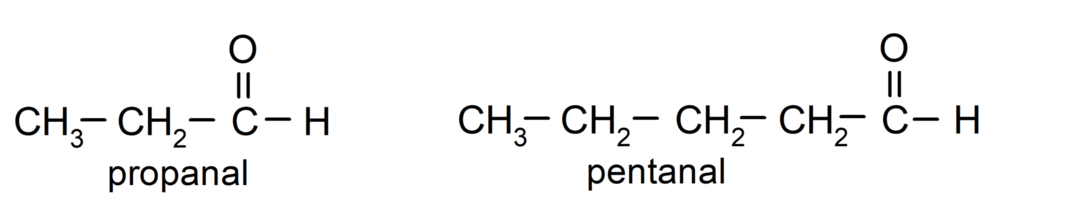
Ако се алдехид састоји од неколико угљеничних ланаца, односно има гране, као главни ланац се бира угљенични ланац са највећим бројем атома угљеника. Остали ланци су именовани као супституентске групе, а позиција сваког супституента је одабрана тако да заузима најмањи могући број у ланцу. Поред тога, атоми угљеника почињу да се броје почевши од краја који има карбонилну групу. На пример:
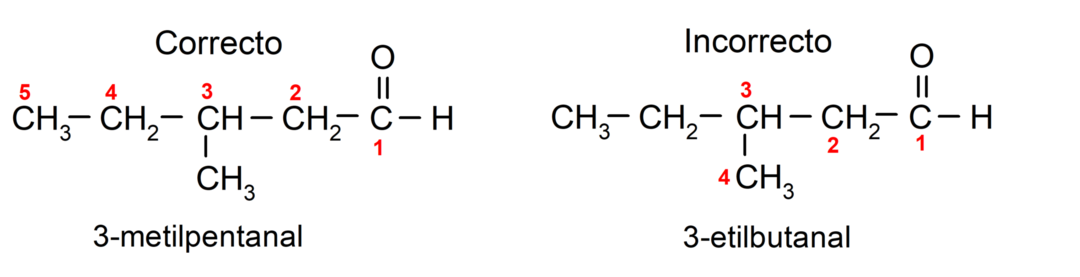
Алдехиди који имају две карбонилне групе се именују помоћу суфикса -диал. На пример:
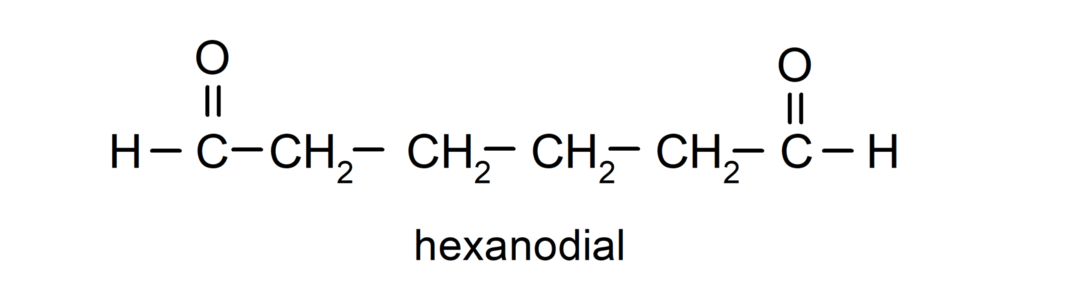
Кетонска номенклатура
Према Међународној унији за чисту и примењену хемију (ИУПАЦ), кетони се именују помоћу префикса који означавају број угљеника у ланцу угљеника.
С друге стране, назив ацетона пише се суфиксом -оне, којем претходи број који означава положај карбонилне групе у ланцу угљеника. Положај карбонилне групе треба изабрати на такав начин да одговара најмањој могућој нумерацији. На пример:
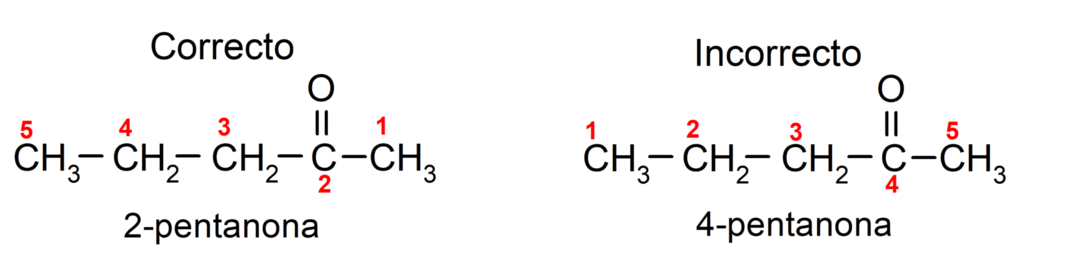
Да именујемо кетон који се састоји од неколико угљеничних ланаца, односно са гранама, бирамо као главни ланац, угљенични ланац са највећим бројем атома угљеника и који садржи групу карбонил. Остали ланци су именовани као супституентске групе. На пример:
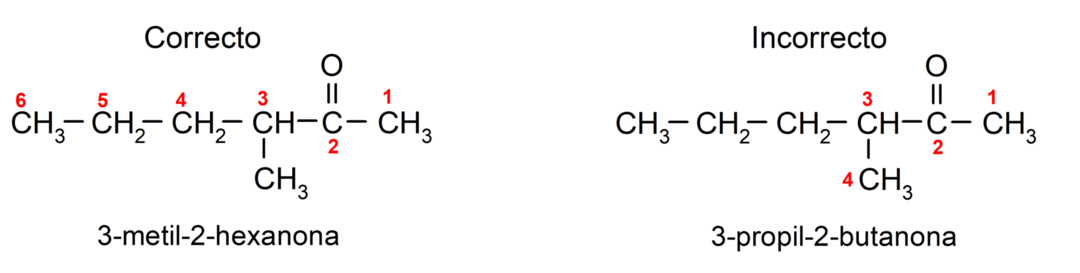
Постоје кетони који имају две карбонилне групе, зову се диони. На пример:
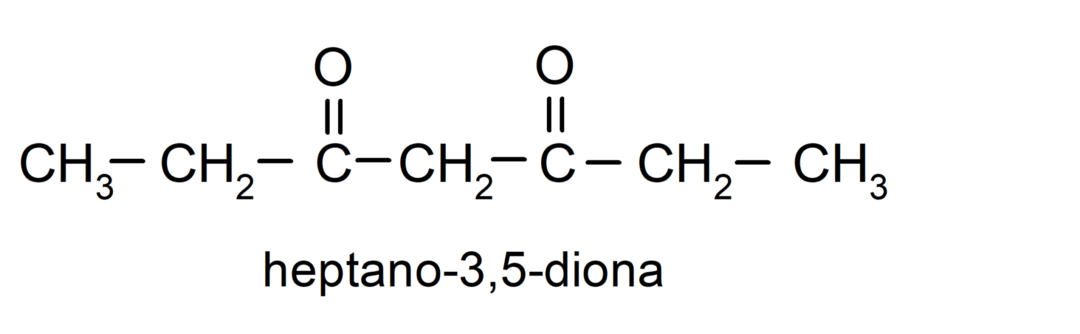
Примери алдехида
- метанал (формалдехид)
- етанал (ацеталдехид)
- пропанал (пропалдехид)
- бутанал
- пентанал
- хексанал
- 3-бромоциклопентанкарбалдехид
- циклохексанкарбалдехид
- бензалдехид
- 4,4-диметилпентанал
- 2-хидрокси-бутанал
- 2-хидрокси-2-метил-бутанал
- 2,3-диметилпентанал
- пентанедијални
- 4-хидрокси-3-метоксибензалдехид
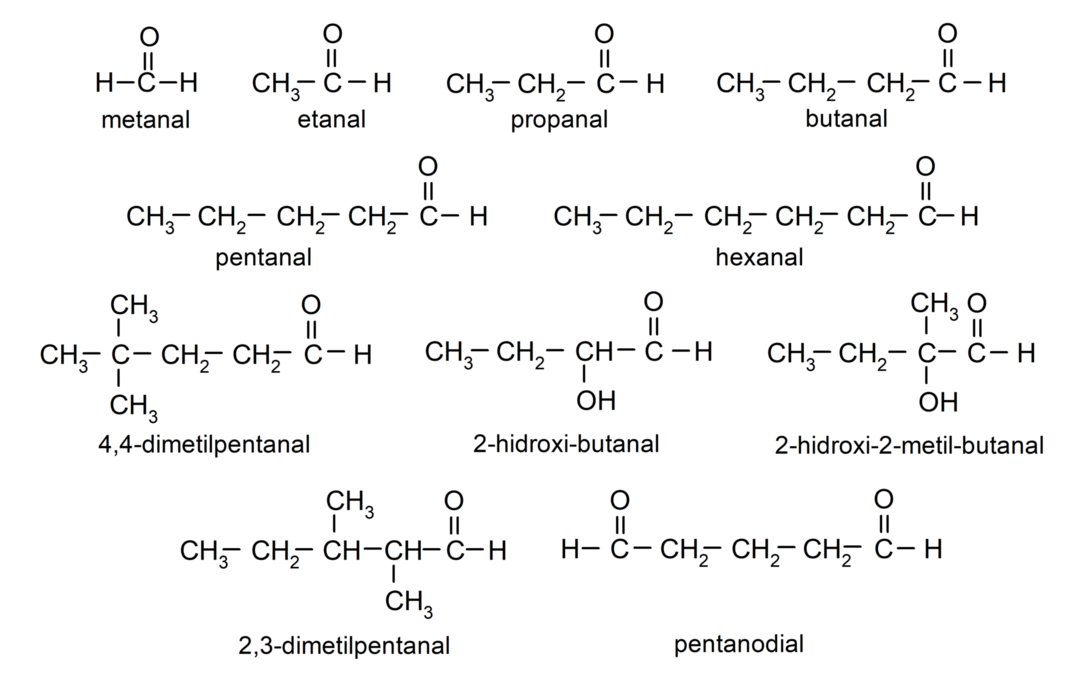
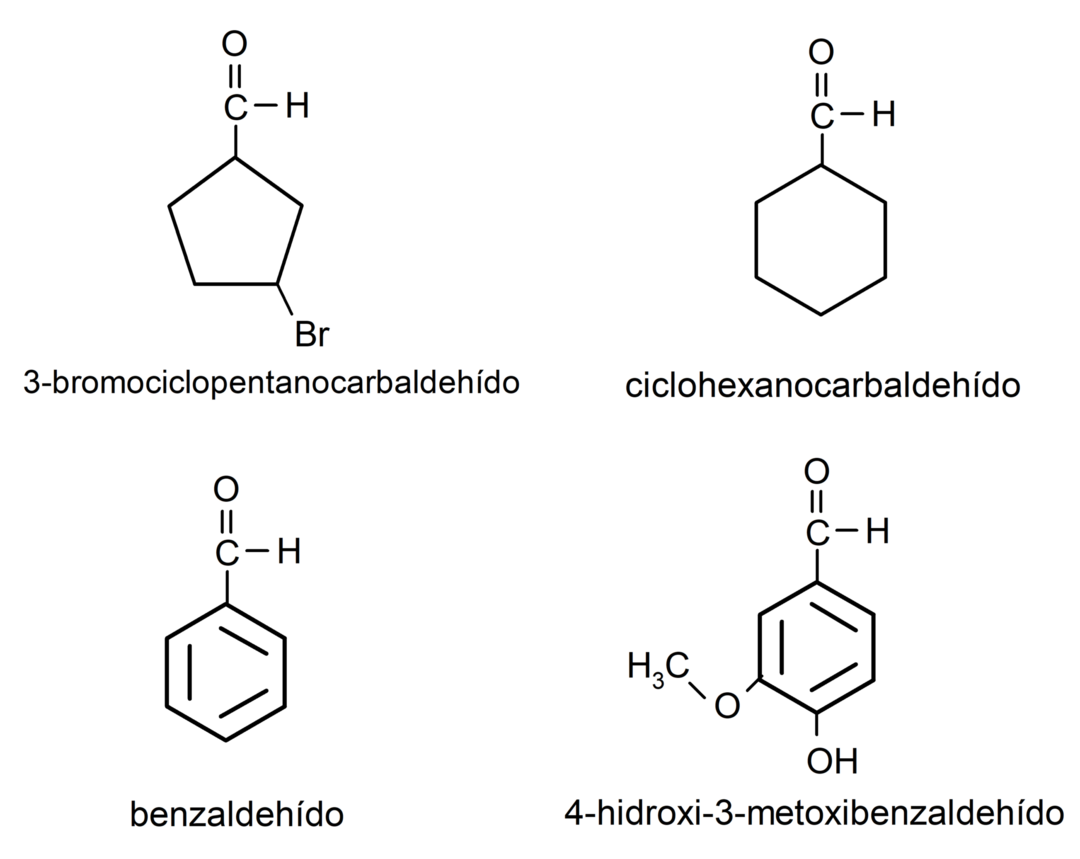
Примери кетона
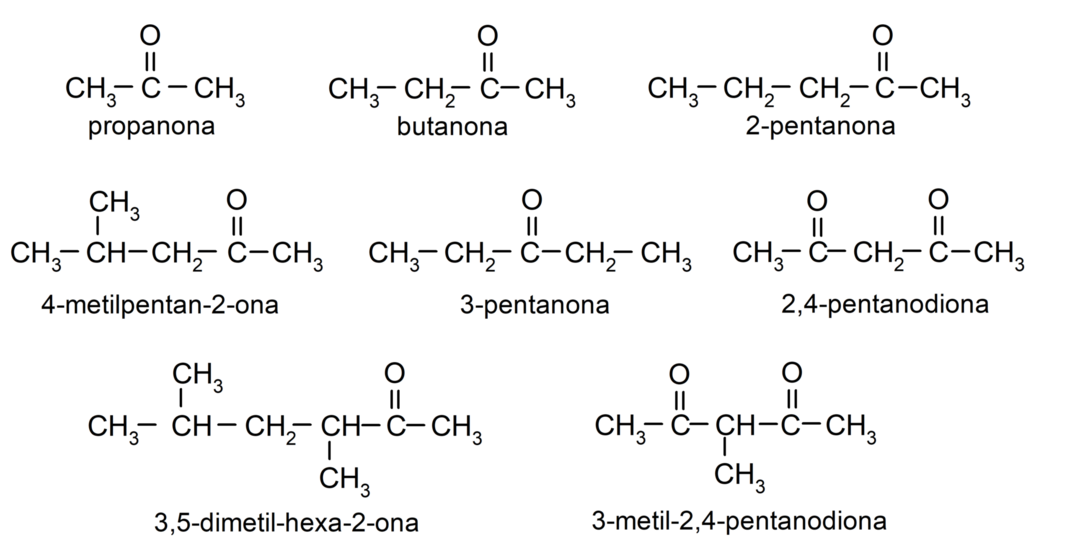
- пропанон (ацетон)
- бутанон
- 2-пентанон
- 4-метилпентан-2-он
- 3-метилциклохексанон
- циклохексилметилкетон
- 3,4 диметил-хексан-2-он
- етил фенил кетон
- 2,4-пентандион
- циклохексанона
- 3-пентанон
- 3-метил-2,4-пентандион
- 1-фенилпропанон
- циклопентанон
- дифенил кетон
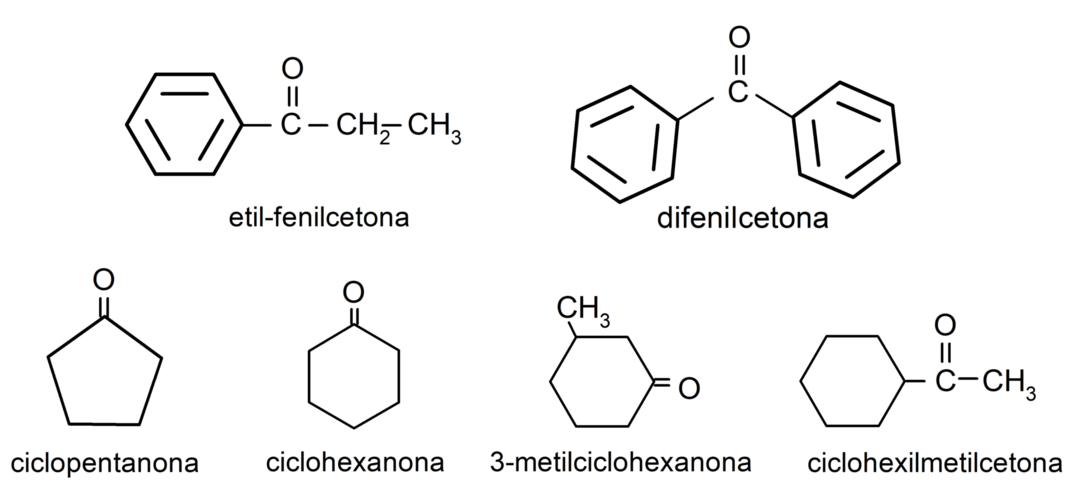
Употреба алдехида у свакодневном животу
Неке употребе алдехида су:
- Користе се за производњу растварача, боја, парфема, смола и есенција.
- Користе се као конзерванси у козметичким производима, биолошким узорцима и лешевима. Формалдехид се највише користи у ове сврхе.
- Користе се за производњу пластике, која омогућава замену металних делова у аутомобилској индустрији.
- Користе се као ароме за неке намирнице.
- Користе се као дезинфекциона средства.
- Коришћени су за прављење неких експлозива, као што је пентаеритритол тетранитрат (ТНПЕ).
Употреба кетона у свакодневном животу
Неке употребе кетона су:
- Користе се у производњи растварача. Посебно се ацетон широко користи за уклањање боја и лакова.
- Користе се у производњи неких гума и мазива.
- Користе се за производњу боја, лакова и лакова.
- Користе се за производњу лекова и козметике.
Токсичност алдехида и кетона
- Алдехиди. Контакт са алдехидима изазива иритацију коже, очију и респираторног тракта. Поред тога, изложеност алдехидима је повезана са болестима као што су рак, контактни дерматитис, јетре и неуродегенеративне болести. Формалдехид, на пример, СЗО (Светска здравствена организација) сматра канцерогеним једињењем.
- кетони. Поновљено излагање кетонима може изазвати оштећење централног нервног система. То може довести до губитка памћења, слабости, болова у мишићима и грчева. Поред тога, ако кожа дође у контакт са кетонима, долази до сувоће и пукотина. С друге стране, ако се кетони удишу, долази до иритације респираторног тракта и кашља.
Референце
- Ллоренс Молина, ЈА. (2018). “Алдехиди и кетони: неки примери.” http://hdl.handle.net/
- Габријел Пинто Кањон, Мануела Мартин Санчез, Хосе Марија Ернандез Ернандез, Марија Тереза Мартин Санчез (2015) “Толленсов реагенс: од идентификације алдехида до њихове употребе у нанотехнологији. Историјски аспекти и дидактичке примене.”Вол. 111 бр. 3. Краљевско шпанско друштво за хемију.
- Вилијам Бауер, млађи (2000) «Метакрилна киселина и деривати» у Уллманновој Енциклопедији индустријске хемије 2002, Вилеи-ВЦХ, Веинхеим. ДОИ: 10.1002/14356007.а16_441.
- „Они откривају нови механизам токсичности у групи канцерогених једињења која потичу из исхране и животне средине“ (2022) У: ввв.цоницет.гов.ар Доступна у: https://www.conicet.gov.ar/ Приступ: 20. јуна 2023.
Пратите са:
- Алцохолс
- Шећери
- Алканес



