30 Примери алдехида
Примери / / November 06, 2023
Тхе алдехиди су органска једињења који су формирани од угљеничног ланца који има закачену терминалну карбонилну групу (= Ц = О) (налази се на једном крају молекула), који је заузврат везан за атом водоника.
Веома чести алдехиди су метанал (формалдехид), етанал (ацеталдехид) и пропанал (пропалдехид).

Нека од ових једињења су присутна у природи, на пример, ванилин или ванилин је природни алдехид који чини главну арому ваниле.
- Такође погледајте: Алдехиди и кетони
Номенклатура алдехида
Алдехиди се могу именовати према правилима номенклатуре које је успоставила Међународна унија чисте и примењене хемије (ИУПАЦ).
За именовање алдехида користе се префикси који означавају број атома угљеника које је ланац угљеника везао за карбонилну групу. Карбонилна група се увек налази на једном крају угљеничног ланца, што значи да ће увек имати позицију један и није потребно назначити њену локацију у ланцу. Додатно, суфикс -ал се ставља на крај назива алдехида. Неки примери су:
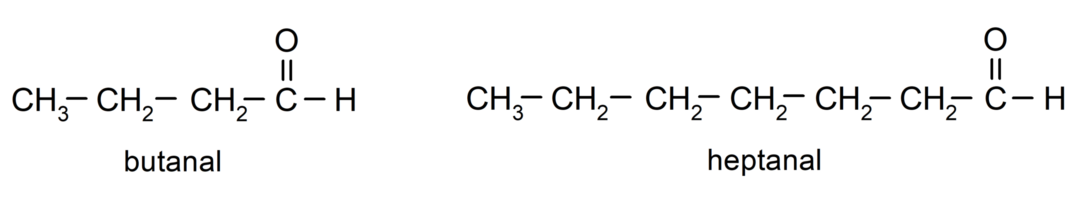
Ако је алдехид разгранат, односно састављен је од неколико угљеничних ланаца, тј главни ланац као ланац који има највећи број атома угљеника, а који такође садржи групу карбонил. Остали ланци су именовани као супституентске групе.
Штавише, свака супституентска група мора бити одабрана тако да њена позиција заузима најмањи могући број у главном угљениковом ланцу. С друге стране, атоми угљеника главног ланца почињу да се броје на крају који садржи карбонилну групу. Неки примери су:
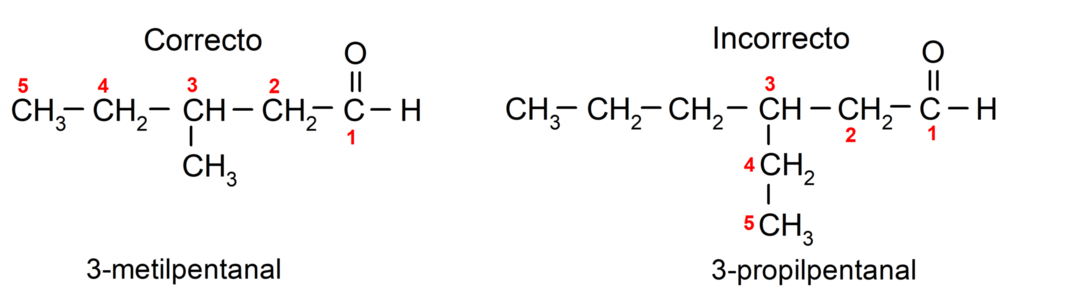
Ако алдехид делује као супституент у молекулу, јер је такође састављен од група функције вишег приоритета, као што су киселине и естри, тада се алдехидна група назива као -око. На пример:

Ако алдехид има неколико карбонилних група, он се именује помоћу префикса који означавају број ових група, диал (две карбонил групе), триал (три карбонил групе) итд. На пример:
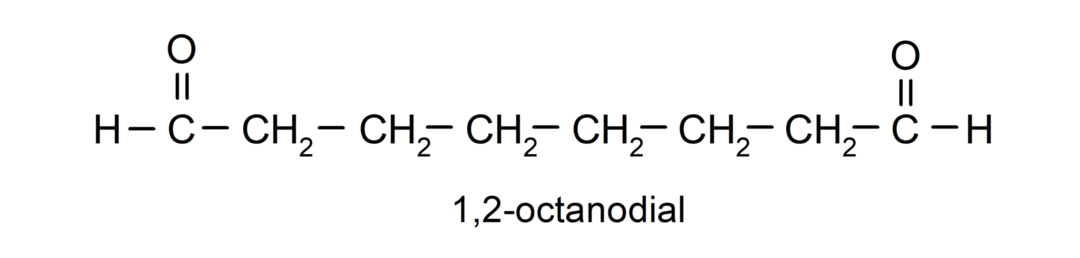
Када је карбонил група повезана са циклусом, алдехиди се називају термином карбалдехид. На пример:

Физичка својства алдехида
Алдехиди обично имају неку варијацију истог физичког својства. Ово се дешава зато што физичка својства алдехида зависе од тога како се формира угљенични ланац који је везан за карбонилну групу.
Нека физичка својства алдехида су:
- Растворљивост. Растворљивост алдехида у води зависи од количине атоми који има угљенични ланац. Алдехиди са краћим угљеничним ланцима (до око пет атома угљеника) су растворљиви у води. Алдехиди са угљеничним ланцима од много атома угљеника нису растворљиви у води. Метанал и етанал су веома растворљиви у води.
- Густина. Генерално, алдехиди су једињења која су мање густа од воде.
- Стање агрегације. Алдехиди састављени од једног и два атома угљеника су гасови, они који садрже између три и дванаест атома угљеника су течности, а они састављени од више од дванаест атома угљеника су чврсти.
- Мирис. Неки алдехиди имају иритирајући мирис, док други имају пријатан мирис.
- Поларитет. Карбонилна група им даје поларитет.
- Тачка кључања. Имају више тачке кључања од алкана сличне молекулске тежине, а имају ниже тачке кључања од карбоксилних киселина и алкохола упоредиве молекулске тежине.
Хемијска својства алдехида
Нека од хемијских својстава алдехида су:
Алдехиди се оксидују када реагују са Толленсовим, Бенедиктовим и Фелинговим реагенсима. да би се формирала одговарајућа карбоксилна киселина. Формирана киселина имаће исти број угљеника у ланцу угљеника као и алдехид од којег је настала. На пример:
- Оксидација Толленсовим реагенсом (комплекс амонијачног сребра у базичном раствору, [Аг (НХ3)2]+). Ова реакција производи одговарајућу киселину и метално сребро.

- Оксидација са Бенедиктовим и Фелинговим реагенсом (алкални раствори бакар (ИИ) сулфата (ЦуСО4) са различитим саставима). Ова реакција производи одговарајућу киселину и бакров оксид (Цу2ИЛИ).

Они пролазе кроз реакције нуклеофилне адиције, где су нуклеофили додати карбонилној групи алдехида. Неки примери су:
- реакције адиције алкохоли на карбонилну групу алдехида да би се формирали ацетали и хемиацетали.
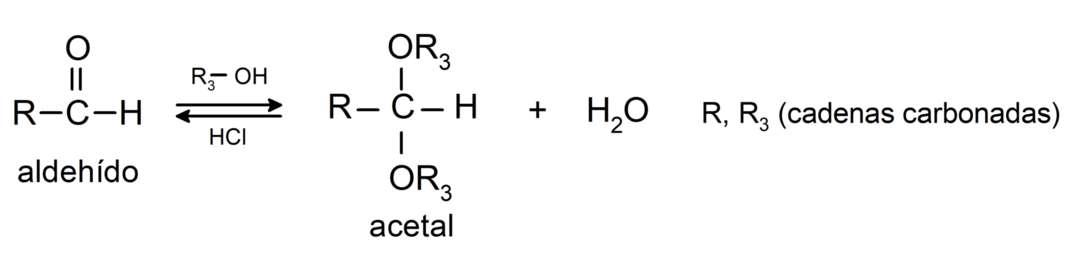
- реакције адиције амини примарно карбонилној групи.

- Реакције додавања цијановодоничне киселине (ХЦН), где се формирају цијанохидрини или цијанохидрини.

Они пролазе кроз реакције кондензације алдола. У овој врсти реакције, два алдехида се кондензују и формирају алдол. То су реакције које се јављају са натријум хидроксидом (НаОХ). На пример:
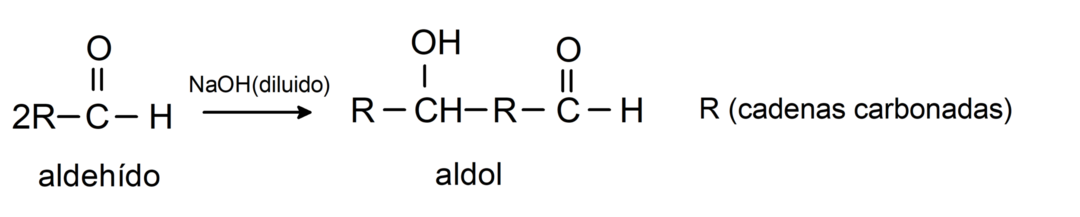
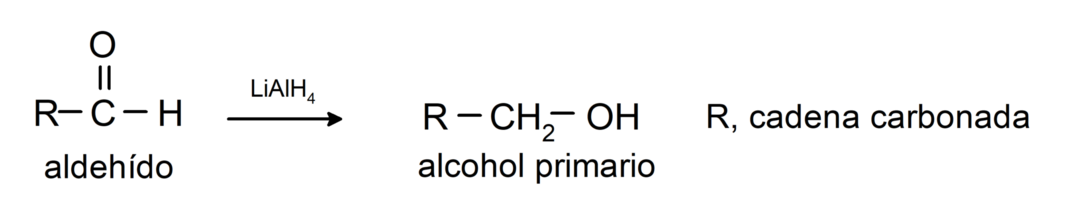
Они пролазе кроз редукционе реакције на примарне алкохоле. У присуству натријум борохидрида (НаБХ4) и литијум алуминијум хидрида (ЛиАлХ4) или каталитичком хидрогенацијом, редукују се у примарне алкохоле. На пример:
Примери алдехида
- метанал (формалдехид)
- етанал (ацеталдехид)
- пропанал (пропалдехид)
- бутанал
- пентанал
- ванилин
- цинамалдехид
- пропенални
- бензалдехид
- хексанал
- 3-бромоциклопентанкарбалдехид
- циклохексанкарбалдехид
- 4,4-диметилпентанал
- 2-хидрокси-бутанал
- 2-хидрокси-2-метил-бутанал
- 2,3-диметилпентанал
- пентанедијални
- циклопентанкарбалдехид
- изобутанал
- 2-хлоро-бутанал

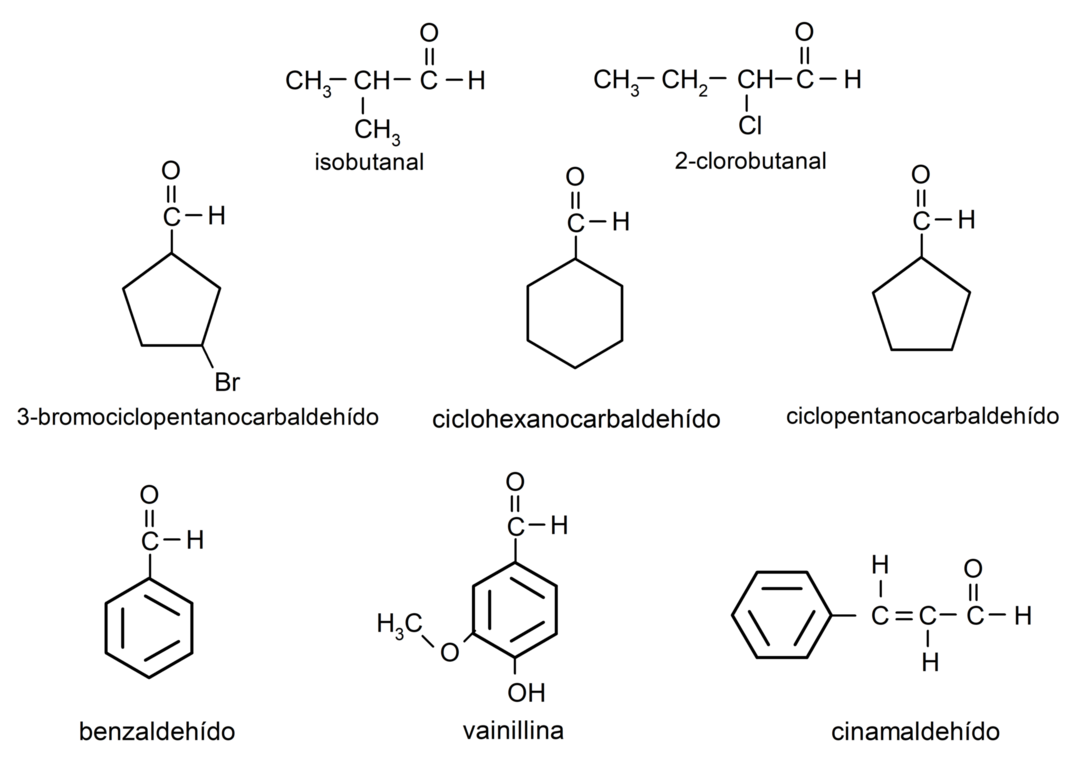
Алдехиди у природи
Неки алдехиди присутни у природи су:
- Бензалдехид, компонента бадема.
- Циметалдехид, компонента која даје мирис есенције цимета.
- Ванилин, компонента која ванили даје њен укус.
С друге стране, један од облика глукозе, отворени облик, има алдехидну функционалну групу.
Верује се да ацеталдехид, који се формира као међупроизвод у метаболизму алкохола, изазива симптоме мамурлука када се интоксицира алкохолом.
Употреба алдехида
Неке од главних употреба алдехида су:
- Користе се у производњи растварача, боја, козметичких производа и есенција.
- Користе се у производњи смола. Бакелит је направљен од формалдехида и је смола која веома добро функционише као електрични изолатор.
- Коришћени су као седативи. Паралдехид је коришћен као седатив и хипнотик, иако је сада ван употребе због свог непријатног мириса.
- Користе се као конзерванси за биолошке узорке и лешеве. Формалдехид се широко користи у овом смислу.
- Користе се као ароме за храну. Пример је ванилин, који се користи за давање десерта ароме ваниле.
- Користе се као дезинфекциона средства.
Опасности од алдехида
Неколико алдехида се сматра канцерогеним, на пример, формалдехид је проглашен канцерогеним једињењем према СЗО (Светска здравствена организација).
Излагање и контакт са многим алдехидима изазива иритацију коже, очију и респираторног тракта. С друге стране, изазива контактни дерматитис и обољења јетре.
Референце
- Соломонс, Т.В. Грахам и Марија Кристина Сангинес Францини (1985). “органска хемија” Мексико, Д.Ф.: Лимуса.
- Витен, К. В., Гејли, К. Д., Давис, Р. Е., де Сандовал, М. Т. ДО. О., & Мурадас, Р. М. г. (1992). “Општа хемија" (стр. 108-117). МцГрав-Хилл.
- Артеага, П. М. (2017). “Кетони и алдехиди” Научни научни гласник Припремне школе бр. 3, 4(8).
Пратите са:
- Шећери
- Хидрациди
- Етил алкохол
- Органска и неорганска једињења



