Карактеристике лантанида
Хемија / / July 04, 2021
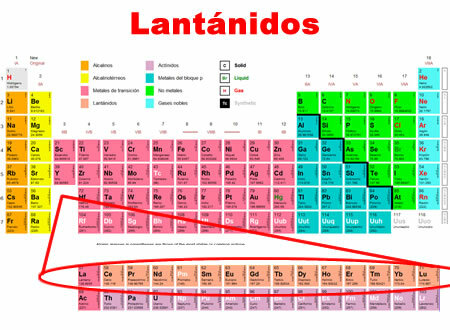
Лантаниди су хемијски елементи који се крећу од Лантана до Лутеција. Они деле заједничке карактеристике, за које су сврстани у посебну категорију на дну периодног система.
Главне карактеристике лантанида:
- Они се налазе у периоду 6 периодног система.
- Обухватају 15 елемената, од 57 до 71.
- Они деле структуру лантана, коме се додаје ниво енергије ф, који је мање хемијски реактиван.
- Названи су ретким земљама, јер се у природном стању увек комбинују да би створили оксиде.
- Неких је релативно пуно.
- Иако имају променљиве валенције, већина има валенције +3.
- Како се његов атомски број повећава, његов радијус се смањује.
- Сви имају сјајни метални изглед.
Индивидуалне карактеристике лантанида:
Лантан (Ла).
- Атомски број 57
- Атомска тежина: 139
- Чврсто стање
- Изглед: металик, сребрно бела
- Валенциас: +3
- Тачка топљења: 920 ° Ц
- Тачка кључања: 3457 ° Ц
Откривен је 1839. У индустрији се користи у легурама са другим лантанидима за израду лакших каменаца; у оптици се користи за оптичке наочаре. Такође се користи за водоничне спужве, које садрже гасове. У медицини се користи у облику лантановог карбоната за лечење бубрежне инсуфицијенције, јер има афинитет за мешање са фостатима, смањујући хиперфосфемију.
Церијум (Це)
- Атомски број 58
- Атомска тежина: 140
- Стање: Меко чврсто
- Изглед: металик, сребрно сива, налик гвожђу
- Валенсија: +3, +4
- Тачка топљења: 798 ° Ц
- Тачка кључања: 3426 ° Ц
Откривен је 1803. године. То је најзаступљенији лантанид. Од њега се израђују катализатори, углавном за аутомобиле (катализатори) и за крековање уља. У оксидном облику користи се за полирање наочара и сочива. Иако нема познате биолошке функције, у медицини се користи у масти од опекотина.
Празеодимијум (Пр)
- Атомски број 59
- Атомска тежина: 144
- Стање: Меко чврсто
- Изглед: металик, сребрно бела
- Валенциас: +3
- Тачка топљења: 931 ° Ц
- Тачка кључања: 3520 ° Ц
Откривен је 1841. године, а изолован 1885. године. У индустрији се користи у легурама са магнезијумом за израду авионских мотора; Користи се за добијање стакла и емајла жуте боје. Легуре никла имају магнетна својства. Реагује са халогенима дајући флуориде, хлориде, бромиде и јодиде.
Неодимијум (Нд)
- Атомски број 60
- Атомска тежина: 139
- Чврсто стање
- Изглед: металик, сребрно бела
- Валенциас: +3
- Тачка топљења: 1024 ° Ц
- Тачка кључања: 3100 ° Ц
Откривен је 1885. године, када је изолован прасеодим; неодим је изолован до 1925. То је један од најреактивнијих лантанида. У индустрији се користи за бојење стакла и емајла. Због своје способности да апсорбује светлост, користи се у астрономији за стварање кристала помоћу којих су калибрисани инфрацрвени спектрометри и филтери. Једна од његових главних примена је израда магнета високог магнетног интензитета. Ови магнети се користе за прецизне инструменте, попут оних који се користе у рачунарским чврстим дисковима, као и за неке звучнике танког формата.
Прометијум (Пм)
- Атомски број 61
- Атомска тежина: 145
- Чврсто стање
- Изглед:?
- Валенциас: +3
- Тачка топљења: 1100 ° Ц
- Тачка кључања: 3000 ° Ц
Његово постојање било је предвиђено 1902, али се могло доказати тек 1944. Овај лантанид се у природи не налази, јер је извор његовог добијања и проучавања фисије уранијума. Када се уранијум дели у нуклеарном реактору, један од атома који се добијају из ове атомске сепарације је прометхијум. Има радиоактивне карактеристике које му дају фосфоресценцију, а користи се за калибраторе и нуклеарне батерије које се користе у свемирским летелицама.
Самаријум (См)
- Атомски број 62
- Атомска тежина: 150
- Чврсто стање
- Изглед: металик, сребрно бела
- Валенциас: +3
- Тачка топљења: 1072 ° Ц
- Тачка кључања: 1803 ° Ц
Откривен је 1853. године, а изолован 1879. године. Има неколико изотопа, а најмање два су радиоактивна. У индустрији се користи у оптици за израду кристала који апсорбују инфрацрвену светлост. Такође се користи као катализатор за добијање алкохола и као елемент у неким флуоресцентним лампама и телевизорима. У здравственом смислу, ако се удише (као што је оксид који се користи за полирање кристала), може изазвати плућне емболије или утицати на јетру. Радиоактивни изотопи се користе у радиотерапији терминално болесних пацијената.
Еуропиум (Еу)
- Атомски број 63
- Атомска тежина: 152
- Чврсто стање
- Изглед: металик, сребрно бела
- Валенциас: +2, +3
- Тачка топљења: 826 ° Ц
- Тачка кључања: 1527 ° Ц
Откривен је 1890. Најреактивнији је од лантанида. Коришћен је у флуоресцентним лампама и телевизорима, међутим ако изазива плућну емболију удисање или оштећење јетре ако се акумулира у људском телу, готово да нема индустријску употребу. У атомским истраживањима се користи јер апсорбује неутроне.
Гадолинијум (Гд)
- Атомски број 64
- Атомска тежина: 157
- Чврсто стање
- Изглед: металик, сребрно бела
- Валенциас: +3
- Тачка топљења: 1312 ° Ц
- Тачка кључања: 3250 ° Ц
Гадолинијум има мало употреба, од којих је главна магнетно индустријско хлађење, јер повећава своја магнетна својства на ниским температурама; али како ова врста хладњака захтева употребу арсена, они се не користе у домаћем хлађењу. У медицини се користи као контрастно средство за магнетно-нуклеарну резонанцу.
Тербијум (Тб)
- Атомски број 65
- Атомска тежина: 159
- Чврсто стање
- Изглед: металик, сребрно бела
- Валенциас: +4
- Тачка топљења: 1356 ° Ц
- Тачка кључања: 3230 ° Ц
Откривен је 1843. године, а изолован 1905. године. Веома је важан у електронској индустрији, јер је један од елемената који се користе за израду полупроводника. Друга употреба је израда флуоресцентних цеви и сликовних цеви. Такође се користи као катализатор у горивим ћелијама. Иако нема биолошке функције, његово удисање или улазак у људско тело има токсичне ефекте, углавном утичући на јетру.
Диспрозијум (Ди)
- Атомски број 66
- Атомска тежина: 162,5
- Чврсто стање
- Изглед: металик, сребрно бела
- Валенциас: +2, +3
- Тачка топљења: 1407 ° Ц
- Тачка кључања: 2567 ° Ц
Откривен је 1843. године, а изолован 1905. године. Веома је важан у електронској индустрији, јер је један од елемената који се користе за израду полупроводника. Друга употреба је израда флуоресцентних цеви и сликовних цеви. Такође се користи као катализатор у горивим ћелијама. Иако нема биолошке функције, његово удисање или улазак у људско тело има токсичне ефекте, углавном утичући на јетру.
Холмијум (Хо)
- Атомски број 67
- Атомска тежина: 166
- Чврсто стање
- Изглед: металик, сребрно бела
- Валенциас: +3
- Тачка топљења: 1474 ° Ц
- Тачка кључања: 2700 ° Ц
Откривен је 1878. године, а његово име потиче од града његовог открића, Стокхолма, на латинском Холмиа. Готово да нема практичну употребу; међутим, користи се у неким индустријама као катализатор хемијских реакција, као и за неке електронске компоненте. Такође се користи за промену фреквенције и интензитета ласерског зрака.
Ербијум (Ер)
- Атомски број 68
- Атомска тежина: 167
- Чврсто стање
- Изглед: металик, сребрно бела
- Валенциас: +3
- Тачка топљења: 1795 ° Ц
- Тачка кључања: 2863 ° Ц
Откривен је 1843. године. Користи се у нуклеарној индустрији као неутронски пуфер. У оксидном облику је боја за кристале, која им даје ружичасту нијансу; Ови кристали се користе у оптици и накиту. Такође се користи за израду оптичких влакана.
Тулијум (Тм)
- Атомски број 69
- Атомска тежина: 167
- Чврсто стање
- Изглед: металик, сребрно бела
- Валенциас: +3
- Тачка топљења: 1545 ° Ц
- Тачка кључања: 1947 ° Ц
Откривен је 1879. Упркос малој доступности, због радиоактивних карактеристика, његова главна употреба је као извор Кс-зрака у преносној опреми и за солид-стате ласере.
Итербијум (Иб)
- Атомски број 70
- Атомска тежина: 173
- Чврсто стање
- Изглед: металик, сребрно бела
- Валенциас: +3
- Тачка топљења: 824 ° Ц
- Тачка кључања: 1194 ° Ц
Откривен је 1878. године, а изолован 1907. године. Радиоактивни изотопи се користе за преносну рендгенску опрему која ради без електричне енергије. Такође се користи за побољшање челичних легура и повећање њихове отпорности, карактеристике која се користи у стоматологији, због побољшања механичких својстава челика. Са њом се мора поступати пажљиво, јер може изазвати иритацију и опекотине. Такође, када реагује са ваздухом, може изазвати експлозију или пожар.
Лутетиум (Лу)
- Атомски број 71
- Атомска тежина: 175
- Чврсто стање
- Изглед: металик, сребрно бела
- Валенциас: +3
- Тачка топљења: 1652 ° Ц
- Тачка кључања: 3402 ° Ц
Откривен је 1907. године. То је најмање заступљени хемијски елемент у земљиној кори. Упркос малој доступности, користи се за прераду уља и као катализатор за реакције органске хемије. Неки радиоактивни изотопи су такође тестирани за терапије зрачењем.
