20 Exempel på alkaner
Miscellanea / / July 04, 2021
De alkaner de är ett slags kolväten där ett variabelt antal kolatomer sammanfogas av enkelbindningar, som ett skelett, och varje kolatom är i sin tur kopplad till väteatomer, som så småningom kan ersättas med andra atomer eller funktionella grupper. Till exempel: kloroform, metan, oktan.
De molekylär formel av de öppna linjära kedjealkanerna är CnH2n + 2där C representerar kol, H representerar väte och n representerar antalet kolatomer. Alkaner är mättade kolväten, vilket innebär att de inte har dubbla eller trippelbindningar. För att namnge dem använder du ändelse "-Ano" efter att ha känt kolkedjan med hjälp av prefix motsvarande antalet kolatomer (et- (2), pro- (3), men- (4), pen- (5), hex- (6), hep- (7), etc).
Det kan tjäna dig:
Klassificering av alkaner
Inom alkanerna känns de vanligtvis igen två stora grupper: öppen kedja (även kallad acyklisk) och sluten kedja (eller cyklisk).
När föreningar med öppen kedja De utgör ingen substitution av väten som följer med varje kolatom, de kallas linjära alkaner: dessa är de enklaste alkanerna. När de presenterar en substitution av någon av sina väten med en eller flera kolkedjor kallas de grenade alkaner. De vanligaste substituenterna är etylgrupper (CH
3CH2-) och metyl (CH3-).För sin del finns det föreningar med en enda cykel i molekylen (monocyklisk) och andra med flera (polycykliska). De cykliska alkaner de kan vara homocykliska (de bildas med exklusivt ingripande av kolatomer) eller heterocykliska (i vilka andra atomer deltar, till exempel syre eller svavel).
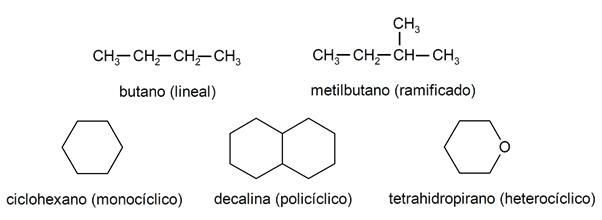
Fysiska egenskaper hos alkaner
I allmänhet, fysikaliska egenskaper av alkaner är konditionerade av molekylmassa (i sin tur kopplad till kolkedjans längd). De med det lägsta antalet kol är gasformig till temperatur miljö, är de från 5 till 18 kolatomer vätskoroch ovanför detta nummer är fast (liknar vax).
Att vara mindre tät än vatten, de tenderar att flyta på det. I allmänhet är alkaner olösliga i vatten och lösliga i organiska lösningsmedel.
Poängen med kokande och av fusion av alkaner beror på deras molekylär massa, det vill säga på längden på kolkedjan, även om de också beror många gånger på atomernas rumsliga arrangemang. Linjära och cykliska alkaner har högre kokpunkter än grenade.
Kemiska egenskaper hos alkaner
Alkaner kännetecknas av att vara kemiska föreningar av mycket dålig reaktivitet, varför de också är kända som "paraffiner" (på latin, parum affinis betyder "låg affinitet"). De är föreningar som har en mycket hög aktiveringsenergi när de är inblandade i kemiska reaktioner. Den viktigaste reaktionen som alkaner kan genomgå är förbränning genererar i närvaro av syre, värme, koldioxid och vatten.
Alkaner är grunden för en viktig mängd olika reaktioner associerade med industriella processer mycket viktigt, eftersom de är de mest traditionella bränslen. De framträder också som slutprodukter av biologiska processer som metanogen jäsning som utförs av vissa mikroorganismer.
Exempel på alkaner
Några exempel på alkaner (inklusive några välkända linjära och grenade) är:
- Kloroform (snyggt namn på triklormetan; CHCl3). Ångor av detta ämne brukade användas som bedövningsmedel. Det har avbrutits för detta ändamål eftersom det visade sig skada det organ viktigt, såsom levern eller njurarna. Dess användning idag är främst som lösningsmedel eller kylvätska.
- Metan (CH4). Det är den enklaste alkanen av alla: den består av endast en kolatom och fyra väteatomer. Det är en gas som förekommer naturligt genom nedbrytning av olika organiska substrat och är huvudkomponenten i naturgas. På senare tid har det erkänts som en av de gaser som bidrar mest till den så kallade växthuseffekten.
- Oktan (C8H18). Det är åtta kolalkanen och är av stor betydelse eftersom den bestämmer den slutliga kvaliteten på nafta, vilket är en blanda av olika kolväten. Denna kvalitet mäts med oktan- eller oktantalet på bränslet, som tar som referens en låg-detonerande (index 100) och en mycket detonerande (index 0).
- Hexan (C6H14). Det är ett viktigt lösningsmedel, inandning bör undvikas eftersom det är mycket giftigt.
- Butan (C4H10). Tillsammans med propan (C3H8), utgör så kallade flytande petroleumgaser (LPG), som bildas i gaspåsar under oljeutvinningsprocessen. För närvarande främjas ersättning av bensin eller diesel med LPG som bränsle eftersom det är av ett mer miljövänligt kolväte (det avger endast koldioxid och vatten under förbränningen).
- Icosano (C20H42). Det är tjugo-kol-alkanen (prefixet 'ico' betyder tjugo)
- Cyklopropan (C3H6). Tidigare användes det som bedövningsmedel
- n-heptan (C7H16). Det är den som tas som referens för nollpunkten för bensinoktanskalan, vilket skulle vara minst önskvärt, eftersom det brinner explosivt. Det erhålls från vissa hartser växter.
- 3-etyl-2,3-dimetylpentan (C9H20)
- 2-metylbutan (C5H12)
- 3-klor-4-n-propylheptan (C10H21Cl)
- 3,4,6-trimetylheptan (C10H22)
- 1-brom-2-fenyletan (C8H9Br)
- 3-etyl-4-metylhexan (C9H18)
- 5-isopropyl-3-metylnonan (C13H28)
- Kubansk (C8H8)
- 1-brompropan (C3H7Br)
- 3-metyl-5-n-propyloktan (C12H26)
- 5-n-butyl-4,7-dietyldekan (C18H28)
- 3,3-dimetyldekan (C12H26)

