Exempel på Charles's Law
Fysik / / November 13, 2021
Charles gaslag eller lag om konstant tryck, är en annan av gaslagarna, uttalad av Gay-Lussac, som släppte Jacques Charles verk, publicerad omkring 20 år innan.
Charles lag förutsäger beteendet hos en gasmassa när trycket förblir konstant och temperaturen och volymen varierar.
Karls lag sägs enligt följande:
Vid konstant tryck är volymen av en gas direkt proportionell mot förändringen i dess temperatur.
Konstant tryck: hänvisar till det faktum att trycket som gasen utövar på behållarens väggar inte kommer att variera under upplevelsen.
Volym: det är det upptagna utrymmet som gasen upptar, i allmänhet anses det vara en behållare med väggar som inte deformeras, och vars lock fungerar som en kolv.
Temperatur: Det är ökningen eller förlusten av värme som gasen genomgår under experimentet. Om temperaturen ökar ökar volymen. Om temperaturen sjunker minskar även volymen.
Algebraiskt uttrycks Charles's Law med följande formel:

Var:
V = gasvolym
T = gastemperatur
k = proportionalitetskonstant för den gasmassan.
Detta betyder att för en given gasmassa, vid konstant tryck, förhållandet mellan volymen och temperaturvariationer, kommer alltid att ha samma proportionalitetsförhållande, representerat av konstanten k:

Så när konstanten har bestämts kan vi beräkna något av de andra värdena från andra kända data:
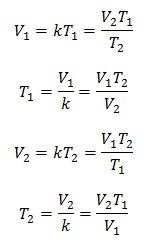
3 exempel på Charles's Law tillämpad på problem:
Exempel 1: Beräkna den nya volymen, om det i en behållare finns en gasmassa som upptar en volym på 1,3 liter, vid en temperatur av 280 K. Beräkna volymen när du når en temperatur på 303 K.
V1 = 1,3 l.
T1 = 280 K
V2 = ?
T2 = 303 K
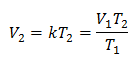
Ersättande värden:
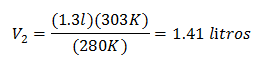
Den nya volymen vid 303 K är 1,41 liter.
Exempel 2. Om vi har en gas som upptar 2,4 liter vid 10 grader Celsius, beräkna sluttemperaturen, om den i slutet upptar 2,15 liter.
V1 = 2,4 l
T1 = 10 °C = 283 K
V2 = 2,15 l
T2 = ?
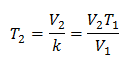
Ersättande värden:
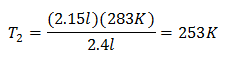
Den nya temperaturen är 253 K, vilket är lika med -20 ° C.
Exempel 3. Vi har en gas vars initiala temperatur är 328 K, dess slutvolym är 3,75 l och dess förhållandekonstant är 0,00885.
V1 = ?
T1 = 328 K
V2 = 3,75 l
T2 = ?
k = 0,00885
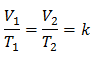
Ersättande värden:
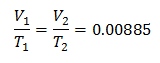
För att veta den initiala volymen:
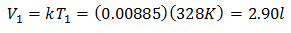
Den initiala volymen är 2,90 l.
För att veta sluttemperaturen:
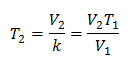
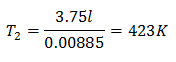
Den slutliga temperaturen blir 423 K, vilket är lika med 150 ° C.



