Exempel på nomenklatur för organiska föreningar
Kemi / / July 04, 2021
Organiska föreningar är molekyler vars egenskaper är att de bildas av en bas av kolmolekyler och väte, även känt som skelettet, och kombinerat med andra grundämnen, främst syre, kväve och svavel.
De IUPAC (International Union of Pure and Applied Chemistry, International Union of Pure and Applied Chemistry) har fastställt allmänna regler för klassificering och nomenklatur för organiska molekyler, av vilka vi förklarar de viktigaste.
Kolväten
Kolväten är de enklaste organiska molekylerna, som består av ett kolskelett och väteatomer. Det finns tre typer av kolväten:
Alkanes
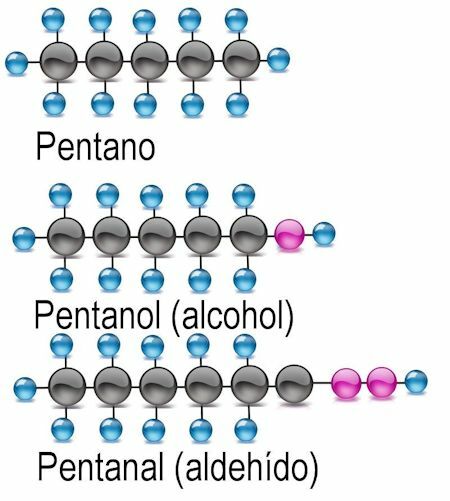
De är de enklaste, bildade av kolatomer förenade av enkla kovalenta bindningar till atomerna i väte, med den allmänna formuleringen H = 2n + 2, det vill säga väteatomerna är dubbelt så många väteatomer. kol, plus 2. Dess nomenklatur är formad med de numeriska prefixen met- för 1 kolatom, et- för 2, prop- för 3 och but- för 4; från 5 kolatomer används de vanliga prefixen pent-, hex-, hept-, oct-, etc. Till alla alkaner läggs änden -ano.
Exempel: CH4: metan; C2H6: etan; C4H10: butan; C6H14: hexan
Alkenes
De bildas av ett kolskelett där det finns en dubbelbindning mellan kolatomerna. Dess allmänna formel är H = 2n, det vill säga dess väteatomer är dubbelt så många kolatomer. Liksom alkaner använder de prefix som indikerar deras antal kolatomer, och i detta fall läggs änden -eno till. Dessutom, i molekyler med mer än tre kolatomer, kol där dubbelbindningen finns, börjar räkna från kolet närmast är.
Exempel: C2H4: eten; C3H6: propen; C4H8: buten, 2-buten; C6H12: Hexen, 2-hexen (dubbelbindning vid atom 2), 3-hexen (dubbelbindning vid atom 3).
Alkynes
Alkyner innehåller en trippelbindning vid sina kolatomer. Dess allmänna formel är H = 2n-2, vilket indikerar att molekylen kommer att innehålla två väteatomer mindre än dubbelt så många kolatomer. Till prefixet som anger antalet kol, läggs slutet -ino till. Som i fallet med alkener nämns kolet som innehåller trippelbindningen, räknat från det yttersta närmast det.
Exempel: C2H2: ethyne; C3H4: dricks; C4H6: butyne, 2-butyne; C6H12: Hexino, 2-hexino (trippelbindning vid atom 2), 3-hexyn (trippelbindning vid atom 3).
Funktionella grupper
Funktionella grupper är kombinationer av atomer som fungerar som en jon och ersätter en väteatom med formeln en alkan.
Radikaler
Alkanen utan väteatomen kallas Radical, och för att identifiera den läggs änden -ilo till:
Exempel CH4: metan - CH3+ metyl; C2H6: etan - C2H5+ etyl; C4H10: butan - C4H9+ butyl; C6H14: hexan - C6H13+ hexyl.
Kombination av kolväten
Ett av fallen som kan uppstå är att två eller flera kolväten kombineras i en molekyl. Kolvätena med vilka det kombineras kallas arborescenser. I dessa fall kommer baskolvätet att vara det med den längsta kedjan, och antalet kol var arborescenser hittas, följt av namnet på radikalen med änden -il, och sedan namnet på kolväten bas. Numret kommer att nämnas så många gånger som trädlinjerna fästa vid det. I det fall att arborescenserna är av samma radikal i olika kolatomer kommer siffrorna åtskilda med komma att nämnas, följt av ett bindestreck, namnet på radikalen, sedan antalet atomer där den andra radikalen är fäst, om någon, ett streck, namnet på radikalen och namnet på kolväten bas. Om det finns två radikaler fästa vid samma kolatom kommer antalet att nämnas två gånger. Om de är olika radikaler kommer det att nämnas en gång före namnet på varje radikal; om radikalerna är lika kommer antalet att nämnas två gånger. Vi kommer att börja med att nämna de enklaste arborescenserna först (de med minst mängd kol) och sedan de med den högsta mängden.
Exempel: En pentanmolekyl med två etanradikaler, bundna vid kol 2 och 3:
2,3-etylpentan. En oktanmolekyl, en propanradikal vid kol 6, metanradikaler vid kol 4 och 5 och etanradikaler bundna vid kol 2, 3 och 4: 4,5-metyl-2,3,4-etyl-6- propyl -oktan.
Alkoholfunktionell grupp
Den enklaste av de funktionella grupperna är alkohol, i vilken en väteatom ersätts med en hydroxylgrupp (OH). I dessa föreningar tillsätts änden -anol till namnet på radikalen. I förekommande fall bör kolatomen där den funktionella gruppen finns nämnas:
Exempel CH3OH: metanol: C2H5OH etanol; C4H9OH butanol eller 2-butanol; C6H13OH-hexanol, 2-hexanol (funktionell grupp vid atom 2), 3-hexanol (funktionell grupp vid atom 3).
Aldehyd funktionell grupp
I aldehyder byts väteatomen ut mot den funktionella gruppen -CHO. För att identifiera dem läggs änden -anal till och kolatomen där den funktionella gruppen finns nämns också:
Exempel CH3COH: metanal: C2H5Ethanal COH; C4H9COH butanal eller 2-butanal; C6H13COH-hexanal, 2-hexanal (funktionell grupp vid atom 2), 3-hexanal (funktionell grupp vid atom 3).
Syrafunktionell grupp
I organiska syror byts väteatomen ut mot den funktionella gruppen -COOH. För att identifiera dem nämns ordet syra och tillägget -anoic tillsätts och kolatomen där den funktionella gruppen finns nämns också:
Exempel CH3COOH: metansyra: C2H5COOH etansyra; C4H9COOH butansyra eller 2-butansyra; C6H13COH-hexansyra, 2-hexansyra (funktionell grupp vid atom 2), 3-hexansyra (funktionell grupp vid atom 3).

