50 ตัวอย่างของกรดและเบส
เบ็ดเตล็ด / / July 04, 2021
ในด้านของ เคมีเรียกว่า ฐาน (หรือ ไฮดรอกไซด์) กับสารที่เมื่อละลายในน้ำ จะปล่อยไฮดรอกซิลไอออน (OH–) และเรียกว่า กรด สารที่สามารถปล่อยโปรตอน (H+) ในสารละลายที่เป็นน้ำ ตัวอย่างเช่น: กรดซัลฟิวริก, กรดไนตริก, แคลเซียมไฮดรอกไซด์, โพแทสเซียมไฮดรอกไซด์.
การจำแนกกรดและเบส
ตามแนวโน้มที่จะแยกตัวออกเป็นไอออน กรดและเบสแบ่งออกเป็น:
กรดลดลงpH ของสารละลาย, เบส หรือ ด่าง ยกขึ้น. กรดแก่มักมีฤทธิ์กัดกร่อน สารบางชนิดละลายได้ดีกว่าในตัวกลางที่เป็นกรดหรือด่างเล็กน้อย
ตัวอย่างของกรด
กรดบางชนิดที่รู้จักคือ:
- กรดซัลฟิวริก (H2SW4). เป็นกรดแก่ที่มีประโยชน์มากมาย โดยเฉพาะใน in อุตสาหกรรมหนัก, กัดกร่อนและระคายเคืองมาก. เมื่อเจือจางแล้วจะปล่อยความร้อนออกมามาก จึงต้องจัดการ (เช่น กรดแก่อื่นๆ) ด้วยความระมัดระวัง มันออกซิไดซ์อย่างเข้มข้น
- กรดไฮโดรคลอริก (HCl). แม้ว่าจะเป็นกรดแก่ แต่ก็มีอยู่ในร่างกายมนุษย์ โดยเฉพาะในกระเพาะอาหาร ซึ่งมีบทบาทสำคัญในกระบวนการย่อยอาหาร ส่วนเกินทำให้เกิดอาการเสียดท้อง
- กรดฟอสฟอริก (H3ป4). กรดนี้เป็นส่วนประกอบทั่วไปในเครื่องดื่มอัดลม ไม่ควรบริโภคเครื่องดื่มดังกล่าวเป็นประจำเนื่องจากผลกระทบด้านลบของกรดนี้ต่อการเผาผลาญแคลเซียมซึ่งส่งผลกระทบ กระดูก และฟันโดยเฉพาะ
- กรดไนตริก (HNO3). เป็นกรดแก่ที่เป็นที่รู้จัก ใช้ทำระเบิดและปุ๋ยไนโตรเจน
- กรดเปอร์คลอริก (HClO4). เป็นกรดแก่ ของเหลว a อุณหภูมิ สิ่งแวดล้อม มันเป็นหนึ่งในการออกซิไดซ์มากที่สุด
- ไฮโดรเจนซัลไฟด์ (H2ส). เป็นสารก๊าซที่มีกลิ่นแรงและไม่พึงประสงค์ เป็นพิษในระดับความเข้มข้นสูง มีการใช้งานทางอุตสาหกรรมมากมาย
- กรดไรโบนิวคลีอิก. เป็นส่วนประกอบสำคัญของไรโบโซม ซึ่งจำเป็นสำหรับกระบวนการสังเคราะห์โปรตีนจากกรดดีออกซีไรโบนิวคลีอิกทั่วโลก
- กรดอะซิทิลซาลิไซลิก. เป็นกรดอินทรีย์ที่สำคัญมาก มีคุณสมบัติในการระงับปวดและต้านการอักเสบ เป็นพื้นฐานของแอสไพริน
- กรดแลคติก. มันมาจากการสลายตัวของกลูโคสในระหว่างการออกกำลังกายแบบไม่ใช้ออกซิเจนที่มีความเข้มข้นสูงและระยะเวลาสั้น ภายใต้สภาวะปกติ กรดแลคติคนี้จะถูกนำกลับมาใช้ใหม่ แต่ถ้าสะสมเข้าไปจะทำให้เกิดความเสียหายต่อเส้นใยกล้ามเนื้อ ซึ่งทำให้เป็นตะคริวได้
- กรดอัลลิลิก. เป็นกรดที่มีอยู่ในผักเช่นกระเทียมหรือหัวหอมซึ่งได้มาจากสารตั้งต้นที่มีอยู่ในสายพันธุ์ดังกล่าว ได้แก่ อัลลิซิน เป็นสารฆ่าเชื้อโรคและสารต้านอนุมูลอิสระ
- กรดเรติโนอิก. ใช้ทาเฉพาะที่ยับยั้ง keratinization ใช้ในครีมต่อต้านสิวและริ้วรอยของผิว ควรใช้ภายใต้การดูแลของแพทย์
- กรดบิวทิริก. เป็นผลิตภัณฑ์สุดท้ายของ การหมัก ของคาร์โบไฮเดรตบางชนิดที่ดำเนินการโดย จุลินทรีย์ ของกระเพาะหมัก มันมักจะเป็นส่วนหนึ่งของ ไขมัน สัตว์ในปริมาณน้อย
- กรดโพรพิโอนิก. เป็นสารกันบูดในอาหาร ใช้เพื่อป้องกันเชื้อราและแบคทีเรียเน่าเสียของผลิตภัณฑ์เบเกอรี่และอื่นๆ
- กรดเบนโซอิก. ใช้เป็นสารกันบูดที่เติมลงในผลิตภัณฑ์ต่างๆ (มายองเนส สินค้ากระป๋อง) มักอยู่ในรูปแบบของเกลือ (โซเดียมเบนโซเอต)
- กรดอะซิติก (CH3ซีโอเอช). เป็นสารกันบูดในอาหารที่ใช้กันอย่างแพร่หลายในบ้าน และยังใช้เป็นฐานสำหรับน้ำส้มสายชูและผักดอง เป็นส่วนประกอบส่วนใหญ่ของน้ำส้มสายชู
- กรดไฮโดรไอโอดิก (HI(ค)). เป็นกรดแก่ที่สามารถเพิ่มระดับไอโอดีนใน คุณออกไป.
- กรดซัคซินิก (C4โฮ6หรือ4). เป็นของแข็งผลึกที่ได้จากอำพัน สามารถเกิดขึ้นได้ในกระบวนการหมักไวน์และเบียร์
- กรดไฮโดรโบรมิก (HBr(ค)). เป็นกรดแก่ที่มีฤทธิ์กัดกร่อนมาก ปฏิกิริยากับเบสรุนแรงมาก และระคายเคืองมากด้วย ใช้ในอุตสาหกรรมเคมีและยา
- กรดซิตริก (C6โฮ8หรือ7) เป็นกรดอินทรีย์ที่อุดมสมบูรณ์ในผลไม้ เป็นสารต้านอนุมูลอิสระตามธรรมชาติ
- กรดออกซาลิก (H2ค2หรือ4). เป็นกรดอินทรีย์ที่พบได้ตามธรรมชาติใน พืช. ใช้ในการเลี้ยงผึ้งเพื่อควบคุมโรคในผึ้ง นอกจากนี้ยังใช้ในการผลิตผลิตภัณฑ์ทำความสะอาด ในอุตสาหกรรมสิ่งทอ และการใช้งานอื่นๆ
ตัวอย่างของฐาน
ฐานโลหะเป็นที่รู้จักกันทั่วไปว่า ไฮดรอกไซด์ ฐานบางส่วนคือ:
- โซเดียมไฮดรอกไซด์ (NaOH, โซดาไฟ). เป็นฐานที่แข็งแกร่งที่ใช้ในอุตสาหกรรมกระดาษและในการผลิตผงซักฟอก ในชีวิตประจำวันใช้เพื่อคลายท่อห้องน้ำและห้องครัว
- แมกนีเซียมไฮดรอกไซด์ (Mg (OH)2, น้ำนมแห่งแมกนีเซีย). เป็นฐานที่แข็งแกร่งซึ่งบางครั้งใช้เป็น ยาลดกรด หรือยาระบาย
- แคลเซียมไฮดรอกไซด์ (แคลิฟอร์เนีย (OH)2, มะนาว). หรือที่เรียกว่าปูนขาว ใช้ในอุตสาหกรรมโลหะและน้ำมัน นอกจากนี้ยังใช้ทำยาฆ่าแมลง ในอุตสาหกรรมน้ำตาลและนม เป็นต้น
- โพแทสเซียมไฮดรอกไซด์ (KOH). เป็นฐานที่แข็งแรงและมีฤทธิ์กัดกร่อนที่ใช้กันอย่างแพร่หลายในอุตสาหกรรมต่างๆ นิยมนำมาทำสบู่
- แบเรียมไฮดรอกไซด์ (Ba (OH)2). เนื่องจากมีความเป็นพิษจึงใช้ทำพิษ นอกจากนี้ยังใช้ในอุตสาหกรรมเซรามิก ในอุตสาหกรรมกระดาษ และในกระบวนการกลั่นน้ำตาล
- ไฮดรอกไซด์ของเหล็ก II หรือ III (Fe (OH)2 หรือเฟ (OH)3). มักถูกสร้างขึ้นโดยเป็นส่วนหนึ่งของอุตสาหกรรมโลหการ ใช้ในการผลิตสีรวมถึงการใช้งานอื่น ๆ
- แอมโมเนีย (NH3). เป็นก๊าซที่มีกลิ่นเฉพาะตัว ใช้ทำปุ๋ยและยาหลายชนิด เป็นอันตรายอย่างยิ่งหากสูดดมในปริมาณที่สูง
- สบู่. เป็นเกลือโซเดียมหรือโพแทสเซียม ใช้สำหรับสุขอนามัยส่วนบุคคลและทั่วไป
- ผงซักฟอก. นอกจากนี้ยังเป็นผลิตภัณฑ์ที่ใช้กันอย่างแพร่หลายเพื่อสุขอนามัย
- ควินิน. เป็นฐานธรรมชาติที่ผลิตโดยพืชบางชนิด มีคุณสมบัติลดไข้และยาแก้ปวด ในสมัยโบราณใช้รักษาโรคมาลาเรีย
- Aniline. เป็นสารประกอบที่เป็นพิษเมื่อกลืนกินหรือสูดดม ใช้ในอุตสาหกรรมยาง ในการผลิตสารกำจัดวัชพืชและวัตถุระเบิด เป็นต้น
- Guanine. เป็นหนึ่งในฐานไนโตรเจนที่เป็นส่วนหนึ่งของกรดนิวคลีอิก (DNA และ RNA)
- พีริมิดีน. เบสไนโตรเจนที่ประกอบเป็นกรดนิวคลีอิกได้มาจากไพริมิดีน
- ไซโตซีน. มันเป็นหนึ่งในฐานไนโตรเจนที่เป็นส่วนหนึ่งของ กรดนิวคลีอิก.
- อะดีนีน. เป็นหนึ่งในฐานไนโตรเจนที่เป็นส่วนหนึ่งของกรดนิวคลีอิก
- ซิงค์ไฮดรอกไซด์ (Zn (OH)2). เป็นสารแอมโฟเทอริก (สามารถทำหน้าที่เป็นทั้งกรดและเบส) เป็นสารพิษหากสัมผัสกับดวงตาหรือผิวหนัง ใช้ในกระบวนการผลิตแผ่นปิดแผลผ่าตัด
- คอปเปอร์ไฮดรอกไซด์ (Cu (OH)2). ใช้เป็นยาฆ่าเชื้อราและสีวัตถุเซรามิก นอกจากนี้ยังใช้เป็นตัวเร่งปฏิกิริยาสำหรับบางคน ปฏิกริยาเคมี.
- เซอร์โคเนียมไฮดรอกไซด์ IV (Zr (OH)4). ใช้ในอุตสาหกรรมเซรามิกและแก้ว
- เบริลเลียมไฮดรอกไซด์ (Be (OH)2). มีคุณสมบัติแอมโฟเทอริก ใช้ในอุตสาหกรรมเพื่อให้ได้โลหะเบริลเลียม เป็นสารที่มีความอุดมสมบูรณ์จำกัด
- อะลูมิเนียมไฮดรอกไซด์ (Al (OH)3, ยาลดกรด). มันถูกใช้ในยาเป็นยาลดกรดและเสริมวัคซีน
ทฤษฎีเกี่ยวกับกรดและเบส
แนวความคิดของเบสและกรดเปลี่ยนไปตามกาลเวลา มันเป็น อาร์เรเนียส ที่ร่างนิยามแรกขึ้นซึ่งนิยามกรดเป็นสารที่ให้ไอออน H ในสารละลายที่เป็นน้ำ+และถึงเบสเช่นสารที่ละลาย OH ไอออนในสารละลายในน้ำ–. ทฤษฎีของเขามีข้อ จำกัด บางประการเนื่องจากสารบางชนิด (เช่นแอมโมเนีย) ทำตัวเหมือนเบสโดยไม่ต้องมีอยู่ใน โมเลกุล สู่ไฮดรอกซิลไอออน
นอกจากนี้ Arrhenius ยังพิจารณาเฉพาะสารในตัวกลางที่เป็นน้ำเท่านั้น แต่ปฏิกิริยากรด-เบสก็เกิดขึ้นในตัวกลางอื่นด้วย การละลาย ไม่เป็นน้ำ ตัวแทนของกรดและเบสตามทฤษฎี Arrhenius คือ:
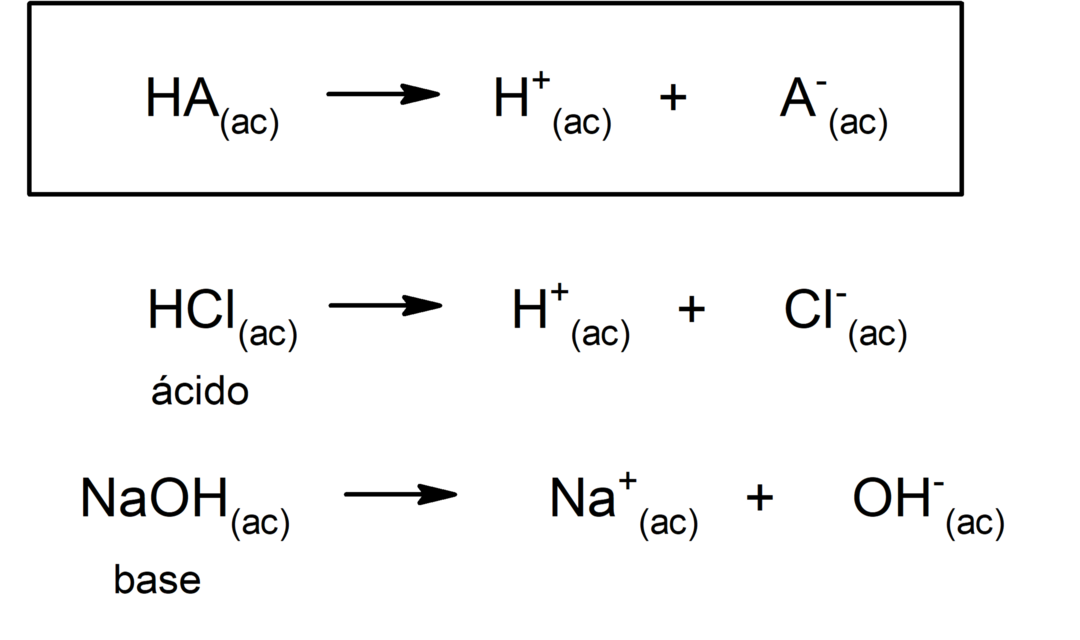
เกือบสี่สิบปีต่อมา ราวปี 1923 Brönsted และ Lowry ได้กำหนดทฤษฎีอื่นโดยระบุว่ากรดและเบสทำหน้าที่เป็นคู่คอนจูเกต ตามทฤษฎีนี้ กรดคือสารที่มีความสามารถในการให้โปรตอน (ในกรณีนี้ไม่ได้หมายถึงโปรตอนของนิวเคลียสของอะตอม แต่หมายถึงไอออนบวก H+, เป็น H+ ตัวย่อสำหรับ cation H3หรือ+) และเบสคือสารที่สามารถรับโปรตอนเหล่านั้นได้
ทฤษฎีนี้ระบุว่าในปฏิกิริยากรด-เบส เบสคอนจูเกตคือสปีชีส์เคมีที่เกิดขึ้นภายหลัง กรดบริจาคโปรตอนและกรดคอนจูเกตเป็นสารเคมีที่เกิดขึ้นหลังจากเบสรับโปรตอน ทฤษฎีนี้ไม่สมบูรณ์ทั้งหมด เนื่องจากมีสารหลายชนิดที่มีคุณสมบัติเป็นกรดโดยไม่ต้องมี อะตอม ไฮโดรเจนไอออนไนซ์ได้ในโครงสร้าง
แต่ในทางกลับกัน ในทฤษฎีนี้ ไม่จำเป็นว่าสารจะมีอยู่ในสารละลายที่เป็นน้ำ ตัวแทนของกรด (และเบสคอนจูเกต) และเบส (และกรดคอนจูเกตของกรด) ตามทฤษฎีของบรอนสเตด - โลว์รีคือโปรตอนของแอมโมเนีย ซึ่งไม่จำเป็นต้องเกิดขึ้นในตัวกลางที่เป็นน้ำ:
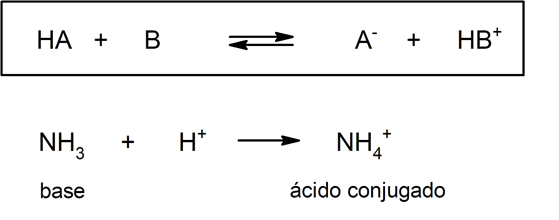
ดังนั้น เป็นส่วนเพิ่มเติมของทฤษฎีของเขาเกี่ยวกับ พันธะโควาเลนต์ลูอิสได้พัฒนาทฤษฎีที่เขานิยามกรดเป็นทั้งหมดนั้น สาร ที่สามารถรับคู่ของอิเล็กตรอนได้ในขณะที่ฐานคือสารใด ๆ ที่สามารถละทิ้งคู่อิเล็กทรอนิกส์ดังกล่าวได้
ตาม ลูอิสแนวคิดของกรดและเบสไม่เกี่ยวข้องกับการเพิ่มหรือการสูญเสียไอออนของ OH– และ H+แต่เขาเสนอว่า H + เองเป็นกรด (สามารถรับอิเล็กตรอนได้) และ OH- เป็นฐาน (สามารถบริจาคอิเล็กตรอนได้) การแสดงปฏิกิริยากรด-เบสตามทฤษฎีของลูอิสคือ:

โดยที่ OH- (ซึ่งเป็นของ NaOH) บริจาคคู่อิเล็กตรอนที่ไม่แบ่งให้ H + (ซึ่งเป็นของ HCl) อันเป็นผลให้ พิกัดหรือลิงค์ข้อมูล (พันธะโควาเลนต์ซึ่งอิเล็กตรอนคู่ที่ใช้ร่วมกันมีส่วนร่วมกับอะตอมเพียงอะตอมเดียวที่เกี่ยวข้องกับพันธะ) เพื่อสร้างโมเลกุลของน้ำ

