นิยามสมการ Arrhenius
เบ็ดเตล็ด / / June 02, 2022
นิยามแนวคิด
สมการ Arrhenius คือการแทนค่าทางคณิตศาสตร์ที่ใช้เพื่อแสดงการพึ่งพาของ ค่าคงที่จลนศาสตร์ของปฏิกิริยาเคมีกับอุณหภูมิที่สามารถทำได้ ปฏิกิริยา.

วิศวกรเคมี
สมการนี้เป็นการแก้ไขสมการ Van't Hoff และอิงจากข้อมูลเชิงประจักษ์ กล่าวคือ ประสบการณ์ที่ดำเนินการและศึกษาเพื่อหาความสัมพันธ์ที่เหมาะสมที่สุด ของพวกเขา การแสดงออก สรุปเป็น:
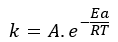
โดยที่ k คือค่าคงที่จลนศาสตร์ของปฏิกิริยา A คือปัจจัยความถี่ (ค่าคงที่ที่เกี่ยวข้องกับความถี่ของการชน) Ea คือ พลังงาน ของการกระตุ้น (J/ โมล) ที่จำเป็นในการทำปฏิกิริยา นั่นคือ พลังงานขั้นต่ำที่จำเป็นสำหรับ มีการชนกันอย่างมีประสิทธิผลระหว่างโมเลกุล R (J/ K.mol) คือค่าคงที่แก๊สสากล และ T คือค่าจริง ที่ อุณหภูมิ ของปฏิกิริยา
ควรสังเกตว่า ค่าของ k ซึ่งไม่ซ้ำกันสำหรับอุณหภูมิที่กำหนด สามารถหาได้จาก กฎ ของ ความเร็วปฏิกิริยา ไกลออกไป:

เป็น v the ความเร็ว ของปฏิกิริยา สำหรับปฏิกิริยาประเภท A + B → C โดยที่ n และ m คือลำดับปฏิกิริยาเทียบกับ A และ B
จากการทดลองจะสังเกตว่าความเร็วของ a ปฏิกิริยาเคมี เพิ่มขึ้นตามอุณหภูมิที่เพิ่มขึ้น ในขณะเดียวกัน ค่าคงที่อัตราการเกิดปฏิกิริยาจะเพิ่มขึ้นตามอุณหภูมิที่เพิ่มขึ้นและพลังงานกระตุ้นลดลง อย่างไรก็ตาม เราสังเกตว่าการพึ่งพาอาศัยกันระหว่างค่าคงที่อัตราการเกิดปฏิกิริยากับอุณหภูมิคือ อย่างไรก็ตาม หลายครั้งเราจะเห็นสมการถูกแก้ไขให้อยู่ในรูปลอการิทึม ดังนั้น เชิงเส้น:
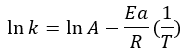
แบบจำลองนี้ช่วยให้เราสามารถหาการถดถอยเชิงเส้นโดยที่แกนกำหนดแทนด้วย ln (k) ในขณะที่อยู่บน abscissa (1/T) มี ln (A) อยู่ในตำแหน่งกับจุดกำเนิดและ ln (A) เป็นความชัน -หู.
การบังคับใช้
การใช้งานครั้งแรกและบ่อยที่สุดคือการกำหนดอัตราคงที่ของปฏิกิริยาเคมีและ จากค่านี้ ยังสามารถกำหนดความเร็วของ. ได้ (โดย Speed Law) ปฏิกิริยา. ในขณะเดียวกัน สมการ Arrhenius ยังมีประโยชน์ในการทราบพลังงานกระตุ้นและสังเกตการพึ่งพากันระหว่างค่าทั้งสอง
ตัวอย่างเช่น หากกำหนดค่าคงที่อัตราการเกิดปฏิกิริยาสำหรับอุณหภูมิที่แตกต่างกัน จากความชันของเส้นโค้ง ln (k) เทียบกับ (1/T) เป็นไปได้ที่จะได้รับค่าพลังงานกระตุ้นของปฏิกิริยา

*ภาพประกอบการทำงาน"การวิจัย นำไปใช้กับการแปรรูปแร่และอุทกโลหะวิทยา" เผยแพร่ในปี 2015 โดย UadeC
ที่นี่คุณสามารถเห็นการทำให้เป็นเส้นตรงที่ยกขึ้นด้านบน
คุณค่าของพลังงานกระตุ้นทำให้เรามีความคิดว่าความเร็วตอบสนองอย่างไรเมื่อเทียบกับการเปลี่ยนแปลงของอุณหภูมิ กล่าวคือ พลังงานกระตุ้นสูงสอดคล้องกับอัตราการเกิดปฏิกิริยาที่ไวต่ออุณหภูมิมาก (มีความลาดชัน) ในขณะที่พลังงานกระตุ้นเล็กน้อยสอดคล้องกับอัตราการเกิดปฏิกิริยาที่ค่อนข้างไม่ไวต่อการเปลี่ยนแปลงใน อุณหภูมิ.
ในทางกลับกัน ถ้าพลังงานกระตุ้นและค่าของอัตราการเกิดปฏิกิริยาคงที่ที่ค่าที่กำหนด อุณหภูมิ แบบจำลองอนุญาตให้ทำนายอัตราการเกิดปฏิกิริยาที่อุณหภูมิที่กำหนดอื่น เนื่องจากสำหรับสองเงื่อนไข คุณมี:
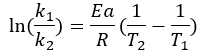
ในสาขาอื่นๆ เช่น วิศวกรรมวัสดุและ อาหารสมการนี้ได้รับการพัฒนาและดำเนินการในแบบจำลองที่ช่วยให้สามารถทำนายคุณสมบัติและพฤติกรรมจากการเปลี่ยนแปลงของอุณหภูมิของปฏิกิริยา
ในทำนองเดียวกัน สมการนี้ใช้ในด้านอิเล็กทรอนิกส์เพื่อศึกษาแบตเตอรี่เมทัลไฮไดรด์และอายุการใช้งาน นอกจากนี้ สมการนี้ได้รับการพัฒนาเพื่อให้ได้ค่าสัมประสิทธิ์การกระจาย อัตราคืบ และแบบจำลองทางความร้อนอื่นๆ
ข้อจำกัด
ข้อจำกัดที่แพร่หลายที่สุดของสมการนี้คือการบังคับใช้ในสารละลายที่เป็นน้ำเท่านั้น แม้ว่าจะถูกดัดแปลงเพื่อนำไปใช้กับของแข็ง แต่โดยหลักการแล้ว มันถูกเสนอสำหรับสารละลายที่มีตัวทำละลายเป็นน้ำ
ในทำนองเดียวกัน ควรสังเกตว่าแบบจำลองนี้เป็นแบบจำลองเชิงประจักษ์และไม่แม่นยำ โดยอิงจากประสบการณ์ที่หลากหลายและผลลัพธ์ทางสถิติ



