25 ตัวอย่างของเฮไลด์
ตัวอย่าง / / November 09, 2023
ก เฮไลด์หรือเฮไลด์ มันคือ สารประกอบเคมี ไบนารีที่ประกอบด้วย อะตอม ของฮาโลเจนและธาตุหรือแคตไอออนที่มีอิเล็กโตรเนกาติวีตี้ต่ำกว่าฮาโลเจน ตัวอย่างเช่น:
- โซเดียมคลอไรด์ (NaCl)
- แคลเซียมฟลูออไรด์ (CaF2)
- โพแทสเซียมโบรไมด์ (KBr)
- ไฮโดรเจนคลอไรด์ (HCl(ช))
ฮาโลเจนนั้น องค์ประกอบทางเคมี ซึ่งประกอบขึ้นเป็นกลุ่มที่ 17 ของ ตารางธาตุ. ฮาโลเจนได้แก่: ฟลูออรีน (F), คลอรีน (Cl), โบรมีน (Br), ไอโอดีน (I), แอสทาทีน (At), เทเนโซ (Ts)
- ดูสิ่งนี้ด้วย: อัลดีไฮด์และคีโตน
ประเภทของเฮไลด์
เฮไลด์อาจเป็น: ขึ้นอยู่กับองค์ประกอบ
- เฮไลด์อนินทรีย์. เป็นสารประกอบเคมีอนินทรีย์ที่มีอะตอมของฮาโลเจนตั้งแต่หนึ่งอะตอมขึ้นไป อาจเป็นเกลืออนินทรีย์ ไฮโดรเจนเฮไลด์ หรือสารเชิงซ้อนของโลหะ ตัวอย่างเช่น: โซเดียมคลอไรด์ (NaCl) และไอออน HgI ที่เป็นเตตระโอโดเมอร์คิวเรต42-.
- เฮไลด์อินทรีย์. เป็นสารประกอบเคมีอินทรีย์ที่มีอะตอมของฮาโลเจนตั้งแต่หนึ่งอะตอมขึ้นไปจับกับอะตอมคาร์บอนของสารประกอบอินทรีย์ ตัวอย่างเช่น: เมทิลคลอไรด์ (CH3 – Cl) และไตรคลอโรมีเทน (CH – Cl3).
ตัวอย่างของเฮไลด์
- โซเดียมคลอไรด์ (NaCl)
- แคลเซียมคลอไรด์ (CaCl2)
- ซิลเวอร์ฟลูออไรด์ (AgF)
- ลิเธียมฟลูออไรด์ (LiF)
- โพแทสเซียมไอโอไดด์ (KI)
- โพแทสเซียมโบรไมด์ (KBr)
- คอปเปอร์(II) คลอไรด์ (CuCl2)
- เหล็ก(III) คลอไรด์ (FeCl3)
- โครเมียม(III) โบรไมด์ (CrBr3)
- อะลูมิเนียมคลอไรด์ (AlCl3)
- แอมโมเนียมคลอไรด์ ((NH4)ซีแอล)
- ตะกั่ว(II) ไอโอไดด์ (PbI2)
- แมกนีเซียมไอโอไดด์ (MgI2)
- เบริลเลี่ยม ฟลูออไรด์ (BeF2)
- อะลูมิเนียมฟลูออไรด์ (AlF3)
- โบรโมมีเทน (CH3 – บรา)
- ไอโอโดฟอร์ม (CHI3)
- เมทิลคลอไรด์ (CH3 –Cl)
- โบรโมมีเทน (CH3 – ช2 – บรา)
- ไดคลอโรอีเทน (Cl – CH2 – ช2 –Cl)
- ซิลเวอร์โบรไมด์ (AgBr)
- ดีบุก(IV) คลอไรด์ (SnCl4)
- ไทเทเนียม(IV) คลอไรด์ (TiCl4)
- ไฮโดรเจนคลอไรด์ (HCl(ช))
- ไฮโดรเจนโบรไมด์ (HBr(ช))
คุณสมบัติทางกายภาพของเฮไลด์
คุณสมบัติทางกายภาพบางประการของเฮไลด์คือ:
- อัลคิลเฮไลด์ (เฮไลด์อินทรีย์) มีความหนาแน่นและจุดเดือดสูงกว่าอัลเคนที่เกี่ยวข้อง สิ่งนี้เกิดขึ้นเนื่องจากอะตอมของฮาโลเจนได้เข้ามาแทนที่อะตอมของไฮโดรเจนใน ไฮโดรคาร์บอน ซึ่งเป็นที่มาของเฮไลด์
- ฟลูออไรด์และคลอไรด์อินทรีย์มีความหนาแน่นน้อยกว่าน้ำ ในขณะที่โบรไมด์และไอโอไดด์อินทรีย์มีความหนาแน่นมากกว่าน้ำ
- อัลคิลเฮไลด์ไม่ละลายในน้ำและละลายได้ในตัวทำละลายอินทรีย์
- ไฮโดรเจนเฮไลด์เป็นก๊าซที่มีกลิ่นรุนแรงที่อุณหภูมิห้อง
- เฮไลด์ที่เกิดจากอะตอมของธาตุในกลุ่มที่ 1 ของตารางธาตุจะเป็นของแข็งสีขาว
คุณสมบัติทางเคมีของเฮไลด์
- อัลคิลเฮไลด์ผ่านปฏิกิริยาการแทนที่อะลิฟาติกนิวคลีโอฟิลิก เหล่านี้เป็นปฏิกิริยาที่อะตอมนิวคลีโอฟิลิก (อุดมไปด้วยอิเล็กตรอน) เข้ามาแทนที่อะตอม (ออกจากหมู่) ที่เกาะติดกับอะตอมอิเล็กโทรฟิลิก (ขาดอิเล็กตรอน)
ตัวอย่างเช่น: ในปฏิกิริยาของเมทิลโบรไมด์ (CH3 – Br) ด้วยโซเดียมไฮดรอกไซด์ (NaOH) โบรมีน (หมู่ที่ออกจากกัน) จะถูกแทนที่ด้วยไฮดรอกไซด์ไอออน (นิวคลีโอไฟล์) ในเมทิลโบรไมด์ โดยที่คาร์บอนคืออิเล็กโทรฟิล
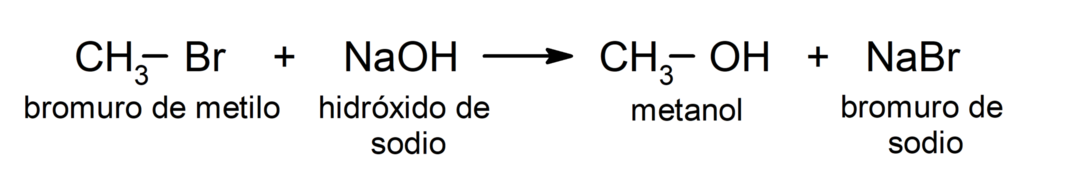
- อัลคิลเฮไลด์บางชนิดทำปฏิกิริยากับแมกนีเซียมในตัวทำละลาย เช่น อีเทอร์หรือเตตระไฮโดรฟูแรน และผลลัพธ์ที่ได้คือสารประกอบออร์แกโนเมทัลลิกที่เรียกว่า “น้ำยากริกนาร์ด” ตัวอย่างเช่น: เอทิลโบรไมด์ (CH3 – ช2 – Br) มีแมกนีเซียม (Mg) ทำปฏิกิริยาในตัวกลางแห้งเพื่อผลิตเอทิลแมกนีเซียมโบรไมด์ (CH3 – ช2 – มก.)

- อัลคิลเฮไลด์ปฐมภูมิเกิดปฏิกิริยากับอัลคอกไซด์หรือ แอลกอฮอล์ ในตัวกลางพื้นฐานเพื่อผลิตอีเทอร์ ปฏิกิริยาเหล่านี้เรียกว่า “การสังเคราะห์วิลเลียมสัน” ตัวอย่างเช่น: ปฏิกิริยาระหว่างเมทิลโบรไมด์ (CH3Br) และโซเดียมเมทอกไซด์ (CH3ONa) ผลิตไดเมทิลอีเทอร์ (CH3โอช3).
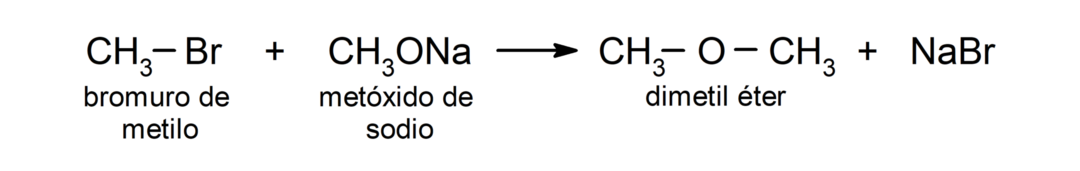
การใช้เฮไลด์
เฮไลด์หรือเฮไลด์มีการใช้งานที่หลากหลายในอุตสาหกรรม ยา และชีวิตประจำวัน แอปพลิเคชันบางส่วนเหล่านี้ ได้แก่:
- พวกมันถูกใช้เป็นตัวทำละลายสำหรับหลายๆ คน สารประกอบอินทรีย์.
- ใช้เป็นยาฆ่าเชื้อและน้ำยาฆ่าเชื้อ
- พวกมันถูกใช้เป็นสารทำความเย็น
- ใช้ในการผลิตโพลีเมอร์ฟลูออริเนต ตัวอย่างเช่น เทฟล่อน.
- ใช้เป็นเกลือที่กินได้หรือทิงเจอร์ในทางการแพทย์
- ใช้ในการบำบัดน้ำและการทำให้บริสุทธิ์
- โลหะเฮไลด์ใช้ในการผลิตโคมไฟ
- ใช้ในการทำความสะอาดชิ้นส่วนอิเล็กทรอนิกส์
- ใช้เป็นสารเคมีตั้งต้นเพื่อสังเคราะห์สารประกอบอินทรีย์ที่ซับซ้อนมากขึ้น
- บางชนิด เช่น ซิลเวอร์โบรไมด์ (AgBr) ถูกนำมาใช้ในการพัฒนาเพลทถ่ายภาพ
อันตรายจากเฮไลด์
อัลคิลเฮไลด์ที่ใช้เป็นตัวทำละลายจะทำปฏิกิริยาอย่างรุนแรงกับเบสแก่และสารออกซิไดซ์อย่างแรง ซึ่งอาจทำให้เกิดการระเบิดและไฟไหม้ได้
นอกจากนี้ คลอโรฟลูออโรคาร์บอน (CFC) ยังเป็นอัลคิลเฮไลด์ที่ใช้เป็นสารทำความเย็นมานานหลายทศวรรษ แต่ การจ้างงานเป็นสิ่งต้องห้ามโดยหน่วยงานระหว่างประเทศเพราะพวกเขามีหน้าที่หลักในการเจาะรูในชั้นของ โอโซน.
ในทางกลับกัน ไฮโดรเจนเฮไลด์ทำให้เกิดอาการระคายเคืองต่อดวงตา ผิวหนัง และเยื่อเมือก
ติดตามด้วย:
- คุณออกไป
- เกลือของกรด
- เกลือที่เป็นกลาง
อ้างอิง
- ซาโลมอนส์, ที. ก. (1996). พื้นฐานของเคมีอินทรีย์ ไวลีย์.
- ไวท์เทน, เค. ดับเบิลยู. เกลลีย์ เค. ดี. เดวิส อาร์. อี., เดอ แซนโดวาล, ม. ต. ถึง. O. และ Muradás, R. ม. ก. (1992). เคมีทั่วไป (หน้า 108-117). แมคกรอ-ฮิลล์.
- เวลส์, เอ. เอฟ (1978). เคมีอนินทรีย์โครงสร้าง. เปลี่ยนกลับ



