Homojen ve Heterojen Dengenin Tanımı
Çeşitli / / December 12, 2021
kavramsal tanım
Bir kimyasal reaksiyonun dengesi, tüm reaktanlar ve ürünler bir arada ise homojen olabilir. aynı kümelenme durumu veya farklı ürünler ve reaktanlar söz konusuysa heterojen aşamalar.

Kimya Mühendisi
homojen denge
Genel olarak asit-baz dengesi, sulu çözeltilerde meydana geldikleri için homojendir. Benzer şekilde, her bir asit veya bazın iyonlaşma derecesi, pH değerini yükseltecektir. çözüm ve bu süreç, sırasıyla Ka ve Kb olarak bilinen asitlik veya bazlık sabiti tarafından yönetilir.
İşte bir örnek Denge homojen kimyasal ve ilgili denge sabiti:
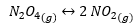
Olmak:
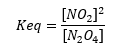
Unutulmamalıdır ki kimyasal denge, reaksiyon hızı doğrudan eşittir hız dolaylı reaksiyon.
heterojen denge
Genel olarak, ilk veya son fazları sulu çözeltide seyreltilmiş veya çökeltilmiş bir katıya tepki verdiğinden, bunları iyonik bileşiklerin çözeltilerine veya çökeltilerine bağlarız. Bu durumlarda, süreci yöneten sabitin denge sabiti Keq olduğu, ancak katıların bu sabitin ürünlerinde devreye girmediği belirtilmelidir.
Heterojen bir dengenin açık bir örneği, yüksek seviyedeki ayrışmadır. hava sıcaklığı katı kalsiyum oksit ve gaz halinde karbon dioksit oluşturan katı kalsiyum karbonat:
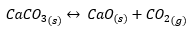
Olmak:
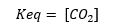
Heterojen katı-sıvı dengesi
Bir katının çökeldiği heterojen dengede, çözünürlük çarpımı sabiti veya Kps temel bir rol oynar ve bu durumda, süreci yöneten ve katının kullanılan çözücüde ne kadar çözünür olduğunu gösteren denge sabitidir. Suçlu.
Bu ne hakkında? Pratik olarak, bir iyonik bileşikten çözünmeyen veya az çözünen bir ürünün oluşumuna kadar, bu nedenle, bu durumlarda bir dizi faktörler Önemli bir rol oynarlar.
İlk olarak, tüm dengelerde olduğu gibi, sıcaklık, çünkü sıcaklıktaki artış, sıcaklıkta bir artışa yol açar. Kinetik enerji neden olduğu titreşimler nedeniyle bağlanma kuvvetlerini zayıflatan kristallerin.
Öte yandan, etkileşen bileşiklerin doğası, bildiğimiz gibi, daha büyük Çözücünün ve çözülecek bileşiğin polaritesindeki benzerlik, derecesi daha iyi çözünürlük. Çözücü ile çözülecek katı arasındaki etkileşim kuvvetlerinin büyüklüğü katının başlangıçta sahip olduğu kuvvetlere benzer olması gerektiği için bu açıklanmaktadır.
Son olarak, sistemin entropisi çok önemli bir rol oynar. Entropi varyasyonu, bir sistemin düzen derecesini açıklar ve bilindiği gibi, Evren her zaman kaosa veya düzensizliğe eğilimlidir. Çözünme gerçekleştiğinde, iyonik bileşiğin bağları bozularak düzensizlik artar, bu nedenle süreç yaygın olarak tercih edilir.
Dolayısıyla, bir iyonik bileşik denge reaksiyonunun doğrudan anlamında çözündüğünde ve çökeldiğinde, tersi anlamda, süreci yöneten bağıntı, bahsedilen çözünürlük ürününün sabitidir.
Her iki denge türünde de ortak özellikleri vurgulayabiliriz: ilk olarak, dengeyi kontrol ettiği için sıcaklık temel bir rol oynar. Bu değişken değişirse, Le Chatelier İlkesine göre sistem, söz konusu bozukluğa karşı koyacak şekilde tepki verecektir. Benzer şekilde, denge sabitinin değeri, belirli bir sıcaklıkta her bir denge reaksiyonu için benzersizdir ve faaliyetlerin bir bölümüne karşılık gelir, bu nedenle ürünlerin konsantrasyonundan veya basıncından bağımsızdır ve reaktifler. Keq'in sıcaklıkla değişiminin çalışmasını derinleştirmek için, Denklem Van't Hoff'un fotoğrafı.
İkincisi, denge durumu zamanla değişmemelidir ve bir denge durumundan bahsettiğimizde kapalı bir sistemde gerçekleşen bir sürece atıfta bulunuruz.
Öte yandan, her durumda, ifade gerçekleştirilen süreç ne olursa olsun, denge sabitlerinin oranı şu şekilde kalır: ürünlerin konsantrasyonu katsayılarına yükseltilmiş reaktif konsantrasyonuna göre ilgili stokiyometrik katsayılarına yükseltilmiş stokiyometrik. Bu sabitlerin çoğunun 25ºC'de tablolaştırıldığına dikkat edilmelidir.
bibliyografya
Başkan notları, Genel Kimya I, UNMdP, Mühendislik Fakültesi, 2019.
Homojen ve Heterojen Denge Konuları


