Arrhenius Denklemi Tanımı
Çeşitli / / June 02, 2022
kavram tanımı
Arrhenius denklemi, denklemin bağımlılığını ifade etmek için kullanılan matematiksel bir temsildir. bir kimyasal reaksiyonun gerçekleştirilebildiği sıcaklıkla kinetik sabiti reaksiyon.

Kimya Mühendisi
Bu denklem Van't Hoff denkleminin bir modifikasyonudur ve ampirik verilere, yani en uygun korelasyonu bulmak için yürütülen ve incelenen deneyimlere dayanmaktadır. Onların ifade özetlenmiştir:
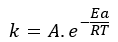
Burada, k reaksiyonun kinetik sabitidir, A frekans faktörüdür (çarpışmaların frekansını içeren bir sabit), Ea ise Enerji reaksiyonu gerçekleştirmek için gereken aktivasyonun (J/mol) miktarı, yani moleküller arasında etkili çarpışmalar vardır, R (J/ K.mol) evrensel gaz sabitidir ve T gerçek değerdir en sıcaklık tepkime.
Belirli bir sıcaklık için benzersiz olan k değerinin, Yasa nın-nin reaksiyon hızı daha öte:

v olmak hız A + B → C tipi bir reaksiyon için reaksiyonun Burada n ve m, A ve B'ye göre reaksiyon mertebeleridir.
Deneysel olarak, bir hızın Kimyasal reaksiyon
artan sıcaklıkla artar. Bu arada, artan sıcaklık ve azalan aktivasyon enerjisi ile reaksiyon hız sabiti artacaktır. Bununla birlikte, reaksiyon hızı sabiti ile sıcaklık arasındaki bağımlılığın Ancak üstel, ancak birçok kez denklemin logaritmik biçimine değiştirildiğini göreceğiz, bu nedenle doğrusallaştırılmış: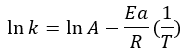
Bu model, ordinat ekseninin ln ile temsil edildiği bir lineer regresyon bulmamızı sağlar. (k) apsis üzerindeyken (1/T), ordinatın ln (A) ve eğim olarak ln (A) olması -Kulak.
uygulanabilirlik
İlk ve en yaygın kullanım, kimyasal reaksiyonun hız sabitinin belirlenmesidir ve, Bu değerden (Hız Kanunu ile) aracın hızını da belirlemek mümkündür. reaksiyon. Bu arada Arrhenius Denklemi, Aktivasyon Enerjisini bilmek ve her iki değer arasındaki bağımlılığı gözlemlemek için de yararlıdır.
Örneğin, farklı sıcaklıklar için reaksiyon hızı sabitlerinin değerleri belirlenirse, eğrinin eğiminden ln (k) vs. (1/T) Reaksiyonun aktivasyon enerjisi değerini elde etmek mümkündür.

*İşin resmi"Araştırma Maden İşleme ve Hidrometalurjiye Uygulanır", UAdeC tarafından 2015 yılında yayınlandı
Burada yukarıda yükseltilmiş doğrusallaştırmayı görebilirsiniz.
Aktivasyon Enerjisinin değeri, sıcaklıktaki değişikliklere göre hızın nasıl tepki verdiği hakkında bize bir fikir verir, yani bir Yüksek Aktivasyon Enerjisi, sıcaklığa çok duyarlı (dik eğimli) bir reaksiyon hızına karşılık gelir, küçük bir Aktivasyon Enerjisi, reaksiyon hızındaki değişimlere nispeten duyarsız olan bir reaksiyon hızına karşılık gelir. sıcaklık.
Öte yandan, belirli bir noktada Aktivasyon Enerjisi ve reaksiyon hızının değeri sabitse, sıcaklık, model, iki koşul için olduğundan, verilen başka bir sıcaklıkta reaksiyon hızının tahmin edilmesini sağlar. sahip olduğunuz farklı:
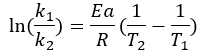
Malzeme mühendisliği gibi diğer alanlarda ve gıdalarBu Denklem, reaksiyon sıcaklıklarındaki değişikliklerden özelliklerin ve davranışların tahmin edilmesini sağlayan modellerde geliştirilmiş ve uygulanmıştır.
Benzer şekilde, bu Denklem elektronik alanında metal hidrit pillerin ve hizmet ömürlerinin incelenmesi için kullanılır. Ek olarak, bu Denklem, yayılma katsayıları, sürünme oranları ve diğer termal modellemeleri elde etmek için geliştirilmiştir.
sınırlamalar
Bu Denklemin en yaygın sınırlaması, sadece sulu çözeltilerde uygulanabilirliğidir. Katılara uygulanmak üzere modifiye edilmiş olmasına rağmen, prensip olarak çözücüsü su olan çözeltiler için önerilmiştir.
Aynı şekilde, ampirik bir model olduğu ve kesin olmadığı, çoklu deneyimlere ve istatistiksel sonuçlara dayalı olduğu belirtilmelidir.