10 Приклади газових сумішей
Різне / / July 04, 2021
Суміші газоподібні речовини Їх досягти найпростіше, оскільки дуже можливо, що речовини, що перебувають у такому агрегатному стані, змішуються. Наприклад: Неон, суміш аргону та ксенону, аерозольний інсектицид, повітря та гелій.
Практично всі гази можуть поєднуватися необмежено, звичайно, деякими умовами хімічні, фізичні та принципово пов'язані з аспектами безпеки користувачів, що маніпулює. Як і різні типи сумішей, які встановлюються між речовинами, суміші гази вони також мають властивості, властиві лише їм.
Вивчення газовані суміші зазвичай корисний, як і газів у чистому стані: ті самі знання про повітря, що є в атмосфера була б неможливою, якби не знання про пропорції та поведінку змішаних газів.
Таким чином, важливо знати деяких особливості газових сумішей, таких як властивість парціального тиску (що надається кожним з газів всередині суміші) та мольної частки (співвідношення між кількістю молей газоподібного компонента та кількістю молей загальної суміші сода). Родимки виражають кількість газу в суміші.
Закон Дальтона стверджує, що загальний тиск газової суміші дорівнює сумі парціальних тисків кожного з них один з окремих газів, які в ньому беруть участь (це залежить від газів, які не реагують між собою Так). Під парціальним тиском тут розуміють тиск, який би чинив кожен з газів, якби він знаходився лише в одному контейнері та за однакових умов температури. A) Так:
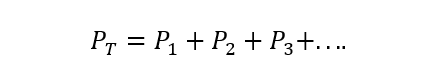
Де PТ - загальний тиск і Р1, С2 І с3 - парціальний тиск гіпотетичних газів 1, 2 і 3 в газовій суміші.
Використовуючи закон Далтона, було розроблено вираз для обчислення парціальний тиск газу в газовій суміші, якщо ми знаємо його загальний тиск і мольну частку.
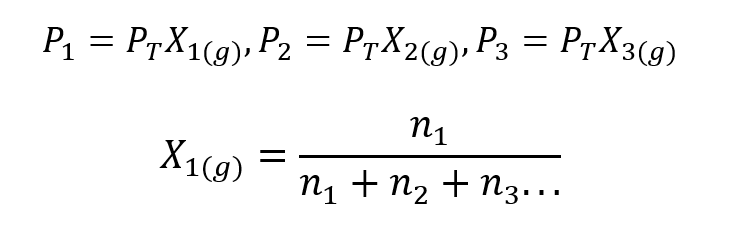
Де X1, X2 Y X3 - мольні частки гіпотетичних газів 1, 2 і 3 в газовій суміші, і п1, п2 Y п3 - це кількість речовини кожного з цих газів в одній суміші.
Один з основні властивості компонентів у сумішах - це концентрація, яка може бути виражена в різних одиницях. У разі газових сумішей концентрація його компонентів може бути виражена в мільйонних частках (частин на мільйон), одиниця віднесена до його об’єму. Тобто, певна кількість частин на мільйон компонента в газовій суміші - це відношення об’єму цієї певної кількості до об’єму кожного мільйона одиниць суміші.
Важливо зазначити, що ppm газу залежать від температури та тиску газу. З цієї причини для розрахунку проміле газу зазвичай використовують звичайні умови тиску та температури. (CNPT), які дають нормальний стан до 0 градусів Цельсія температури, і 1013 гектопаскалів (1 бар) Тиск. Якщо ці умови не використовуються, ви повинні вказати, які саме будуть використовуватися.
Це може послужити вам:
Приклади газових сумішей
Наступний перелік містить газові суміші із зазначенням елементів, які містяться в суміші:
- Повітря (суміш 21% кисню та 79% азоту, плюс інші гази в малих пропорціях)
- Кронігон (суміш 99% аргону та 1% кисню)
- Тримікс (суміш кисню, азоту та гелію)
- Неон, аргон і ксенон
- Суміш 85% метану, 9% етану, 4% пропану та 2% бутану.
- Гексафторид сірки та повітря
- Аерозольний інсектицид
- Повітря та гелій
- Нітрокс (повітряна суміш, збагачена киснем та азотом)
Слідуйте за:



