20 Приклади кислот
Різне / / July 04, 2021
кислоти складають важливу групу хімічні сполуки, дуже широкий. Кислоти зазвичай визначаються як сполуки, які можуть віддавати одну або кілька катіони водень (H+) до іншої сполуки, відомої як база. Хоча насправді кислоти визначаються за кількома теоріями:
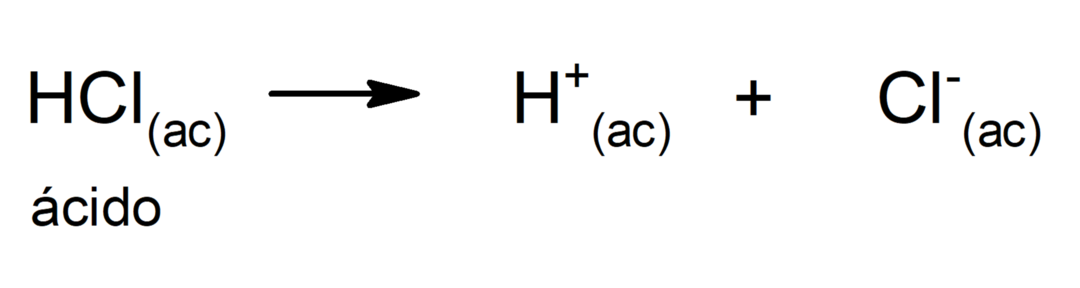 Обмеження цієї теорії полягає в тому, що кислоти визначаються лише у водному розчині.
Обмеження цієї теорії полягає в тому, що кислоти визначаються лише у водному розчині. 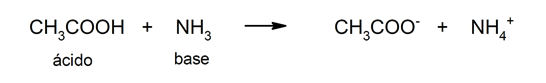

Властивість звільнення катіони водню це те, що змушує кислоти виробляти розчини рН менше 7. Кислоти, які можуть виділяти більше одного протона (використовуючи цю назву для H+) називаються поліпротонними або поліфункціональними.
Кислотні властивості
Щодо їх властивості, кислоти можна представити як рідини або як гази, рідше як твердий. Кислий смак, який ми можемо впізнати і який характеризує ці сполуки, ми знаходимо, наприклад, у цитрусові, багаті лимонною кислотою, або оцет, який є розчином кислоти оцтовий. Це органічні кислоти.
існувати органічні та неорганічні кислоти; найсильнішими, як правило, є неорганічні. Багато органічних кислот виконують важливу біологічну роль. Серед неорганічних є одна, соляна кислота, яка відіграє дуже важливу роль у процесі травлення.
нуклеїнові кислоти Вони також мають життєво важливе значення, оскільки є основою генетичного матеріалу клітин і містять ключ до синтезу білка.Тенденція до втрати протонів - це те, що визначає силу кислоти.
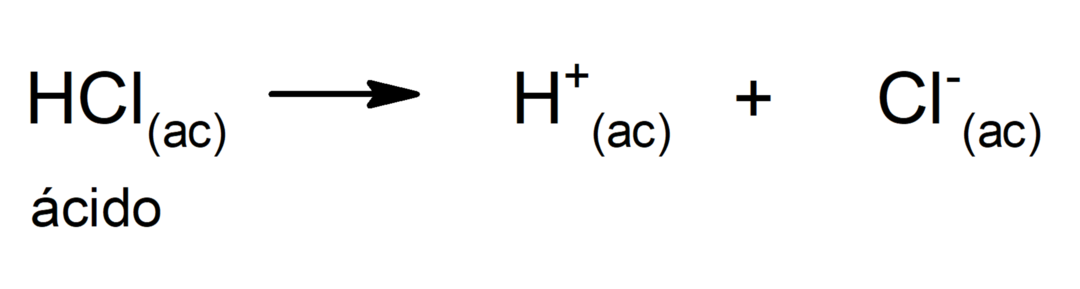
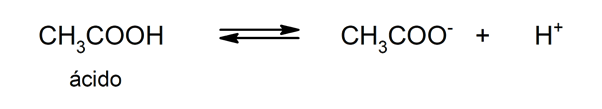
Використання кислот
Кислоти мають багато застосувань, як в промисловому, так і в домашньому масштабі. Вони часто використовуються як добавки та консерванти в Росії їжа, косметика, напої тощо Деякі кислі тверді речовини використовуються як каталізатори (прискорювачі хімічних реакцій) у нафтохімічній або паперовій промисловості.
Є також кислоти, які використовуються як дезінфікуючі засоби (карболова кислота, саліцилова кислота). Крім того, їх можна використовувати як електроліти в автомобільних акумуляторах, як це має місце з сірчаною кислотою. Остання сильна кислота також часто використовується при обробці мінерали, такий випадок є виробництвом добрив із фосфатів гірських порід.
Варто уточнити, що деякі речовини можуть бути солюбілізовані лише в кислих середовищах, і що певні реакції відбуваються лише за таких умов. Азотна кислота та аміак утворюють аміачну селітру, також важливе добриво для сільськогосподарських культур.
Приклади кислот
Двадцять кислот перераховані нижче, як приклад:
- Хлорна кислота (HClO4). Це сильна кислотна рідина a температури середовище, сильно окислюється.
- Азотна кислота (HNO3). Це сильна та інтенсивно окислююча кислота, яка використовується для виготовлення певних вибухових речовин, а також азотних добрив.
- Аскорбінова кислота (C6H8АБО6). Це вітамін С, так необхідний для здоров’я. Це захисна речовина для своєї антиоксидантної дії.
- Соляна кислота (HCl(змінного струму)). Це єдина сильна кислота, яку синтезує людський організм, - процес, який специфічно відбувається в шлунку, щоб здійснити деградацію їжа в процесі травлення.
- Винна кислота (C4H6АБО6). Це білий кристалічний порошок, він використовується у приготуванні шипучих напоїв, у хлібопекарській, виноробній та фармацевтичній промисловості. Крем із зубного каменю, який містять деякі рецепти, - це винна кислота.
- Плавикова кислота (HF(змінного струму)). Завдяки своїй здатності атакувати скло, він використовується в різьбленні та гравіруванні кришталю.
- Сірчана кислота (H2SW4). Це сильна кислота передового рівня, вона має незліченну кількість різноманітних застосувань галузей та процеси синтезу.
- Трифтороцтова кислота (C2HF3АБО2). Це хороший розчинник для багатьох органічні сполуки.
- Фосфорна кислота (H3PO4). Він присутній (у низьких концентраціях) у різних напоях кола. Вважається шкідливим для здоров’я, оскільки сприяє декальцифікації.
- Оцтова кислота (СН3COOH). Це основний компонент оцту. Кислотність, яку він створює, робить його широко використовуваним консервантом для їжі.
- Фтороантимонова кислота (SbHF6). Це найсильніша відома надкислота, яка перевищує кислотність чистої сірчаної кислоти на 1019.
- Хромна кислота (H2CrO4). Це темно-червоний порошок, він бере участь у процесі хромування. Застосовується також для скління кераміки.
- Індолуксусна кислота (C10H9НЕ2). Це головний представник ауксинів, важливих у рості гормонів Росії рослини.
- Дезоксирибонуклеїнова кислота (ДНК). Саме він утримує ключ до життя, оскільки він утворює гени, які керують синтезом незліченних білків.
- Трикарбонові кислоти. Вони включають групу карбонових кислот, що мають три карбонові групи (-СООН). Лимонна кислота (C6H8АБО7) Це одна з них.
- Мурашина кислота (СН2АБО2). Це найпростіша з органічних кислот. Тривалий вплив цієї кислоти може спричинити дихальну недостатність та смерть.
- Глюконова кислота (C6H12АБО7). Солі цієї кислоти широко використовуються в процесах очищення скляного посуду.
- Молочна кислота (C3H6АБО3). Це важлива частина біохімічних процесів.
- Бензойна кислота (C7H6АБО2). Це кислота з характерним запахом, яка широко використовується для консервування продуктів, для яких потрібна рН кислота.
- Яблучна кислота (C4H6АБО5). Він широко використовується у фармацевтичній промисловості для виробництва проносних препаратів.
- Вугільна кислота (H2CO3). Подекуди це частина процесу формування печер. Він присутній у газованих напоях.

