Приклад органічних і неорганічних молекул
Хімія / / November 13, 2021
The Загальна хімія це наука, яка вивчає всі види матерії, які існують, і його внутрішні зміни наявність контакту між різними типами цього.
The Органічна хімія Це частина загальної хімії, призначена для вивчення матерії, основною складовою якої є Елемент вуглецю, І що це частина живих організмів.
The Неорганічна хімія Саме частина загальної хімії відповідає за вивчення т. зв "мінеральна речовина", що є частиною Я не живу середовищі.
The Молекула є союзом різні атоми різних елементів хімічні речовини для утворення нових речовин з їх особливими властивостями.
З загальної хімії, Елементи Є чисті речовини які утворюються за атоми одного типу. Елементи класифікуються в періодичній системі хімічних елементів.
Так само, як він Атом є основною одиницею Елементів, Молекула є основною одиницею Сполук, які є речовинами, які мають характерну хімічну поведінку.
The сполуки може утворитися як наслідок природні явища, або створюватися в лабораторіях або в Промислові підприємства, тож молекули присутні всюди. Молекули містяться в мінералах, листі дерев, їжі, ліках, воді, яку ми п’ємо, повітрі, яким дихаємо, і навіть у забрудненні навколишнього середовища.
Загальна хімія в основному поділяється на Неорганічна хімія і Хімічнийдо оргпica, тому молекули також можна класифікувати на неорганічні та органічні.
Неорганічні молекули
У неорганічній хімії молекули в основному утворюються поєднання атомів позитивних валентностей з іншими негативними валентностями, в іонних зв'язках. Ці зв’язки утворюються в основному за рахунок електромагнітних сил між атомами, утворених наявністю валентних електронів.
Таким чином виникають всі йонні сполуки, такі як солі, оксисолі, кислоти, оксикислоти, оксиди та гідроксиди.
Неорганічні молекули як електроліти
Основна властивість іонних молекул полягає в тому, що при контакті з водою H2АБО, їх поділяють на дві його частини: позитивну і негативну. Ці дві частини, електрично заряджені атоми або групи атомів, розсіяні у воді. До неорганічної речовини, здатної таким чином розділятися у воді, його називають електролітом.
Розчин, утворений водою та позитивно і негативно зарядженими частинками, називається «Електролітичний розчин». Цей тип розчину має здатність проводити електричні струми, тому він використовується в електрохімічних елементах, таких як автомобільні акумулятори.
Молекули неорганічної кислоти та лугу
У випадку неорганічних молекул, таких як кислоти, Оксикислоти і Гідроксиди, в той же час, коли вони розділяються на позитивну і негативну частини, вони вносять у Розчин властивість під назвою Гідрогенний потенціал, що вимірюється як негативний логарифм концентрації іонів водню.
The Водневий потенціал (pH) визначає, наскільки розчин кислий. На шкалі рН, яка змінюється від значення 1 для максимальної кислотності до 14, що є повною лужністю або основною, кислотний характер змінюється від значень від 1 до 6, а лужний – від 8 до 14. 7 являє нейтральний рН; ні кислотна, ні основна. Результат від’ємного логарифма концентрації H + покаже нам, де ми знаходимося на шкалі.
Приклади кислот:
Соляна кислота: HCl: H+ + Кл-
Бромистоводнева кислота: HBr: H+ + Br-
Сірчана кислота: H2S: 2 год+ + С-2
Ціановодна кислота: HCN: H+ + CN-
Соляна кислота: HI: H+ + я-
Приклади оксикислот:
Сірчана кислота: H2ПЗ4: 2 год+ + ТАК4-2
Вугільна кислота: H2CO3: 2 год+ + CO3-2
Нітратна кислота: HNO3: H+ + НІ3-
Фосфорна кислота: H3PO4: 3 год+ + PO4-3
Хлорна кислота: HClO4: H+ + ClO4-
Приклади гідроксидів:
Гідроксид натрію: NaOH: Na+ + О-
Гідроксид кальцію: Ca (OH)2: прибл+ + 2OH-
Гідроксид амонію: NH4OH: NH4+ + О-
Гідроксид калію: KOH: K+ + О-
Гідроксид магнію: Mg (OH)2: Mg+ + 2OH-
Неорганічні молекули в хімічних реакціях
Коли неорганічні молекули беруть участь в хімічній реакції, існують чотири основних і прості механізми реакції: Синтез, декомпозиція, проста заміна та подвійна заміна. Ось приклад кожного:
Синтез
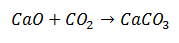
Реакція синтезу - це реакція, в якій дві молекули об’єднуються в кінцевий продукт, що складається з однієї молекули. У прикладі це випадок, коли оксид кальцію з’єднується з двоокисом вуглецю з утворенням молекули карбонату кальцію.
Розкладання:

Реакція розкладання - це реакція, в якій початкова молекула розпадається на дві нові стабільні молекули. Таким є випадок гідроксиду кальцію, який розділяється на молекулу оксиду кальцію та іншу молекулу води.
Проста заміна:

У реакції простого заміщення, атом елемента обмінюється з одним з атомів молекули. Такий випадок з металевим цинком, який ставиться на місце Гідрогену в хлориді водню, вивільняючи його та утворюючи молекули хлориду цинку.
Подвійна заміна:
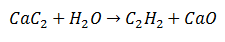
У реакції подвійного заміщення, певні атоми двох початкових молекул обмінюються, щоб утворити дві різні молекули як продукти. Такий випадок з карбідом кальцію, який піддається вивільненню вуглецю, який з’єднується з воднем з води, утворюючи ацетилен. Кальцій зв’язується з киснем, утворюючи оксид кальцію як другий продукт.
Органічні молекули
Органічна хімія - це хімія вуглецю, що означає, що всі органічні молекули будуть мати присутність цього елемента в різних структурних розташуваннях.
Органічні молекули характеризуються постійна наявність ковалентних зв'язків. Ковалентні зв'язки з тими, в яких два атоми об’єднуються, щоб поділитися своїми валентними електронами і таким чином взаємно доповнити свої октети.
Це стосується Карбону, який зв’язується з іншими атомами того ж елемента. Утворюються ланцюги дуже різної довжини, від двох до шістдесяти атомів вуглецю, і навіть ці ланцюги вони розгалужуються з іншими ланцюгами з такою ж різноманітністю довжин, досягаючи величезної різноманітності молекул органічний.
Іонні зв’язки також присутні, але вони виникають на проміжних стадіях тривалих реакційних механізмів, в яких утворюється потрібна молекула.
Найпростіші органічні молекули включають вуглець і водень. Останній доповнює валентність вуглецю, яка цього вимагає.
В органічній хімії молекули можуть бути лінійними або аліфатичними, розгалуженими, циклічними та ароматичними.
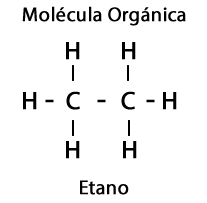
Крім того, в органічних молекулах беруть участь елементи Оксиген, Нітроген, Сірка і Фосфор, що створює вражаючу різноманітність функціональних груп для молекул.
Функціональні групи в органічних молекулах
The Функціональні групи – це групи з двох або більше атомів, які, приєднуючись до вуглець-водневого ланцюга, утворюють різні хімічні речовини з певною поведінкою.. Далі наведено сім основних типів органічних молекул з відповідними функціональними групами. Буква «R» використовується для позначення ланцюга вуглець-водень.
Алкілгалогеніди - Форма: R-X / Функціональна група: А галогенний елемент (хлор, бром, йод)

Спирти - Форма: R-OH / Функціональна група: -OH або гідроксил.
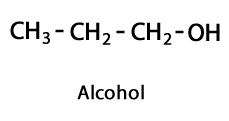
Альдегіди - Форма: R-CHO / Функціональна група: -CHO, яка завжди йде до кінця ланцюга.
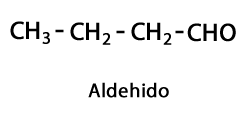
кетони - Форма: R-CO-R / Функціональна група: -CO- або Carboxy, завжди в середині Carbon ланцюга.
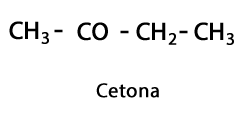
Органічні кислоти - Форма: R-COOH / Функціональна група: -COOH або Карбоксил, завжди на кінці ланцюга.
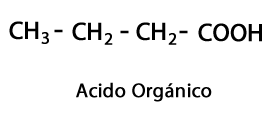
Ефіри кислоти - Форма: R-COO-R / Функціональна група: -COO-, є результатом з'єднання кислотного ланцюга з іншим ланцюгом вуглець-водень.
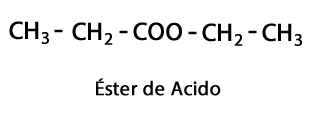
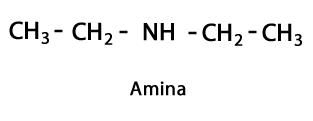
Аміни - Форма: R-NH2, R-NH-R, R-N-2R / Функціональна група: -NH2, -NH-, -N = або аміно, що є азотом, доповненим Гідрогеном у місцях, де відсутній вуглець-водневий ланцюг. Як сказано, він може йти в кінці ланцюжка або в середині. Атом Нітрогену може супроводжуватися одним, двома або трьома органічними ланцюгами для утворення кінцевої молекули. Амінами можна вважати органічні похідні аміаку NH3.
Органічні молекули в хімічних реакціях
Органічні молекули, чим довші їхні вуглецево-водневі ланцюги, тим більше місць або атомів доступно для участі в хімічній реакції.
Найчастіше елементи або ланцюги додаються до одного з присутніх вуглецю, або частина основного ланцюга відокремлюється для утворення іншої органічної сполуки окремо.
Оскільки такі реакції протікають повільно, використовуються каталізатори, які є хімічними агентами для прискорення реакцій. У деяких випадках каталізатор являє собою дрібну сітку платинового металу.
Приклади неорганічних молекул
Хлорид натрію NaCl
Калій хлорид KCl
Хлорид амонію NH4кл
Нітрат натрію NaNO3
Нітрат калію KNO3
Нітрат амонію NH4НЕМАЄ3
Сірчана кислота H2ПЗ4
Фосфорна кислота H3PO4
Фосфорна кислота H3PO3
Соляна кислота HCl
Йодоводнева кислота HI
Гідроксид натрію NaOH
Гідроксид калію KOH
Гідроксид амонію NH4о
гідроксид кальцію Ca (OH)2
Гідроксид магнію Mg (OH)2
Гідроксид заліза Fe (OH)2
Гідроксид заліза Fe (OH)3
Сульфід заліза FeS
Сульфат заліза FeSO4
Сульфат заліза Fe2(ПЗ4)3
Приклади органічних молекул
Глюкоза С6Х12АБО6
Метан CH4
Етан С2Х6
Ацетилен С2Х2
Пропан C3Х8
Бутан С4Х10
Етанол С2Х6АБО
Сахароза C12Х22АБО11
Метанол CH4АБО
Гліцерин С3Х8АБО3

