Приклади ендотермічних реакцій
Приклади / / November 09, 2023
А ендотермічна реакція Це реакція, яка поглинає енергію середовища у вигляді тепла. У цих реакціях, щоб реагенти перетворювалися на продукти, їм необхідно поглинати тепло, що призводить до того, що продукти мають більшу енергію, ніж реагенти, які їх породили. Деякі приклади ендотермічних реакцій: фотосинтез і електроліз води.
- Дивись також: Хімічні реакції
Приклади ендотермічних реакцій у повсякденному житті
Деякі з основних ендотермічних реакцій:
Вироблення озону в атмосфері. Озон утворюється в атмосфері, коли молекулярний кисень (О2) поглинає ультрафіолетове випромінювання і руйнується. Тоді атом кисню (O) може взаємодіяти з іншою молекулою кисню (O2) і утворюють озон (O3).

Електроліз води. Це процес, за допомогою якого він застосовується електрична енергія до води, щоб розділити її на два компоненти, водень (H) і кисень (O).
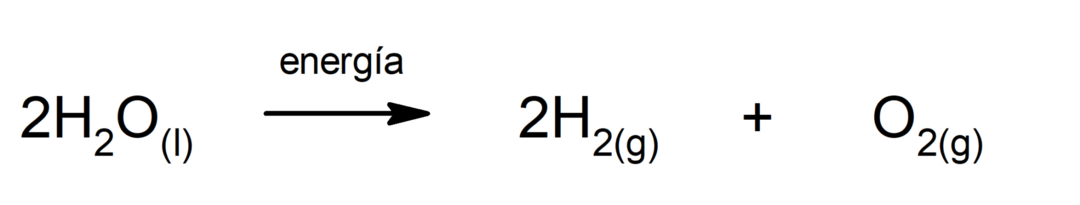
Фотосинтез. Це хімічна реакція, за допомогою якої поглинання сонячна енергія, вуглекислий газ (CO2) перетворюється на глюкозу. Ця реакція є основним шляхом живлення рослин.
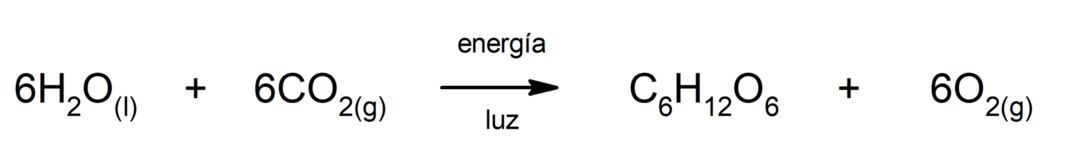
Виробництво ферум(ІІ) сульфіду. Щоб відбулася реакція між сіркою та залізом, необхідно забезпечити енергію у вигляді тепла.
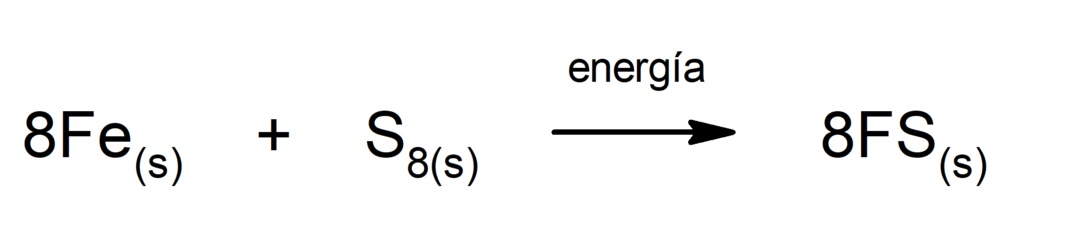
Розкладання вуглекислого газу (CO2). Розкладання CO2 При високих температурах він виробляє чадний газ (CO) і кисень (O2).
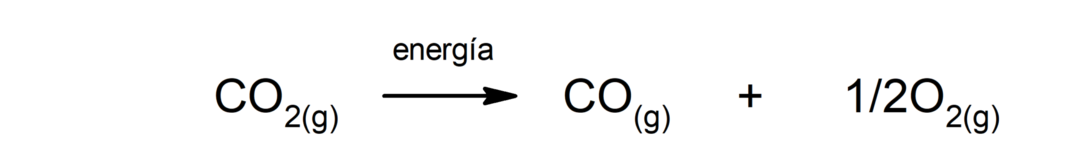
Розкладання карбонату кальцію (CaCO3). Карбонат кальцію розкладається з поглинанням тепла з утворенням оксиду кальцію (CaO) і вуглекислого газу (CO2).
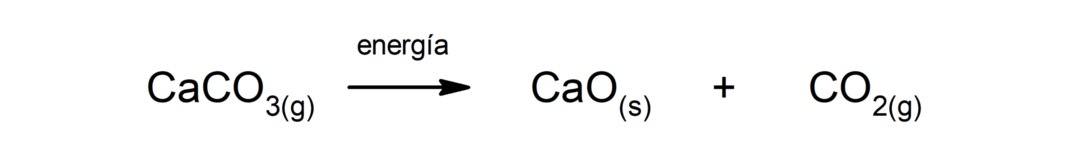
Різниця між ендотермічною та екзотермічною реакцією
Основна відмінність між ендотермічними та екзотермічними реакціями полягає в тому, що ендотермічні реакції поглинають тепло, тоді як екзотермічні реакції виділяють тепло.
Крім того, ендотермічні реакції характеризуються збільшенням ентальпії, тоді як екзотермічні реакції пов’язані зі зменшенням ентальпії.
Ентальпія — це термодинамічна величина, яка визначає потік теплової енергії при постійному тиску під час хімічної реакції. Він позначається літерою H, і його варіація є одним із основних показників, які визначають, чи є хімічна реакція ендотермічною чи екзотермічною.
- Якщо зміна ентальпії хімічної реакції перевищує нуль (ΔH > 0) є ендотермічним.
- Якщо хімічна реакція має зміну ентальпії менше нуля (ΔH < 0) є екзотермічним.
Дотримуйтеся:
- Фізико-хімічні явища
- Хімія в побуті
- Хімія в побуті
- Органічна та неорганічна хімія
Список літератури
- Сото-Кордова, С. (2016). Ендотермічні реакції. Технічне сховище Технологічний інститут Коста-Ріки.
- Коромінас, Дж. (2017). Хімічні реакції повсякденного життя. Алембік, (90), 8-26.
- Санчес, М. Т. М. і Санчес М. М. (2002). Експериментальне вивчення ендотермічних реакцій для студентів ESO. Annals of Chemistry of the RSEQ, (4), 36-39.

