Приклад ароматичних сполук
Хімія / / July 04, 2021
Хіміки виявили корисним розділити всі органічні сполуки на два широкі класи: сполуки Аліфатичний та сполуки Ароматичні. Ароматичні сполуки - це бензол та сполуки з подібною хімічною поведінкою. Ароматичні властивості відрізняють бензол від аліфатичних вуглеводнів. Молекула бензолу - це кільце певного типу. Є й інші сполуки, також кільцеподібні, які, здається, структурно відрізняються від бензолу і все ж поводяться подібним чином.
Виявляється, ці інші сполуки за своєю основною електронною структурою нагадують бензол, тому вони також поводяться як ароматичні речовини.
Аліфатичні вуглеводні (алкани, алкени, алкіни та їх циклічні аналоги) реагують головним чином доповнення, у кількох посиланнях, і за заміщення вільними радикалами, в інших точках аліфатичного ланцюга.
З іншого боку, для ароматичних вуглеводнів підкреслюється, що вони мають тенденцію до гетеролітичне заміщення. Крім того, ці самі реакції заміщення характерні для ароматичних кілець, де б вони не з'явилися, незалежно від того, які інші функціональні групи може містити молекула. Ці останні групи впливають на реакційну здатність ароматичних кілець, і навпаки.
Молекула бензолу
Бензол відомий з 1825 року, і його хімічні та фізичні властивості відомі більше, ніж властивості будь-якої іншої органічної сполуки. Незважаючи на це, лише в 1931 році для цього була запропонована задовільна структура речовини, і знадобилося до 15 років, щоб воно було загальновживаним серед хімічних речовин органічні. Складність полягала в обмеженні розвитку, якого до того часу досягла структурна теорія. Остаточна структура була досягнута завдяки припущенню кількох важливих фактів:
Бензол має молекулярну формулу С6H6. Через елементарний склад та молекулярну масу, як відомо, бензол має шість атомів Карбону та шість Атомів Гідрогену. Проблема полягала в знанні розташування таких атомів.
У 1858 р. Август Кекуле запропонував, щоб атоми Карбону могли бути пов'язані між собою, утворюючи ланцюги. Пізніше, в 1865 р., Він запропонував відповідь на бензольну проблему: ці карбонатні ланцюги іноді можуть бути замкнені, утворюючи кільця.
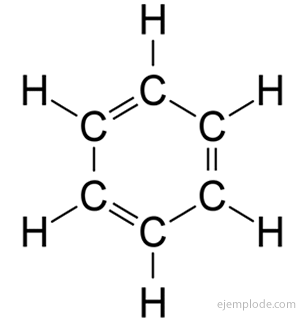
Бензол дає лише однозаміщений продукт С6H5Y. Наприклад, коли атом водню заміщений бромом, виходить лише одна конфігурація бромобензолу С.6H5Br; аналогічно також отримують хлорбензол С6H5Cl, або нітробензол C6H5НЕ2тощо Цей факт накладає суворе обмеження на структуру бензолу: повинен бути весь його водень точно еквівалентні, тобто всі вони повинні бути приєднані до Карбонів, які в свою чергу є однаковими пов'язані. У СН не може бути водню3та інші в СН2та інші в СН. Кінцева структура монозаміщеного повинна бути однаковою для заміщення будь-якого Гідрогену в бензолі.
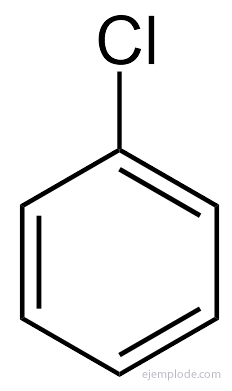
Бензол дає три ізомерні дизаміщені продукти, C6H4Y2 або С6H4І З. Існує лише три ізомерних DiBromoBenzenes, C6H4Br2, три хлоронітробензоли C6H4ClNO2тощо Цей факт ще більше обмежує структурні можливості.
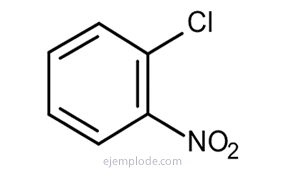
Бензол переживає реакції заміщення, а не реакції приєднання. Бензольна структура Кекуле відповідає такій, яку ми називали б циклогексатрієном. Через це він повинен легко реагувати додаванням, як і подібні сполуки, циклогексадієн та циклогексен, що є характеристикою будови алкенів. Але це не так; в умовах, коли алкени реагують швидко, бензол не реагує або дуже повільно. Замість реакцій приєднання бензол легко проходить безліч реакцій, які всі є заміщення, як Нітрування, Сульфування, Галогенування, Алкілування Фріделя-Крафта, Ациляція від Фрідель-Ремесла. У кожній з цих реакцій атом або група замінюється одним із атомів Гідрогену бензолу.
Стійкість бензолу обумовлена змінними подвійними зв'язками, а також енергією резонансу, в той, при якому подвійні зв’язки змінюють своє положення між вуглецями, зберігаючи те саме чергування структурна. Є енергія стабілізації резонансу відповідає за набір властивостей, що викликаються Ароматичні властивості.
Реакція приєднання перетворює алкен у більш стабільну насичену сполуку. Але у випадку з бензолом додаток робить його менш стабільним, руйнуючи кільцеву систему, стійку і стабілізовану за допомогою резонансу. Кінцевою молекулою буде циклогексадієн. Саме завдяки цьому факту стабільність бензолу призводить до реакцій заміщення.
Властивості ароматичних сполук
На додаток до речовин, що містять бензольні кільця, існує багато інших, які вважаються ароматичними, хоча на поверхні вони майже не мають схожості з бензолом.
З експериментальної точки зору, ароматичні сполуки - це речовини, молекулярні формули яких вказують на високий ступінь ненасиченості, незважаючи на те, якими вони є стійкий до реакцій додавання настільки характерні для ненасичених сполук.
Натомість ці ароматичні сполуки a часто зазнають реакцій електрофільного заміщення подібні до бензолу. Поряд із цим опором додаванню, і, мабуть, через це, є дані про наявність незвичайна стійкість, такі як низькі теплоти гідрування та горіння.
Ароматичні речовини циклічні, зазвичай представляючи кільця з п’яти, шести та семи атомів, і їх фізичний огляд показує, що вони є плоскі або майже плоскі молекули. Його протони мають той самий тип хімічного зсуву в спектрах ядерного магнітного резонансу, що і в бензолі та його похідних.
З теоретичної точки зору, щоб речовина була ароматичною, її молекула повинна мати циклічні хмари делокалізованих π-електронів вище і нижче площини молекули; Крім того, ці π-хмари повинні містити загалом (4n + 2) π-електронів; це означає, що делокалізації недостатньо для того, щоб отримати певну стабільність, що характеризує ароматичну сполуку.
Номенклатура похідних бензолу (ароматичні сполуки)
У випадку з багатьма з цих похідних, особливо з однозаміщеними, досить поставити група-заступник для слова бензол, така як, наприклад, хлорбензол, бромобензол, йодобензол, Нітробензол.
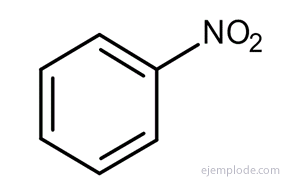
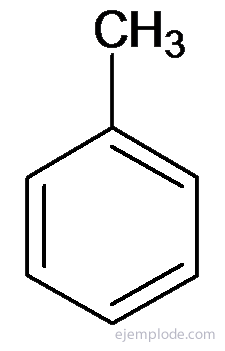
Інші похідні мають спеціальні назви, які можуть не мати подібності до назви групи-заступника. Наприклад, метилбензол відомий лише як толуол; Амінобензол як анілін; Гідроксибензол як фенол та ін.
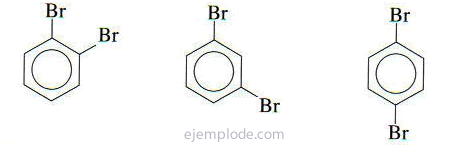
Якщо до бензольного кільця прикріплені дві групи, необхідно не тільки визначити, якими вони є, але і вказати їх відносне місце розташування. Три можливі ізомери для заміщених бензолів характеризуються префіксами ortho, meta і para, скорочено o-, m-, p-. Наприклад: o-DiBromoBenzene, m-DiBromoBenzene, p-DiBromoBenzene.
Якщо одна з двох груп є типом, який надає молекулі особливу назву, сполука називається похідним цієї спеціальної речовини. Наприклад: нітротолуол, бромофенол тощо.
Приклади ароматичних сполук
Толуол або метилбензол
Етилбензол
Ізопропілбензол
TriNitroToluene або TNT
Анілін або амінобензол
Бензойна кислота
Глутамінова кислота або параамінобензойна кислота
Толуол сульфокислота
Фенол або гідроксибензол
Бромофенол
Трихлорбензол
Бензолфеніловий ефір
Йод бензол
Бромбензол


