Приклад пептидного зв’язку
Хімія / / July 04, 2021
Пептидний зв’язок є той, в якому конденсацією з’єднуються дві молекули амінокислот.
Для кращого розуміння пептидних зв’язків спочатку слід визначити амінокислоти:
Амінокислоти - це органічні молекули короткий, що містить щонайменше аміногрупа (-NH2), лужна за своєю природою, і карбоксильної групи (-COOH), кислого характеру.
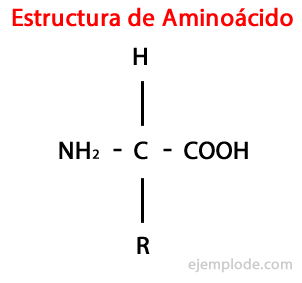
Хоча живі істоти синтезують для різних цілей дуже різноманітні типи амінокислот, найважливішими є ті, які входять до складу білків, всі вони належать до класу α-амінокислоти.
Α-амінокислоти характеризуються тим, що мають кислоту та аміногрупи, приєднані до одного і того ж атома вуглецю, званого α вуглецем. Крім того, цей α-вуглець пов'язує як третій заступник атом водню і як четвертий заступник, додаткова група різноманітних розмірів та характеристик, яка відрізняє кожну амінокислоту від інші.
Четвертий заступник називається Бічний ланцюг Амінокислота і часто в спрощеному вигляді представлена літерою R.
Оскільки чотири заступники α-вуглецю різні і приймають навколо нього тетраедричне розташування, наявні α-амінокислоти
оптична ізомерія, коли молекула має a альтернативна форма це схоже на дзеркальне відображення його, що зрештою не є рівною молекулою. Цим двом ізомерним формам молекули присвоєні літери D або L, залежно від того, як розташовані заступники в просторі. Всі амінокислоти, що містяться в білках, є L.Амінокислоти класифікуються відповідно до їх хімічного характеру в Полярний та Аполярний. Полярні в свою чергу поділяються на Нейтральний і звинувачений (який може бути кислим або основним). Неполярні можуть бути аліфатичними або ароматичними.
Пептиди та пептидна зв'язок
Пептиди є продуктом ковалентного об'єднання амінокислот через амідні зв'язки, утворюючи конденсація карбоксильного кінця одного і аміно-кінця іншого, виділяючи молекулу води в реакція. Цей союз називається пептидним зв’язком.
Механізм цієї реакції представлений нижче, в якому Аміно- та карбоксильні групи, і відбувається конденсація молекул амінокислоти з утворенням пептиду.
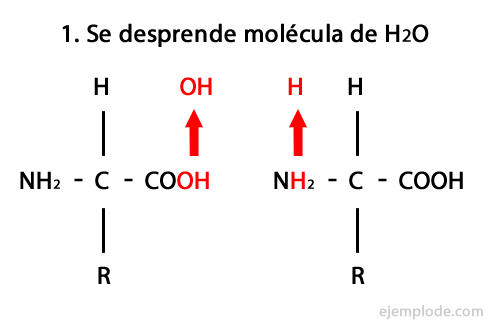
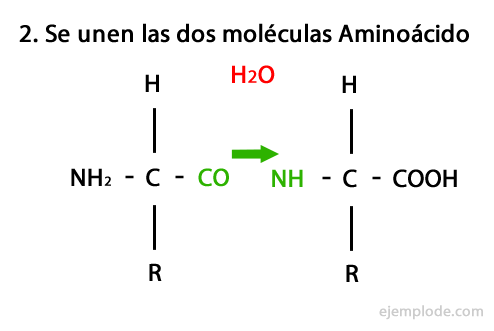

Пептиди, як амінокислоти та білки, мають на своїх кінцях аміногрупу та карбоксильну групу не реагуючи.
Щоб вказати формулу простого пептиду і навіть білка, досить перерахувати амінокислоти, що його складають, починаючи з тієї, що має безкоштовну групу Amino, і закінчуючи тим, у якому є вільна карбоксильна група.
Деякі пептиди, що знаходяться в організмі, є Вазопресин, що підвищує кров’яний тиск і збільшує реабсорбцію води в нирках; Енкефалін, що зменшує відчуття болю; та Окситоцин, що призводить до скорочення матки.
Характеристики пептидного зв’язку
Конденсація аміногрупи однієї амінокислоти з карбоксильною іншої, відбувається у водному розчиннику, так що це не спонтанно, а отже, синтез білка вимагає постачання енергії.
Пептидний зв’язок, як і будь-який амідний зв’язок, представляє резонанс між двома крайніми формами: нейтральна форма, з одинарним зв’язком, що приєднує карбонільний вуглець першої амінокислоти та аміноазот другої (C-N), і форма з поділом зарядів в якому два атоми зв’язані подвійним зв’язком (C = N). Насправді пептидний зв’язок не приймає жодної з двох екстремальних ситуацій, але є резонансним гібридом обох.
Є дзвінок Пептидний літак, складається з всі атоми, що беруть участь у пептидному зв’язку, які приєднуються до двох початкових амінокислот. З одного боку, атоми Нітрогену та Гідрогену з відповідним Вуглецем α у першій амінокислоті. З іншого - вуглець α іншої амінокислоти з киснем і вуглецем карбонільної групи.
Відмінності між пептидами та білками
пептиди мають низьку кількість амінокислот, яка коливається від двох до декількох десятків з них, і їх конформація в розчині стає гнучкою.
дрібні білки, структурно близькі до великих пептидів, мають a визначена конформація і набагато менш гнучка.
Є білки, які, як і пептиди, мають невпорядковану та гнучку конформацію, але такий порядок при взаємодії з іншими макромолекулами в клітині.
20 прикладів амінокислот, які беруть участь у пептидному зв’язуванні
- Гліцинія
- Дівчині
- Валін
- Лейцин
- Ізолейцин
- Пролін
- Метіонін
- Фенілаланін
- Тирозин
- Триптофан
- Серин
- Треонін
- Цистеїн
- Аспарагін
- Глютамін
- Аспарагінова кислота
- Глутамінова кислота
- Лізин
- Аргінін
- Гістидин

