Приклад номенклатури органічних сполук
Хімія / / July 04, 2021
Органічні сполуки - це молекули, характерними для яких є те, що вони утворені основою молекул вуглецю і водень, також відомий як скелет, і в поєднанні з іншими елементами, головним чином киснем, азотом та сіркою.
IUPAC (Міжнародний союз чистої та прикладної хімії, Міжнародний союз чистої та прикладної хімії) встановив загальні правила класифікації та номенклатури органічних молекул, з яких ми пояснюємо найбільш важливі.
Вуглеводні
Вуглеводні - найпростіші органічні молекули, що складаються з вуглецевого скелета та атомів водню. Існує три типи вуглеводнів:
Алкани
Вони найпростіші, утворені атомами вуглецю, з'єднаними простими ковалентними зв'язками з атомами водень із загальним складом Н = 2n + 2, тобто атоми водню вдвічі більше атомів водню. вуглець, плюс 2. Його номенклатура сформована з числовими префіксами met- для 1 атома вуглецю, et- для 2, prop- для 3 та but- для 4; з 5 атомів вуглецю використовуються загальноприйняті префікси pent-, hex-, hept-, oct- та ін. До всіх алканів додається закінчення -ano.
Приклад: СН4: метан; C.2H6: етан; C.4H10: бутан; C.6H14: гексан
Алкени
Вони утворені вуглецевим скелетом, у якому між атомами вуглецю існує подвійний зв’язок. Його загальна формула - H = 2n, тобто атоми водню вдвічі перевищують кількість атомів вуглецю. Як і алкани, вони використовують префікси, що вказують на їх кількість атомів вуглецю, і в цьому випадку додається закінчення -eno. Крім того, в молекулах з більш ніж трьома атомами вуглецю вуглець, де знаходиться подвійний зв’язок, починаючи відлік від вуглецю, найближчого до є.
Приклади: C2H4: етен; C.3H6: пропен; C.4H8: бутен, 2-бутен; C.6H12: Гексен, 2-гексен (подвійний зв’язок у атома 2), 3-гексен (подвійний зв’язок у атома 3).
Алкіни
Алкіни містять потрійний зв’язок у своїх атомах вуглецю. Його загальна формула - H = 2n-2, що вказує на те, що молекула буде містити два атоми водню, що менше подвійного числа атомів вуглецю. До префікса, що вказує кількість вуглецю, додається закінчення -ino. Як і у випадку з алкенами, згадується вуглець, що містить потрійний зв’язок, відлічуючи від найближчого до нього крайнього.
Приклади: C2H2: етин; C.3H4: порада; C.4H6: бутин, 2-бутин; C.6H12: Гексино, 2-гексен (потрійний зв’язок у атома 2), 3-гексин (потрійний зв’язок у атома 3).
Функціональні групи
Функціональні групи - це комбінації атомів, які функціонують як іон і замінюють атом водню у формулі алкану.
Радикали
Алкан без атома водню називається радикалом, і для його ідентифікації додається закінчення -ilo:
Приклади СН4: метан - СН3+ метил; C.2H6: етан - C2H5+ етиловий; C.4H10: бутан - C4H9+ бутил; C.6H14: гексан - C6H13+ гексил.
Поєднання вуглеводнів
Одним із випадків, який може статися, є те, що два або більше вуглеводнів поєднуються в молекулі. Вуглеводні, з якими він поєднується, називаються деревними. У цих випадках базовим вуглеводнем буде той, що має найдовший ланцюг, а кількість вуглецю де знайдені дендроциенти, за якими йде назва радикала з закінченням -il, а потім назва вуглеводню база. Номер буде згадуватися стільки разів, скільки прикріплених до нього дерев. У тому випадку, якщо деревоподібні мають один і той же радикал у різних атомах вуглецю, цифри, відокремлені комами, будуть згадані, після чого буде дефіс, назва радикала, потім числа атомів, до яких приєднаний інший радикал, якщо є, тире, назва радикала та назва вуглеводню база. Якщо до одного і того ж атома вуглецю приєднано два радикали, число буде зазначено двічі. Якщо це різні радикали, то це буде згадано один раз перед назвою кожного радикала; якщо радикали рівні, число буде згадано двічі. Ми почнемо з того, що спочатку згадаємо найпростіші дендроценції (ті, що мають найменшу кількість вуглецю), а потім ті, що мають найбільшу кількість.
Приклад: Молекула пентану з двома радиканами етану, приєднаними до вуглецю 2 та 3:
2,3-етилпентану. Молекула октану, радикал пропану на вуглеці 6, радикали метану на вуглецях 4 та 5 та радикали етану, зв’язані на вуглецях 2, 3 та 4: 4,5-метил-2,3,4-етил-6- пропіл -октан.
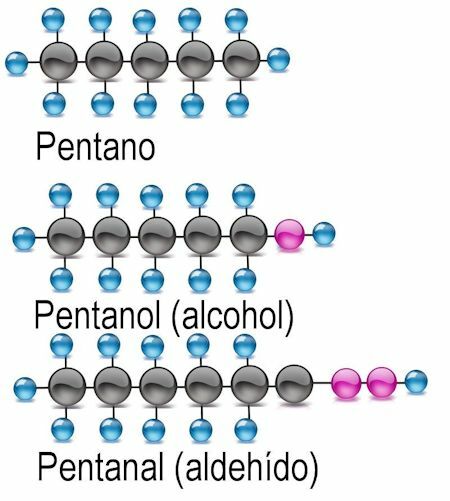
Алкогольна функціональна група
Найпростіша з функціональних груп - спирт, у якому атом водню заміщений гідроксильною групою (ОН). У цих сполуках закінчення -анол додається до назви радикала. Там, де це доречно, слід зазначити атом вуглецю, де знаходиться функціональна група:
Приклади СН3OH: метанол: C2H5OH етанол; C.4H9OH бутанол або 2-бутанол; C.6H13OH гексанол, 2-гексанол (функціональна група у атома 2), 3-гексанол (функціональна група у атома 3).
Альдегідна функціональна група
В альдегідах атом водню обмінюється на функціональну групу -CHO. Для їх ідентифікації додається закінчення -anal, а також згадується атом вуглецю, де знаходиться функціональна група:
Приклади СН3COH: метанал: C2H5Етановий COH; C.4H9COH бутанал або 2-бутанал; C.6H13Гексаналь COH, 2-гексанал (функціональна група у атома 2), 3-гексанал (функціональна група у атома 3).
Кислотна функціональна група
В органічних кислотах атом водню обмінюється на функціональну групу -КУХ. Для їх ідентифікації згадується слово кислота та додається закінчення -anoic, а також згадується атом вуглецю, де знаходиться функціональна група:
Приклади СН3COOH: метанова кислота: C2H5COOH етанова кислота; C.4H9COOH бутанова кислота або 2-бутанова кислота; C.6H13Гексанова кислота COH, 2-гексанова кислота (функціональна група у атома 2), 3-гексанова кислота (функціональна група у атома 3).



