20 أمثلة على الأميدات
أمثلة / / November 06, 2023
ال أميدات نكون المركبات الكيميائية العضوية مشتقات الأحماض الكربوكسيلية، حيث يتم استبدال مجموعة الهيدروكسيل (-OH) من مجموعة الكربوكسيل (-COOH) للحمض بمجموعة أمينية (-NH2، -NH-R، -N-(R)2، R هي أي سلسلة كربون).
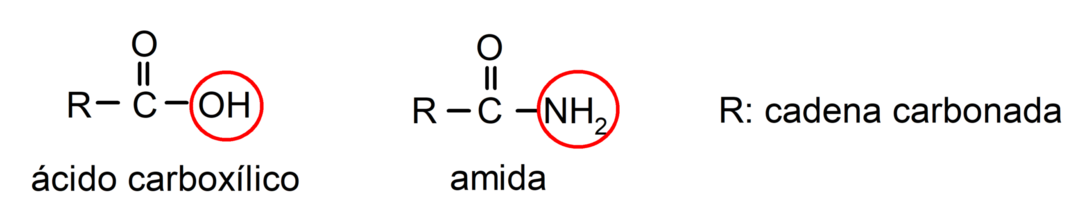
الأميدات هي جزيئات عضوية التي تحتوي على مجموعة الأميد التي تتكون من مجموعة كربونيل ومجموعة أمينية. على سبيل المثال: إيتاناميد، بروباناميد و ن-ميثيل-إيثاناميد.

- أنظر أيضا: الألدهيدات والكيتونات
أنواع الأميدات
يمكن تصنيف الأميدات وفقًا لعدد ذرات الهيدروجين (المرتبطة بنيتروجين المجموعة الأمينية) التي تم استبدالها بمجموعات بديلة مختلفة. وبهذا المعنى، هناك أميدات أولية وثانوية وثلاثية.
- الأميدات الأولية. وهي أميدات لا تحتوي على هيدروجينات المجموعة الأمينية المستبدلة. على سبيل المثال:

- أميدات ثانوية. وهي عبارة عن أميدات يتم فيها استبدال إحدى ذرات الهيدروجين من المجموعة الأمينية. على سبيل المثال:

- أميدات الدرجة الثالثة. وهي عبارة عن أميدات تحتوي على اثنين من ذرات الهيدروجين من المجموعة الأمينية المستبدلة. على سبيل المثال:

تسميات الأميدات
وفقًا للتسميات الشائعة، تتم تسمية الأميدات كمشتقات للأحماض الكربوكسيلية وفقًا للقواعد التالية:
- يقع الكربون المقابل لمجموعة الكربونيل في الموضع 1 ومن هذا الكربون يتم اختيار أطول سلسلة كربون. على سبيل المثال:

- تتم تسمية الأميدات الأولية باستخدام البادئة المقابلة لعدد ذرات الكربون في الحمض الكربوكسيلي الذي أدى إلى ظهورها. على سبيل المثال:

وفقا للاتحاد الدولي للكيمياء البحتة والتطبيقية (IUPAC)، الأمينات يتم تسميتهم باستخدام القواعد التالية:
- تتم تسمية الأميدات الثانوية والثالثية باستخدام البادئة المقابلة لعدد ذرات الكربون في الحمض الكربوكسيلي الذي أدى إلى ظهورها. علاوة على ذلك، لكل هيدروجين من المجموعة الأمينية التي تم استبدالها، يتم وضع N. وهكذا تتم تسمية البدائل المختلفة مع الإشارة إلى كميتها، وفي نهاية الاسم توضع كلمة أميد. على سبيل المثال:

- عندما يكون للجزيء مجموعات ذات أولوية بالنسبة لمجموعة الأميد، يتم تسمية الأميد كبديل. في هذه الحالات تسمى مجموعة الأميد كاربامويل. على سبيل المثال:
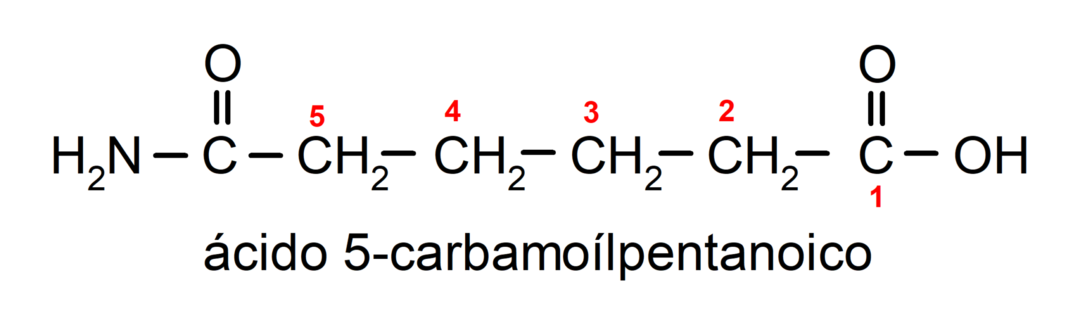
- عندما يتكون الجزيء من دورة ومجموعة أميد، تؤخذ الدورة كسلسلة رئيسية ويتم وضع اللاحقة - كربوكساميد. على سبيل المثال:

الخصائص الفيزيائية للأميدات
- تكون الأميدات صلبة في درجة حرارة الغرفة، باستثناء الميثاناميد.
- لديهم نقاط غليان عالية، حتى أعلى من تلك الخاصة بالأحماض الكربوكسيلية المقابلة.
- الأميدات مذيبات جيدة.
- وهي قواعد ضعيفة.
التفاعلات الكيميائية للأميدات
- تتفاعل الأميدات مع حمض مائي لتكوين حمض الكربوكسيل المقابل وملح الأمونيوم. على سبيل المثال:

- تتفاعل الأميدات مع القلويات لتكوين الحمض الكربوكسيلي المقابل وملح الكربوكسيل. على سبيل المثال:
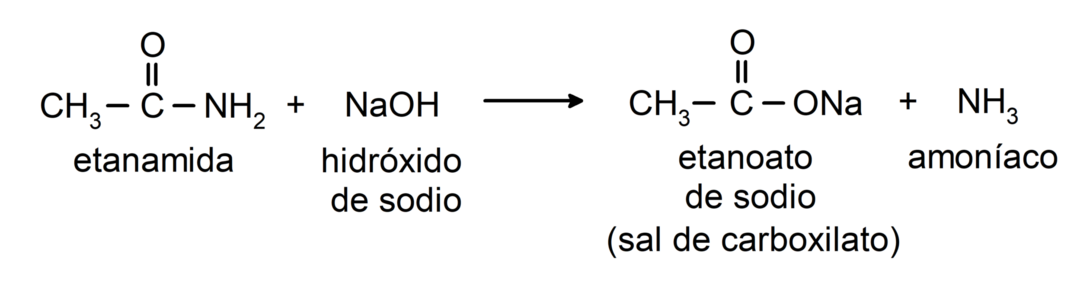
- يتم اختزال الأميدات إلى أمينات في وجود رباعي هيدريد ألومنيوم الليثيوم:
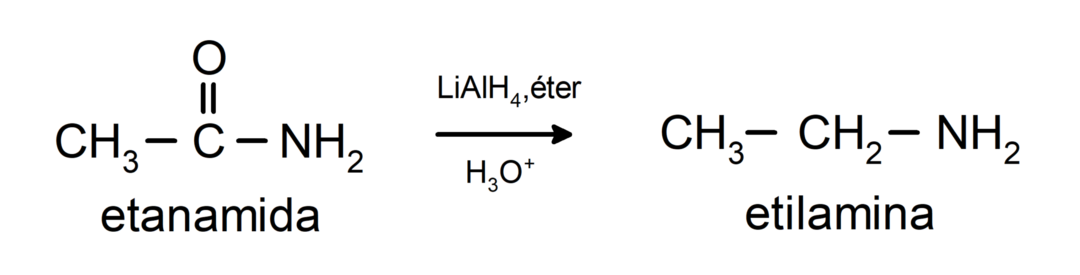
أمثلة على الأميدات
- فورماميد
- اليوريا
- نايلون
- ε-كابرولاكتام
- إيتاناميد
- بروباناميد
- بوتاناميد
- إيثانيدياميد
- ن-ميثيل-إيثاناميد
- ن-إيثيل-إيثاناميد
- ن-بروبيل-إيثاناميد
- N،N- ثنائي ميثيل بوتاناميد
- بنزين كاربوكساميد
- 4-برومو-3-ميثيل-سيكلوهكسان كاربوكساميد
- 3-هيدروكسي بوتاناميد
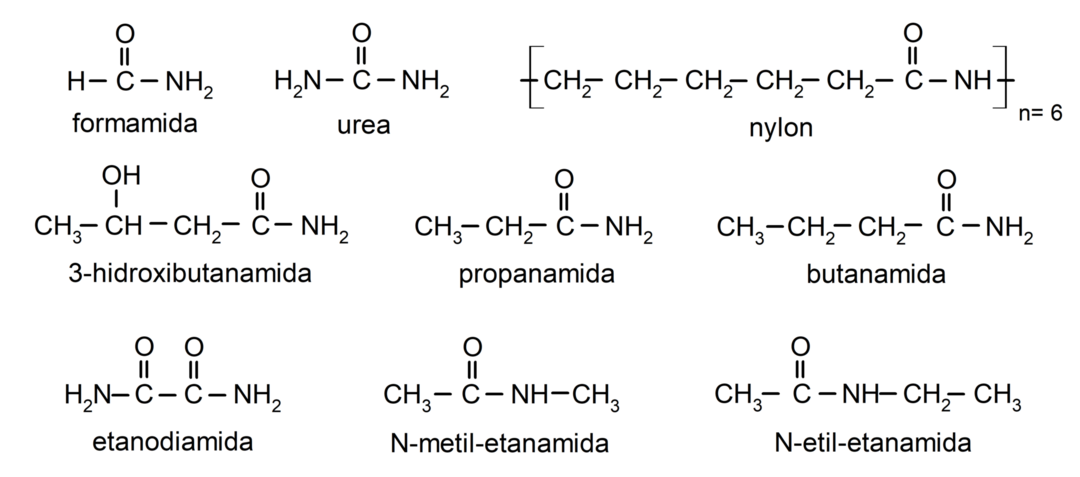

استخدامات الأميدات
تستخدم الأميدات على نطاق واسع في صناعة الأدوية. وبالإضافة إلى ذلك، يتم استخدامها كمكونات تحرير القالب في صناعة البلاستيك. من ناحية أخرى، يتم استخدامها كمستحلبات، السطحي والمذيبات. على سبيل المثال، اليوريا هي مادة أميدية تستخدم على نطاق واسع في صناعة الأدوية وصناعة النايلون.
مراجع
- راميريز بارون، S. ن.، ساينز-جاليندو، أ.، لوبيز-لوبيز، إل.، وكانتو-سيفوينتس، إل. (2013). الأميدات والتطبيق والتوليف. المجلة العلمية لجامعة كواهويلا المستقلة, 5(9).
- كاليري، س. سي، وباجنان، م. (2013). دراسة نظرية على التحلل المائي الحمضي للأميدات الأليفاتية والعطرية. المعلومات التكنولوجية, 24(3), 35-40.
- مارتينيز، ج. ح. م، جوميز، ل. و. ب، دي إسكوبار، م. إس، وإسكالانتي، ف. ل. (2002). الكيمياء العضوية. جامعة لاس بالماس دي غران كناريا، وكالة الجامعة للدراسات وجودة التدريس.
اتبع مع:
- الألدهيدات
- الكحوليات
- المغذيات الكبيرة والمغذيات الدقيقة
- المركبات العضوية وغير العضوية


