Пример за органична химия
Химия / / July 04, 2021
The Органична химия Това е частта от общата химия, която отговаря за изследването и функционалната класификация на химичните съединения, чийто структурен елемент е Въглерод, присъства в изобилие в жива материя; Това създава много диференцирана вселена на неорганичната химия, посветена на химичните съединения, класифицирани като минерали.
Въглеродният атом има четири електрона в последната обвивка на своята електронна конфигурация. Тази характеристика, заедно с тази на атомния му радиус, позволява тя да бъде свързана чрез ковалентни връзки с други атоми на един и същи елемент, в множество вериги, образуващи голямо разнообразие от химични съединения стабилен.
Можете да проверите Ковалентни връзки.
Такива химични съединения, в допълнение към въглеродните атоми, които им придават първоначалната структура, съдържат водородни атоми като основно допълнение за въглеродната валентност. В допълнение, в това разнообразие от съединения има такива с намесата на кислородни атоми, Азот, халогени, сяра и дори фосфор, алкални и алкалоземни елементи и метали на преход. В зависимост от това кой участва в молекулата, това ще бъдат физичните и химичните свойства на крайното вещество.
The органични съединения присъстват в целия жива материя; насърчаване и поддържане на всички биологични функции, за разлика от неорганичните или минералните вещества, които са били използвани от хората за търговски цели, за експерименти или за изпълнение на определени домашни задачи.
История на органичната химия
Преди 1828 г. вече се прави разлика между органична химия и неорганична химия. Органичната материя е свързана със сътворение чрез "жизнена сила", а към неорганичното с неживото, с минерала. Предвид тези концепции, не би могло да се очаква да се получат органични съединения от неорганични материали в лабораторията.
Въпреки това, през 1828 г. Фридрих Вьолер (1800-1882) успя да приготви органично вещество, Карбамид CO (NH2)2, важен продукт на животинския метаболизъм, от неорганични съединения. Лечение Оловен цианат Pb (CNO)2 с Амоняк NH3 да се получи Амониев цианат NH4CNO; Това съединение наистина се образува, но когато разтворът се вари, за да кристализира амониевият цианат, той се трансформира в карбамид.
Тази химическа промяна е пример за Вътрешно прегрупиране, при които броят или класът на атомите в молекулата не се променя, а само техният ред в нея. Тези видове трансформации са много често срещани в органичната химия.
Откритието на Wöhler инициира отказването от теорията за жизнената сила по-късно напълно изхвърлен, следван от приготвянето на много други органични съединения в лаборатория. Въпреки това, квалификаторите за неорганични и органични съществуват, тъй като неорганичните съединения са свързани с минерални продукти и органичните съединения, които всъщност са съединения от въглерод и водород и техните производни, са от вида, произведен от живите организми.
Въпреки че законите на общата химия се прилагат еднакво и за двете съединения, различни причини оправдават и правят необходимото това разделение. По този начин органичните и неорганичните съединения се различават по различни свойства, като: техните Разтворимост предпочитани в органични разтворители (етер, алкохол, хлороформ и др.) и съответно във вода Стабилност (органичните съединения се разлагат при относително ниски температури), и Същност на реакциите; за неорганичните съединения те са йонни, прости и практически мигновени, а за органичните съединения са ковалентни, сложни и бавни.
Органични съединения
Известни са въглеродни съединения с вериги до деветдесет атома. The вериги Въглеродните атоми могат да бъдат линейни и разклонени и имат единични ковалентни връзки или имат двойни или тройни връзки. Известно е, че повече от 2500 съединения съдържат само въглерод и водород (Въглеводороди).
Изомеризъм на органични съединения
В неорганичните съединения формулата обикновено представлява едно съединение; по този начин има само едно вещество с формула Н2ЮЗ4. Молекулата на сярна киселина съдържа два водородни атома, един от сярата и четири от кислорода, в специфично и уникално подреждане. В органичните съединения е рядко се случва това. Така например има две съединения, които реагират на формулата С2Н6Или етилов алкохол или етанол и диметилов етер.

Колкото по-сложна е молекулата, т.е. колкото по-голям е броят на въглеродните атоми, толкова по-голям е броят на възможните изомери.
Анализ на органични съединения
Анализът на органично съединение включва качествен анализ, количествен анализ и Функционален анализ. В случай че се предположи, че съединението е в нечисто състояние, то предварително се пречиства чрез Кристализация, Дестилация, Сублимация, Екстракцияи т.н. Критерият за чистота може да се прецени въз основа на неговите физически константи, като точка на топене, точка на кипене, плътност, разтворимост, кристална форма, индекс на пречупване и др.
The качествен анализ Проверява се чрез изследване на присъствието на елементите, които съставляват съединението, особено въглерод, водород и азот, а понякога и халогени, сяра и фосфор.
The количествен анализ Извършва се като се използват като основа методите, използвани за качествен анализ. Отправната точка е определено количество вещество, което се подлага на изгаряне и въглеродният диоксид се събира и претегля. въглерод и водни пари, образувани за изчисляване на процента на въглерод и водород в съединение. Резултатите от количествения анализ улесняват изчисляването на емпирична формула, въпреки че молекулната формула може да бъде намерена само след определяне на молекулното тегло на веществото. Но проблемът все още не е решен, тъй като една и съща молекулна формула може да съответства на различни изомери.
Класификация на органичните съединения
Според тяхната структура органичните съединения се разделят на съединения алифатен, ароматен Y. хетероциклична. Алифатните съединения са свързани с метан СН4, са с отворена верига, с изключение на циклопарафините, и дължат името си на факта, че животинските и растителните мазнини принадлежат към тази група.
The ароматни съединения, затворена верига, тясно свързана с бензола, C6Н6и те дължат името си на факта, че много от тях имат ароматни, приятни миризми.
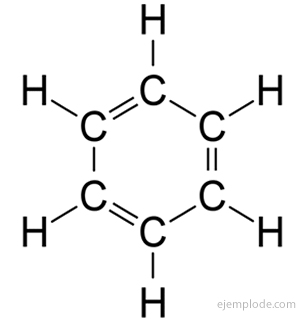
Бензенов пръстен
The хетероциклични съединения Те са съединения със затворена верига, в които в пръстена има елемент, различен от въглерод.
По своята конституция те са:
Въглеводороди, което от своя страна, поради вида на връзките, които има, се класифицира като Алкани, Алкени Y. Алкини. Освен това в тази категория са циклоалкани, бензен и техните производни, съставени само от въглерод и водород.
Хетероциклични съединения
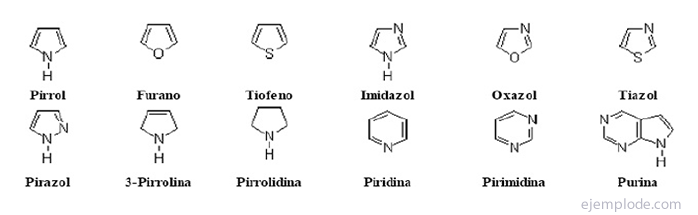
Халогенирани производни:R-X
Нитро съединения:R-NO2
Сулфонови киселини:R-SO3Н
Нитрили (ИЛИ алкил цианиди) и Изонитрили:R-CN и R-NC. Те се различават по начина, по който азотният атом е свързан в молекулата.
Алкохоли:R-OH
Феноли: Съединения на основата на скелет, състоящ се от бензенов пръстен с добавена хидроксилна група.

Етери:R-O-R
Меркаптани: R-SH
Тиоетери:R-S-R
Тиокиселини:R-COSH
Алдехиди:R-CHO
Кетони:R-CO-R
Карбоксилни киселини:R-COOH
Излизаш:R-COOM (М за метал)
Естери: R-COO-R
Анхидриди: R-CO-O-OC-R
Амини:R-NH2, R-NH-R, 2R-N-R
Въглехидрати тип Aldosa:-CHOH-CHOH-CHO
Въглехидрати от кетозен тип:-CHOH-CO-CH2О
Органометални съединения:R-M-R
Метал-алкил халогениди:R-MX (известен също като реактиви на Гринярд)



